Стафилококковый фолликулит
Общее лечение
При распространенных высыпаниях, хроническом течении, а также при наличии осложнений (синдром общей инфекционной интоксикации, регионарный лимфаденит и др.) назначают антибиотики в средних терапевтических дозировках:
Антибиотики группы пенициллина
Антибиотики группы цефалоспоринов
Антибиотики группы макролидов
Антибиотики группы тетрациклина
Доксициклина гидрохлорид, моногидрат 100 мг — детям старше 12 лет с массой тела менее 50 кг в 1-й день — 4 мг/кг массы тела 1 раз в сутки, в последующие дни — 2 мг/кг массы тела 1 раз в сутки. Детям старше 12 лет с массой тела более 50 кг и взрослым — в первые сутки 200 мг однократно, затем по 100 мг 1 раз в сутки. Курс лечения — 10–14 дней.
Фторхинолоны
Антибиотики группы аминогликозидов
Гентамицина сульфат раствор для инъекций 40 мг (1 мл) — детям до 2 лет — 2–5 мг/кг/сут, детям старше 2 лет — 3–5 мг/кг/сут. Кратность введения 3 раза в сутки. Взрослым 3–5 мг/кг/сут, кратность введения 2–4 раза в сутки. Курс лечения 7–10 дней.
Антибиотики группы линкозамидов
Клиндамицин 150 мг — при приеме внутрь детям по 3–6 мг/кг 4 раза в сутки, взрослым по 150–450 мг 4 раза в сутки; при парентеральном введении детям 15–40 мг/кг/сут, взрослым — 600 мг — 2,7 г в сутки, кратность введения 3–4 раза в сутки. Курс лечения — 10 дней.
Наружное лечение
Свежие невскрывшиеся папулы обрабатываются 50% раствором димексида, содержащим антибиотики (доксициклин или рифампицин), 4-5 раз в день, в качестве альтернативы можно использовать официнальный раствор эритромицина с цинком (зинерит). По периферии высыпаний проводят обработку кожи (от здоровой к поражённой) 1-2% борным (салициловым) спиртом 1 раз в день ежедневно в течение 3-4 недель.
Физиотерапия
Применяют местно УФО.
Критерии эффективности лечения
Отсутствие свежих высыпаний, разрешение существующих элементов.
Показания для госпитализации
Наличие осложнений (синдром общей инфекционной интоксикации, регионарный лимфаденит и др.), отсутствие эффекта от амбулаторного лечения.
Наиболее частые ошибки в лечении
Применение антибактериальных препаратов системного действия без проведения микробиологического посева гнойного содержимого с определением чувствительности к антибактериальным препаратам.
Абсцедирующий подрывающий фолликулит и перифолликулит Гоффмана и синдром фолликулярной окклюзии
В статье на основании обзора литературы описаны редкие дерматозы — абсцедирующий подрывающий фолликулит, перифолликулит Гоффмана и синдром фолликулярной окклюзии. На основании современной литературы и собственных наблюдений представлена клиническая и гист
On the basis of literature review, the article describes rare dermotosis — abscessed disruptive folliculitis, Hoffman’s perifolliculitis and follicular occlusion syndrome. On the basis of modern literature and personal observations, clinical and histological picture was presented, as well as modern ideas of etiology and pathogenesis of these diseases, and treatment methods.
Абсцедирующий подрывающий фолликулит и перифолликулит Гоффмана — воспалительное рецидивирующее заболевание кожи волосистой части головы, характеризующееся образованием абсцессов, с последующей рубцовой атрофией. Заболевание возникает преимущественно у мужчин, характеризуется длительным течением [1].
Причина абсцедирующего подрывающего фолликулита и перифолликулита Гофманна до конца не известна. Патофизиологические изменения в коже при этом заболевании связывают с фолликулярной окклюзией, расширением и разрывом фолликулярного канала, что приводит к воспалительной реакции. Бактериальная инфекция на высыпаниях развивается вторично и не является причиной этого заболевания [2, 3].
Клиническая картина заболевания представлена множественными болезненными узлами с гнойным отделяемым, которые, сливаясь, образуют взаимосвязанные абсцессы и пазухи (синусы) [1]. Процесс имеет типичные места локализации с поражением волосистой части головы (чаще теменной и затылочной областей), задней поверхности шеи. Пусковой механизм в формировании воспалительных элементов связывают с окклюзией сальных желез, что и объясняет характерное место локализации [4–7]. Согласно топографической анатомии на коже волосистой части головы расположены самые крупные сальные железы, с количеством до 5 долек, глубоко залегающие, с длинными извитыми протоками [8].
После разрешения воспалительного процесса остаются гипертрофические или атрофические рубцы кожи волосистой части головы, что приводит к ограниченным очагам рубцовой алопеции, локализующейся на местах воспаления [7].
Некоторые авторы указывают на возможность развития осложнений, таких как плоскоклеточный рак и краевой кератит [2, 3, 7, 9].
Диагностика абсцедирующего подрывающего фолликулита и перифолликулита Гоффмана основана на клинической картине, трихологическом исследовании, при необходимости гистологии.
Гистологическая картина заболевания зависит от степени воспаления. На ранней стадии наблюдается фолликулярный гиперкератоз с закупоркой и дилатацией фолликула. Вследствие этого возникает апоптоз и фолликулярный эпителий разрушается. В дальнейшем образуются инфильтраты из нейтрофилов, лимфоцитов и гистиоцитов. Позднее наблюдается образование абсцесса, приводящее к разрушению волосяного фолликула. Абсцессы могут проникать в дерму и подкожно-жировую клетчатку. При развитии процесса в дерме и подкожно-жировой клетчатке формируется грануляционная ткань, содержащая лимфоплазматический инфильтрат и гистиоциты, а также многоядерные гигантские клетки вокруг кератина и волосяных стержней. Процесс заживления завершается обширным фиброзом. На поздних стадиях отмечается рубцевание, фиброз, подкожные синусы, хронические гранулемы, которые представлены лимфоцитами, макрофагами, гигантскими клетками инородных тел, клетками плазмы крови [2, 4, 9, 10].
Методом трихоскопии можно обнаружить характерные признаки: «3D» («трехмерные») желтые точки в области дистрофичных волос, желтые аморфные области, белые точки с ореолами, молочно-красные области, не имеющие фолликулярных отверстий [4, 11].
Наблюдаемые нами пациенты с диагнозом «абсцедирующий подрывающий фолликулит» и «перифолликулит Гоффмана» представлены на фотографиях (рис. 1, 2). Клинические примеры демонстрируют абсцессы и гипертрофические рубцы на месте бывших высыпаний в области волосистой части головы у мужчин 23 и 28 лет. У представленных больных процесс локализовался только на волосистой части головы, кожа в других областях была не затронута, акне отсутствовали.
Абсцедирующий подрывающий перифолликулит может быть одним из симптомов, входящих в синдром фолликулярной окклюзии, который включает сочетание заболеваний кожи, сходных по патофизиологическим проявлениям: конглобатные акне, инверсные акне, абсцедирующий подрывающий перифолликулит, пилонидальная киста. В настоящее время в литературе описаны двойной синдром фолликулярной окклюзии, триада фолликулярной окклюзии и тетрада фолликулярной окклюзии.
Двойной синдром фолликулярной окклюзии сочетает абсцедирующий подрывающий перифолликулит и конглобатные акне. Клинический пример представлен на рис. 3. У мужчины 25 лет на коже волосистой части головы имеются гипертрофические рубцы на месте бывших высыпаний в области волосистой части головы, рубцы постакне на коже в области лица, акне 2–3 степени (рис. 3).
Триада фолликулярной окклюзии встречается у больных, имеющих конглобатные акне, абсцедирующий подрывающий перифолликулит и инверсные акне (или гидраденит), а при наличии пилонидальной кисты диагностируется как тетрада фолликулярной окклюзии [2, 9]. Точный патогенез этой группы заболеваний неизвестен, но данные свидетельствуют о том, что они имеют одинаковый патологический процесс, инициируемый фолликулярной окклюзией. В недавних исследованиях было показано, что цитокератин 17 (обнаруживаемый в норме в протоке сальной железы) отсутствует в эпителии протока сальной железы пациентов с инверсными акне, что способствует хрупкости эпителия и приводит к разрыву стенки фолликулярного протока [12].
Синдром фолликулярной окклюзии возникает чаще на третьем-четвертом десятке жизни у лиц мужского пола. Однако этот синдром описан в подростковом возрасте, а также у женщин [2, 9, 13]. По данным литературы, в редких случаях синдром фолликулярной окклюзии может сочетаться со спондилоартритом, остеомиелитом, болезнью Крона, грудинно-ключичным гиперостозом, синдромом Рейда (редкое сочетание кератита, ихтиоза и глухоты) [2, 9, 14].
Инверсные акне могут быть как самостоятельным заболеванием, а могут являться симптомом синдрома фолликулярной окклюзии. Согласно определению европейских клинических рекомендаций, инверсные акне — хронический, воспалительный, рецидивирующий дерматоз, с первичным поражением волосяного фолликула, возникающий после полового созревания и характеризующийся болезненными, глубокими высыпаниями, локализующимися в частях тела, где находятся апокриновые железы (подмышечные, паховые, аногенитальные области).
Инверсные акне впервые описаны в 1839 г. Velpeau, который первоначально назвал заболевание «гидраденит супуратива» (hidradenitis suppurativa), считая, что воспалительные изменения при этом заболевании происходят в потовых железах [2, 9]. В 1939 г. Brunsting на основании гистологического исследования доказал, что центральным звеном патогенеза гидраденита, подрывающего фолликулита головы и конглобатных акне является гиперкератоз фолликулярных протоков сально-волосяного фолликула [15]. В 1989 г. Plewigand и Steger ввели термин «инверсные акне», указывая на неверный термин «гидраденит», так как патогенетически имеет значение гиперкератоз фолликулярного протока, а не воспаление потовых желез. Отличием инверсных акне от вульгарных акне, помимо локализации, является отсутствие увеличения секреции сальных желез [13, 16].
В настоящее время определены диагностические критерии инверсных акне, в которых выделены основные и дополнительные.
2. Отсутствие патогенной флоры в мазке из отделяемого (только присутствие нормальной микробиоты) [7].
Выделяют несколько стадий инверсных акне:
Тяжелые варианты течения синдрома фолликулярной окклюзии ассоциированы с метаболическим синдромом, ожирением, употреблением в пищу большого количества простых углеводов, курением, мужским полом [7].
Нами представлены клинические случаи триады фолликулярной окклюзии на рис. 4, 5. Пациенты 43 и 52 лет обратились с жалобами на высыпания на коже волосистой части головы, лица, спины, груди, подмышечной области, в паху (рис. 4, 5). Пациенты имели схожие истории заболевания и клиническую картину. Считают себя больными с подросткового возраста, когда впервые появились высыпания на коже лица, груди и спины. Лечились амбулаторно с диагнозом «конглобатные акне». В возрасте около 30 лет стали появляться болезненные высыпания на коже в области волосистой части головы и подмышек. Пациенты лечились амбулаторно, доксициклин в течение 2–3 недель, эксцизия крупных узлов. Лечение приносило временное улучшение, ремиссия длилась менее полугода.
Дифференциальная диагностика абсцедирующего подрывающего фолликулита и перифолликулита Гоффмана
Дифференциальную диагностику необходимо проводить, в первую очередь, с заболеваниями, локализующимися на волосистой части головы. Акне-келоид (син.: сосочковый дерматит головы, склерозирующий фолликулит затылка) также наблюдается у мужчин в области затылка и на задней поверхности шеи. Первоначально появляются группы мелких фолликулярных пустул, которые располагаются в виде тяжа. Кожа вокруг них значительно уплотнена, кожные борозды резко выражены, в связи с чем создается впечатление существования сосочковых опухолей, волосы растут пучками. При разрешении фолликулов остаются келоидные рубцы. Процесс протекает медленно, без образования абсцессов [1]. Отсутствие флуктуирующих узелков, крупных абсцедирующих образований, фистульных ходов является основным отличием акне-келоид от абсцедирующего подрывающего фолликулита и перифолликулита Гоффмана.
Часто случаи рубцовых алопеций, обусловленные предшествующими фолликулитами, обычно диагностируют как абсцедирующий и подрывающий перифолликулит Гоффмана. Декальвирующий (эпилирующий) фолликулит впервые был описан в 1888 г. Quinqaud. Декальвирующий фолликулит также встречается у взрослых и чаще у мужчин. Поражения при декальвирующем фолликулите обычно располагаются на волосистой части головы, однако иногда могут локализоваться на других частях тела, покрытых волосами: борода, подмышечная область, лобок. Процесс начинается с фолликулита, окруженного зоной эритемы. После разрешения воспаления образуются небольшие округлые или овальные очаги рубцовой атрофии. Сливаясь между собой, мелкие очаги становятся крупнее, обычно сохраняя округлые очертания. Старые участки, на которых воспалительный процесс завершился, представлены зонами рубцовой атрофии. Таким образом, клиническая картина представлена небольшими очагами рубцовой алопеции с пучками, состоящими из 5–10 волос, выходящих из расширенных фолликулярных отверстий.
Микотическое поражение волосистой части головы характеризуется отсутствием островоспалительных явлений и положительной грибковой культурой.
Другие состояния, которые могут имитировать абсцедирующий подрывающий фолликулит и перифолликулит Гоффмана, включают злокачественные пролиферирующие пилярные кисты, фолликулотропные грибовидные микозы с крупными клеточными трансформациями, эрозивно-пустулезный дерматоз кожи головы [4, 18, 19].
Лечение абсцедирующего подрывающего фолликулита и перифолликулита Гоффмана и синдрома фолликулярной окклюзии
Терапия синдрома фолликулярной окклюзии, как правило, начинается с лечения антибактериальными препаратами, назначаемыми внутрь (тетрациклин, клиндамицин, рифампицин) и наружно (клиндамицин). Некоторые авторы рекомендуют ципрофлоксацин 250–500 мг или клиндамицин и рифампицин по 300 мг [20].
Тем не менее антибактериальная терапия имеет кратковременный эффект. По мнению некоторых авторов более эффективно сочетать антибиотикотерапию с инъекциями кортикостероидов в очаги поражения [21]. Для лечения устойчивых к терапии случаев рекомендуется применять дапсон 50–150 мг в сутки [13].
Однако, по данным литературы, часто приходится прибегать к хирургическому вмешательству. Хирургическое лечение проводится на фоне антибактериальной терапии с полной резекцией пораженной кожи волосистой части головы в поэтапных процедурах с последующей реконструкцией кожи [22].
В настоящее время большинство публикаций, посвященных лечению фолликулярной окклюзии, утверждают о высокой эффективности изотретиноина в терапии данного дерматоза. Изотретиноин рекомендуется назначать в тех же дозировках, как и при вульгарных акне, — 0,5–1 мг/кг в течение 3–12 месяцев [20, 21].
Некоторые авторы рекомендуют сочетание антибиотиков внутрь и местное применение изотретиноина [20, 21].
В современной литературе имеются единичные публикации, демонстрирующие высокую эффективность генно-инженерных биологических препаратов, таких как адалимумаб, инфлексимаб, которые предлагаются в качестве третьей линии терапии [23, 24].
Под нашим наблюдением находился пациент 52 лет с триадой фолликулярной окклюзии (конглобатные акне, абсцедирующий подрывающий перифолликулит и инверсные акне), получавший лечение изотретиноином в дозе 30 мг в сутки в течение 6 месяцев. В результате терапии отмечалась длительная ремиссия в течение года. На фотографиях представлены результаты терапии через 2 месяца приема препарата (рис. 6). Процесс полностью разрешился, представлен поствоспалительными пятнами и гипертрофическими рубцами.
Таким образом, представленные клинические случаи демонстрируют различные варианты синдрома фолликулярной окклюзии, в результате которого на коже образуются узлы различного характера (воспалительные или невоспалительные), абсцессы и, как следствие воспалительного процесса, формирование различных рубцов. В настоящее время наиболее эффективным препаратом для лечения абсцедирующего подрывающего фолликулита и перифолликулита Гоффмана и синдрома фолликулярной окклюзии является изотретиноин в дозировках, рекомендуемых инструкцией.
Литература
ФГОУ ДПО РМАПО, Москва
Фолликулит
Фолликулит — инфекционный процесс, развивающийся в средних и глубоких отделах волосяных фолликулов человека. Патология сопровождается образованием множественных пустул с гнойным содержимым. Возбудителем заболевания могу стать бактерии, вирусы, грибки и паразиты. По мере развития инфекции количество пустул на коже пациента увеличивается. При вскрытии первичного очага образуются язвы, при их заживлении — мелкие рубцы.
Общая информация
Патология широко распространена среди жителей стран с высокой влажностью и температурой воздуха. Подобные климатические условия способствуют распространению инфекционных поражений волосяных фолликулов. Группа риска представлена социально неблагополучными слоями населения: несоблюдение человеком правил личной гигиены приводит к активному размножению патогенов на кожных покровах.
Часто причинами фолликулита становятся поверхностные воспаления фолликулов — остиофолликулиты. Распространение инфекции в нижние отделы фолликула приводит к образованию гнойных пустул.
Причины развития патологии
Патогены попадают в фолликулы через поврежденные участки: царапины и ссадины. Инфицированию подвержены лица, страдающие от зудящих дерматитов и повышенной потливости. Ослабление иммунитета пациента приводит к проникновению инфекции в волосяные луковицы. По этой причине дерматологи рекомендуют соблюдать профилактические меры мужчинам и женщинам с диагностированным сахарным диабетом и хроническими инфекциями. Часто заболевание проявляется у ВИЧ-инфицированных людей и пациентов, принимающих иммунодепрессанты.
Виды патологии
В процессе диагностики фолликулита дерматологи определяют форму заболевания, которой страдает пациент. Так, стафилококковый тип патологии часто локализуется на лице мужчин, затрагивая подбородок и кожу вокруг губ. Инфицирование происходит в процессе бритья щетинистых волос.
Псевдомонадная форма заболевания становится следствием купания пациента в горячей воде с недостаточным уровнем хлорирования. Жар способствует раскрытию пор, в которые попадают возбудители инфекции. Очаги воспаления образуются на лице и верхней части туловища ребенка или взрослого.
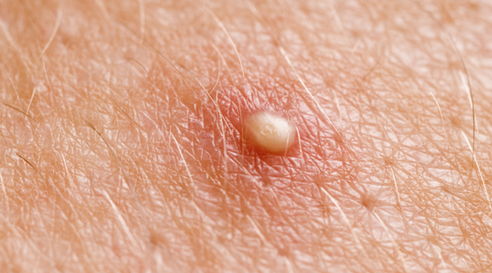
Герпетический тип инфекций волосяных луковиц поражает кожу подбородка и носогубного треугольника пациентов. Характеризуется образованием крупных везикул в фолликулярных устьях.
Кандидозная форма патологии проявляется при наложении на кожные покровы пациента окклюзионных повязок, препятствующих попаданию в рану на грудной клетке патогенной микрофлоры.
Гонорейный вид заболевания становится осложнением гонококковой инфекции. Пустулы формируются в промежности (у женщин) и на крайней плоти (у мужчин).
Фолликулит, вызванный клещами, может локализоваться на любых участках кожных покровов человека. Деятельность Demodex folliculorum и Demodex brevis приводит к образованию скоплений мелких пустул.
Симптоматика патологии
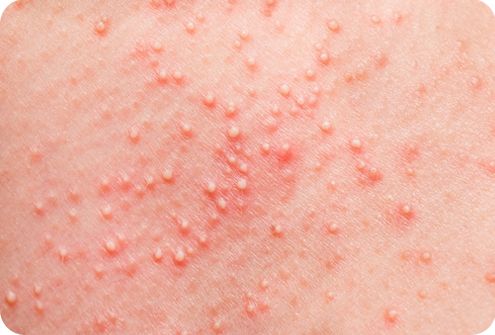
В 80% клинически диагностируемых случаев заболевания на кожных покровах пациентов образовываются множественные пустулы. Распространенными местами их локализации становятся лицо, волосистая часть головы, подмышечные впадины, лобок, внутренняя поверхность бедер. Выраженная болезненность и зуд появляются после образования крупного скопления пустул. При отсутствии медицинской помощи и отказе от соблюдения правил личной гигиены пациент может столкнуться с осложнениями: абсцессами, флегмонами и гидраденитом.
Диагностика

Дифференциальная диагностика позволяет врачам исключить из анамнеза пациента медикаментозную токсикодермию, розовый лишай, стрептококковое импетиго, фурункулез и остиофолликулит.
Лечение

Местная терапия при лечении локализованного на лице фолликулита эффективна на начальной стадии заболевания. При появлении множественных пустул пациенту потребуется обработать высыпания спиртовыми растворами зеленки или фукарцина. Остановить распространение инфекции можно при регулярной обработке кожных покровов салициловым или борным спиртом. Вспомогательной терапевтической мерой становится ультрафиолетовое облучение тела и конечностей ребенка или взрослого.
Осложненное течение патологии требуют комплексной терапии, направленной на лечение заболевания-первопричины фолликулита — гонореи или сифилиса.
Диагностика и лечение фолликулита в Москве
АО «Медицина» (клиника академика Ройтберга) обладает всем необходимым оборудованием для диагностики и лечения инфекционных поражений волосяных фолликулов. Прием пациентов осуществляется в современном диагностическом комплексе, построенном с учетом последних достижений медицины.
Вопросы и ответы
Какой врач лечит инфекции волосяных луковиц человека?
— Лечение патологии осуществляется дерматологом. При осложненном течении заболевания пациенту могут потребоваться консультации с другими врачами — венерологом, иммунологом, терапевтом.
Существуют ли меры по профилактике фолликулита?
— Взрослым и детям рекомендуется избегать контактов с химическими веществами, которые могут привести к повреждениям кожи и проникновению патогенов к волосяным фолликулам. Лицам, страдающим от сахарного диабета и повышенного потоотделения, следует тщательно соблюдать правила личной гигиены.
Передается ли инфекция от носителя к здоровому человеку?
— Вероятность инфицирования здорового человека при контакте с носителем заболевания существует. По этой причине дерматологи не рекомендуют детям и взрослым пользоваться общими полотенцами и средствами личной гигиены.
Фолликулиты и резистентность к антибактериальной терапии: как лечить?
Одним из частых заболеваний кожных покровов с особенной устойчивостью к терапии является фолликулит. Хроническое течение характерно для фолликулитов, вызванных, в частности, стафилококками. В данной статье представлено исследование препарата, который с ус
One of the most common skin diseases, remarkably resistant to the therapy is folliculitis. The chronic process is typical for folliculitis caused, in particular, by Staphylococcus aureus. This article presents a study of the drug which can be successfully used against antibiotic resistance.
С 1928 года, когда А. Флемингом был открыт первый антибиотик пенициллин, до настоящего времени группа антибактериальных препаратов значительно увеличилась. Антибиотики стали чрезвычайно популярны. Порой их назначение не оправдано, зачастую пациенты самовольно назначают себе антибактериальную терапию, что в конечном итоге привело к тому, что медицинское сообщество столкнулось с такой сложной проблемой, как резистентность к антибиотикотерапии. Основой терапевтического действия антибактериальных препаратов является подавление жизнедеятельности возбудителя инфекционной болезни в результате угнетения более или менее специфичного для микроорганизмов метаболического процесса. Угнетение происходит в результате связывания антибиотика с мишенью, в качестве которой может выступать либо фермент, либо структурная молекула микроорганизма.
Резистентность микроорганизмов к антибиотикам может быть природной и приобретенной.
Истинная природная устойчивость характеризуется отсутствием у микроорганизмов мишени действия антибиотика или недоступностью мишени вследствие первично низкой проницаемости или ферментативной инактивации. При наличии у бактерий природной устойчивости антибиотики клинически неэффективны. Природная резистентность является постоянным видовым признаком микроорганизмов и легко прогнозируется.
Под приобретенной устойчивостью понимают свойство отдельных штаммов бактерий сохранять жизнеспособность при воздействии таких концентраций антибиотиков, которые подавляют основную часть микробной популяции. Возможны ситуации, когда большая часть микробной популяции проявляет приобретенную устойчивость. Появление у бактерий приобретенной резистентности не обязательно сопровождается снижением клинической эффективности антибиотика. Формирование резистентности во всех случаях обусловлено генетически: приобретением новой генетической информации или изменением уровня экспрессии собственных генов.
Известны следующие биохимические механизмы приобретенной устойчивости бактерий к антибиотикам:
1) модификация мишени действия;
2) инактивация антибиотика;
3) активное выведение антибиотика из микробной клетки (эффлюкс);
4) нарушение проницаемости внешних структур микробной клетки;
5) формирование метаболического «шунта».
Механизмы резистентности могут быть различны, например, микроорганизм непроницаем для антибиотика (большинство грамотрицательных бактерий невосприимчивы к пенициллину G, поскольку клеточная стенка защищена дополнительной мембраной). Одной из возможных причин приобретенной резистентности может являться то, что микроорганизм в состоянии переводить антибиотик в неактивную форму (многие виды Staphylococcus spp. содержат фермент β-лактамазу, который разрушает β-лактамное кольцо большинства пенициллинов), или вследствие генных мутаций обмен веществ микроорганизма может измениться таким образом, что блокируемые антибиотиком реакции больше не являются критичными для жизнедеятельности организма [1].
Одним из основных механизмов жизненного цикла микроорганизмов, организации формы их существования в окружающей среде и резистентности к ее агрессивным условиям является способность к образованию биопленок. Согласно современным представлениям, биопленка — это совокупность микроорганизмов, в составе которой бактерии взаимодействуют друг с другом, что способствует повышению их устойчивости к факторам внешней среды. Биопленка состоит из непрерывного мультислоя бактериальных клеток, прикрепленных к поверхности раздела фаз и друг к другу и заключенных в биополимерный матрикс [2, 3]. Способностью к образованию биопленок обладает большое количество микроорганизмов, являющихся этиологическими агентами инфекционных, дерматологических, урогенитальных и других заболеваний. Наиболее изученными видами бактерий, образующих биопленки, являются стафилококки, представители семейства Enterobacteriaceae, Pseudomonas aeruginosa, генитальные микоплазмы [4].
Известно, что матрикс биопленки способен препятствовать скорости диффузии некоторых антибиотиков и других биоцидных препаратов, что зависит от его биохимического состава и метаболической активности популяции. Например, аминогликозиды, как отмечается в ряде работ, достаточно длительно диффундируют через матрикс, фторхинолоны, напротив, легко проникают через этот барьер [5–7]. По данным R. Shafreen, левофлоксацин способен проникать в биопленку, сформированную не только бактериями, но и дрожжеподобными грибами Candida albicans, нарушать их биосинтетическую активность, тем самым разрушая структурную организацию грибкового сообщества [8].
Долгие годы оставался малоизученным вопрос о причинах восстановления популяции микроорганизмов после полноценно проведенного курса антибиотикотерапии. Исследования показали, что в культуре бактерий сохраняется небольшая часть клеток, которые проявляют устойчивость к антибиотику, несмотря на то, что остальная популяция чувствительна к его действию [6, 9, 10]. В процессе изучения данной проблемы биологами и генетиками была выявлена субпопуляция клеток, которые впоследствии были названы персистерами. Персистеры — клетки, составляющие 1–5% всей бактериальной массы биотопа, которые образуются в стационарной фазе роста, не проявляют метаболической активности и обеспечивают выживание материнской популяции в присутствии летальных для других клеток факторов. Они замедляют все физиологические процессы и становятся толерантными к действию разных факторов, в том числе антимикробных препаратов. В данном ракурсе понятие антибиотикотолерантности отличается от антибиотикорезистентности. Антибиотики способны оказывать свое действие, влияя на мишени в делящейся и метаболически активной клетке. Стадия физиологического покоя позволяет сохранить часть популяции микроорганизмов и при благоприятных для нее условиях полностью регенерировать [11–14].
Одним из частых заболеваний кожных покровов с особенной устойчивостью к терапии является фолликулит. Фолликулит (folliculitis) — одна из форм пиодермии, которая возникает в волосяном фолликуле. Причиной воспалительного процесса может быть бактериальный, грибковый или вирусный агент. Если не устранены провоцирующие факторы, фолликулит рецидивирует и может стать хроническим. Хроническое течение характерно для фолликулитов, вызванных стафилококками и грибами-дерматофитами. Факторы, провоцирующие развитие фолликулитов:
В лечении стафилококкового фолликулита традиционно используют антибактериальные мази (например, мупироцин), которые наносят на пораженные участки кожи. Прием антибиотиков показан при хроническом течении фолликулита, распространенном процессе, воспалении регионарных лимфатических узлов, недостаточной эффективности местного лечения. Но и в этом случае зачастую невозможно избежать рецидивирования.
В связи с этим было принято решение о поиске средства, способного снизить резистентность бактерий к антибактериальному лечению. Был проведен анализ современной научной литературы, в которой отражалось действие различных антисептиков на рост и размножение бактерий in vitro. По результатам литературного поиска для проведения исследования эффективности антибиотикотерапии рецидивирующего стафилококкового фолликулита был выбран препарат Мирамистин® (группировочное название — бензилдиметил-миристоиламино-пропиламмоний, химическое название — бензилдиметил[3(миристоиламино)пропил]аммоний хлорид моногидрат).
В основе биологического действия препарата Мирамистин® лежит воздействие на клеточные мембраны бактериальных клеток. В результате воздействия препарата происходит нарушение структуры и функции мембран бактериальных клеток, нарушение их осмотического баланса и быстрый лизис. Мирамистин® не воздействует на оболочки клеток человека, поскольку составляющие их липиды имеют значительно большую длину радикалов, и гидрофобных взаимодействий с молекулами препарата Мирамистин® не происходит. Мирамистин® обладает выраженным антимикробным действием в отношении грамположительных и грамотрицательных, аэробных и анаэробных, спорообразующих и аспорогенных бактерий в виде монокультур и микробных ассоциаций, включая госпитальные штаммы с полирезистентностью к антибиотикам. Под действием препарата Мирамистин® снижается устойчивость бактерий и грибов к антибиотикам [15, 16].
Группой ученых были проведены серии экспериментов in vitro, где изучалось влияние бензилдиметил-миристоиламино-пропиламмония на бактерии S. аureus, находящиеся в состоянии как биопленки, так и в обособленных формах. В ходе исследования были получены данные, что, находясь в биопленке, микроорганизмы проявляли большую устойчивость к действию распространенных в практике растворов антисептиков. Вне зависимости от формы существования микроорганизма бензилдиметил-миристоиламино-пропиламмоний оказывал бактерицидный эффект на S. аureus, в том числе MRSA (метицилинорезистентный Staphylococcus aureus) [17]. Бензилдиметил-миристоиламино-пропиламмоний в концентрации 5 мкг/мл и выше обладал 100% бактерицидной активностью в отношении S. аureus [16, 18].
Целью настоящего исследования было оценить эффективность, переносимость, безопасность и удобство применения раствора для местного применения препарата Мирамистин® (бензилдиметил [3-(миристоиламино)пропил]аммоний хлорид моногидрат) при фолликулитах, устойчивых к базовой терапии топическими антибиотиками.
Материалы и методы исследования
В качестве методов оценки эффективности терапии использовались индекс DIDS (Dermatology Index of Disease Severity, дерматологический индекс тяжести заболевания) и индекс DLQI (Dermatology Life Quality Index, дерматологический индекс качества жизни).
В рандомизированном, когортном, контролируемом, простом слепом исследовании участвовали 38 человек, страдающих устойчивыми формами бактериальных фолликулитов. Под наблюдением находились 22 женщины и 16 мужчин в возрасте от 20 до 48 лет. В исследование включались пациенты с диагнозом «фолликулит различной локализации», инфекционным агентом в котором выступал культурально подтвержденный S. аureus с отсутствием значимой терапевтической динамики от использования различных наружных антибактериальных препаратов. Не допускалось включение в исследование пациентов, использовавших любые другие препараты для лечения пиодермии, включая системные, в течение одного месяца до начала терапии или использовавших системные антибиотики в течение одной недели до начала исследования. В исследование не включались больные, соответствующие хотя бы одному из следующих критериев: беременные или кормящие женщины, имеющие гиперчувствительность к действующему веществу или компонентам препарата (в анамнезе или при назначении в текущем исследовании), применяющие системные или наружные антибиотики, глюкокортикостероиды, противогрибковые средства (в период лечения исследуемым препаратом), носители вирусных инфекций, подлежащие вакцинации (в период лечения исследуемым препаратом).
До начала лечения все пациенты проходили инструктаж по применению исследуемого препарата, подписывали форму информированного согласия, по каждому пациенту подробно велась амбулаторная карта. Типовая картина заболевания у пациента с фолликулитом, вызванным S. aureus, представлена на рис. 1. В течение 7 дней пациенты лечились самостоятельно. Терапия была комбинированной: крем, в составе которого метилурацил и хлорамфеникол, и спрей Мирамистин® (0,01%). Схема лечения: аппликация крема 1 раз/сут тонким слоем на весь пораженный участок кожных покровов, а также двукратное орошение в день спреем Мирамистин®. Данные назначения были даны в строгом соответствии с инструкцией препарата. Препарат назначался до полного разрешения симптомов, но не более двух недель (ни у одного из участников исследования симптомы не сохранялись более 9 дней). Первое нанесение препарата осуществлялось пациентами под надзором медицинского персонала. В последующем пациенты лечились самостоятельно, нанося исследуемый препарат 2 раза в день согласно представленным им письменным инструкциям.
В качестве метода оценки эффективности терапии использовался индекс DIDS (Dermatology Index of Disease Severity, дерматологический индекс тяжести заболевания), который был предложен исследователями медицинского центра университета Индианы (США) для оценки степени тяжести воспалительных кожных заболеваний с учетом площади поражения кожи и степени функциональных ограничений. Первый компонент индекса — оценка степени поражения поверхности тела (рис. 2).
Для каждого пациента индивидуально высчитывались проценты по каждому параметру до лечения и по истечении одной недели от начала терапии. После чего высчитывалось среднеарифметическое значение по каждому параметру, которое приобрело не целое, а дробное значение.
Общие принципы подхода к оценке:
К моменту начала лечения среднеарифметическое значение степени поражения поверхности тела составило 14,74%, при этом с 5% площадью поражения поверхности тела было 12 человек, с 10% — 6, с 20% — 18, с 40% — 2. К концу первой недели от начала терапии динамика была следующей: с 5% площадью поражения поверхности тела — 1 человек, с 10% — 3, с 20% — 2, с 40% — 0, а среднеарифметическое значение — 1,97%. Пациент с типовой картиной фолликулита спустя 5 дней комбинированной терапии представлен на рис. 3.
Функциональная ограниченность при выполнении повседневных действий в быту и на работе являлась вторым компонентом оценки тяжести заболевания при использовании индекса DIDS (таблица):
Исходя из данных табл., к моменту начала лечения среднеарифметическое значение степени тяжести заболевания по индексу DIDS составило 1,74, а к концу первой недели — 0,29.
Важным параметром для каждого человека, считающего себя больным, является так называемый уровень качества жизни, для оценки которого авторы исследования использовали индекс DLQI (Dermatology Life Quality Index, дерматологический индекс качества жизни). Данный индекс рассчитан для применения у пациентов старше 16 лет. Анкета заполнялась больным самостоятельно, на заполнение требовалось не более 1–2 минут. Цель анкеты — измерить, насколько проблемы с кожей повлияли на качество жизни за последнюю неделю до лечения и спустя две недели от начала лечения, за исключением последнего пункта. Оценка влияния лечебных процедур на порядок жизни давалась за последнюю неделю до лечения и за неделю самого лечения. Детальный анализ индекса DLQI проводился по шести разделам: 1) симптомы и ощущения (максимум 6 баллов); 2) повседневная деятельность (максимум 6 баллов); 3) отдых и досуг (максимум 6 баллов); 4) работа и учеба (максимум 3 балла); 5) межличностные отношения (максимум 6 баллов); 6) лечение (максимум 3 балла). По каждому показателю высчитывалось среднеарифметическое значение. Результаты измерения качества жизни представлены на рис. 4.
Результаты и их обсуждение
Срок наблюдения составил 2 недели, при этом длительность терапии и клиническое выздоровление большинства пациентов составили 7 дней. Длительность терапии определялась в основном площадью поражения и степенью тяжести клинической картины в начале терапии. Зачастую после лечения на коже в местах поражений отмечались постэруптивные элементы (пятна гиперпигментации, эритематозные пятна), которые со временем разрешались. В статье приведено фото пациента с разрешившимся после лечения фолликулитом, на котором отсутствуют воспалительные элементы, свежих высыпаний нет, наблюдаются постэруптивные элементы (рис. 3). В целом в нашей программе отмечалась высокая комплаентность пациентов. Соблюдение назначенной терапии зафиксировано у 97% участников программы. Это соответствует мировым данным о влиянии различных факторов на приверженность пациентов лечению. Переносимость спрея Мирамистин® по оценке врачей в подавляющем числе случаев была «хорошей», «очень хорошей» и «отличной» у 93% пациентов.
Заключение
В проведенном исследовании установлено, что раствор для местного применения Мирамистин®, основное действующее вещество которого — бензилдиметил [3-(миристоиламино)пропил]аммоний хлорид моногидрат, является эффективным и легко переносимым, а также косметически приемлемым средством борьбы с устойчивыми к антибиотикотерапии фолликулитами. По результатам исследования можно сделать вывод, что оптимальным режимом применения препарата является орошение спреем Мирамистин® два раза в сутки, при этом в подавляющем большинстве случаев достаточно одной недели терапии. Подобная схема лечения способствует хорошей комплаентности. Исходя из этих данных спрей Мирамистин® может быть рекомендован к широкому использованию для комбинированного лечения устойчивых форм фолликулитов различных локализаций.
Литература
* НИИ МПиТМ им. Е. И. Марциновского ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
** ФГБУ «Поликлиника № 5» УДП РФ, Москва
*** ФГБОУ ДПО ИПК ФМБА России, Москва
.jpg)
.jpg)
.jpg)
_575.jpg)

.jpg)
.gif)
.jpg)
_575.gif)
.gif)


