Герпес: что это и какие препараты применять?
Герпес в переводе с греческого «ползущий». На данный момент актуальность этого заболевания не уменьшилась. Оно встречается более чем у 90% населения.
Что такое герпес
Как понять, что это именно герпес?
Но для достоверного подтверждения диагноза необходим анализ крови на наличие специфической реакции организма на вирус (IgM) он будет говорить о том, что на момент сдачи крови у вас протекает острый период болезни.
При генитальном герпесе, также берут на исследование выделения из половых путей и уретры. Обязательна консультация специалиста (дерматовенеролога).
Стоит обратить внимание, что вирус не выводится из организма после перенесенной ветрянки, а остается «жить» в определенном отделе нашей нервной системы, поэтому сдавать анализ на Ig G не имеет смысла.
Как можно заразиться
Заражение происходит через слизистые:
То есть чаще всего заражение происходит при несоблюдении гигиены и защиты при половом акте. Так же при расчесывании уже появившихся пузырьков происходит занос на новые участки кожи и слизистых.
Отдельный путь заражения от матери к плоду, на данный момент является обязательным обследование на ВПГ-1,2 у планирующих беременность и беременных женщин.
Инфекция поражает нервную систему и опасна своими последствиями для организма.
Как себя вести при герпесе

Препараты
Рассмотрим подробно группы препаратов для лечения
Данная группа препаратов воздействуют непосредственно на причину, сам вирус. Курс и схему приема назначает врач после комплексного обследования.
Переносимость препаратов достаточно хорошая, противопоказаны при беременности и кормлении грудью. Так же осторожно и под контролем врача применение у лиц с почечной и печеночной недостаточностью. Детям дозу определяет педиатр исходя из расчета по весу.
2. Препараты интерферона:
Противопоказаний у данной группы практически нет. Она является основным способом лечения такой уязвимой группы как беременные и кормящие женщины.
Используют для стимуляции выработки собственного интерферона и избежания усугубления течения и распространения инфекции. Переносится достаточно хорошо. Противопоказания у каждого препарата определенный возраст указанный в инструкции.
Данные препараты применяются при герпетических поражения слизистой рта, обладают антибактериальным, противовирусным действием, а также снимают воспаление и обезболивают.
Обладают местным противовирусным действием, Зовиракс Дуо Актив в сочетании с гормоном гидрокортизоном дает быстрое снятие воспаления и соответственно боли, также не дает образоваться новым пузырькам. Но так как в составе гормональная составляющая, очень внимательно необходимо прочитать инструкцию. Только с 12 лет. Перед применением любых мазей и гелей необходимо очистить кожу от косметики и загрязнений.
Только под контролем иммунолога.
Снимают боль, воспаление и так же при необходимости температуру.
Помогают избежать отечности.
Также отдельно можно выделить вакцину против герпеса. Показана она взрослым, которые болеют герпесом более 3 раз в год и высоким титром антител, пожилым лицам, ВИЧ-инфицированным. Также детям которые не переболели ветрянкой.
Лечение беременных женщин выбирается в зависимости от срока беременности, строго акушером-гинекологом и зависит от степени тяжести течения!
Герпес-является комплексной проблемой. Причиной повторяющегося или впервые возникшего герпеса является снижение иммунитета, гормональные изменения.
Главной профилактикой является поддержание работы иммунитета:
Федеральные клинические рекомендации по ведению больных генитальным герпесом- Москва 2015; Клинические рекомендации простой герпес у взрослых-2014 год;
Герпесвирусные инфекции при грудном вскармливании
Проявление герпесвирусной инфекции во время кормления грудью — довольно распространенная проблема. Поэтому многие мамы пугаются при появлении симптомов заболевания и испытывают сомнения, можно ли продолжать кормление ребенка грудью и как лечить данное заболевание, не навредив ребенку. Ответы на эти и некоторые другие вопросы изложим в данной статье.
Вирусы герпеса присутствуют в организме каждого взрослого человека. Но, для того чтобы, появились внешние проявления заболевания, нужны определенные условия. Герпес (Herpes) – с греческого переводится как «ползучая, склонная к распространению болезнь кожи». Вирус активизируется только в том организме, в котором защитные механизмы ослаблены. Именно организм кормящей женщины испытывает напряжение всех звеньев иммунитета после беременности и родов, которые являются стрессом для организма. Гиповитаминоз, несбалансированное питание и отсутствие полноценного сна и отдыха, а также ряд других факторов способствуют проявлению болезни. Именно поэтому 70% женского здорового населения сталкиваются с данным заболеванием после родов и в период грудного вскармливания.
Пути передачи герпесвирусных инфекций
Выделяют 8 видов вируса, каждый из которых опасен по своему, а именно:
1 тип — «простой» герпес (ВПГ 1) — самый распространенный вид герпеса, который проявляется пузырьковыми высыпаниями (везикулы) на губах, слизистых глаз, полости носа и на других участках тела, в том числе и на сосках. Появление сыпи сопровождается зудом, припухлостью кожи и болью различной интенсивности.
2 тип — генитальный герпес (ВПГ 2) — проявляется характерной сыпью, сопровождающейся зудом, болью и дискомфортом. Могут быть симптомы интоксикации в виде повышения температуры тела и общего недомогания.
3 тип (Zoster) — причина опоясывающего лишая и ветряной оспы. Опоясывающий лишай и ветряная оспа у кормящей женщины протекает, как правило, остро: повышается температура тела до 38-39С, появляются обильные высыпания на различных участках кожи. Если кормящая мама в детстве переболела «ветрянкой», то вероятность заражения ее и ребенка минимальны.
4 тип (вирус Эпштейн-Барра, ВЭБ) — вирус поражает лимфоциты и распространяется по органам, вызывая развитие мононуклеоза.
5 тип — цитомегаловирус, который в сложных случаях провоцирует поражение внутренних органов и расстройство вегетативной нервной системы.
6, 7, 8 тип — малоизучены, так как обнаружены менее полувека назад.
Из всех видов особо опасными являются вирусы 3 и 5 видов.
Особенностью вируса герпеса является длительный инкубационный (бессимптомный) период, при котором активно происходит размножение и выделение вируса от больного человека. В этот период, а особенно в период клинических проявлений заболевание передается от матери к ребенку.
В период кормления грудью у женщин проявляются разные штаммы герпеса, но чаще всего активизируются простые типы (1 и 2 типы), поэтому дальнейшая тактика лечения и организации грудного вскармливания будет зависеть от локализации герпетических высыпаний.
Если у кормящей женщины высыпания появились в области рта или на губах, то для уменьшения рисков передачи инфекции ребенку, необходимо соблюдать следующие профилактические рекомендации:
Особую настороженность кормящей женщине необходимо проявлять в случае локализации герпетических высыпаний на коже молочной железы. Если везикулы располагаются на сосках и/или ореоле, то кормление из пораженной груди временно прекращается до полного исчезновения высыпаний. Ребенку в данном случае назначается адаптированная молочная смесь, а для сохранения лактации и профилактики лактостаза, женщине рекомендуются регулярные сцеживания и утилизация грудного молока. Если поражение наблюдается только на одной молочной железе, то из второй – кормления продолжаются.
Лечение вируса герпеса простого типа проводится в виде обработки мест поражения противовирусными средствами, приемом противовирусных препаратов (по показаниям врача) и витаминно — минеральных комплексов. Лечение проводится до образования плотных корочек и исчезновения свежих высыпаний.
При всех остальных типах герпесвирусных инфекций вопрос о продолжении грудного вскармливания зависит от степени тяжести проявлений болезни у матери, состояния здоровья ребенка и решается совместно с вашим лечащим врачом. Любое самолечение и самостоятельное решение о приеме любых лекарственных препаратов может иметь негативные последствия, как для мамы, так и для ребенка. Любой лекарственный препарат должен назначаться только врачом и только строго в соответствии с показаниями.
Профилактика герпесвирусных инфекций
Герпевирусные инфекции во время периода грудного вскармливания при строгом соблюдении правил личной гигиены не являются противопоказанием к продолжению кормления грудью (за исключением тяжелых форм). При любых формах проявления заболевания, тактику лечения определяет только врач.
Список литературы:
Статью подготовила: врач-педиатр, Ульяна Владимировна Мельникова
Ацикловир при беременности и грудном вскармливании
Можно ли ацикловир при беременности для лечения герпеса и возможные риски для плода
Ацикловир относится к классу антивирусных препаратов, называемых синтетическими аналогами нуклеозидов. Он работает, останавливая распространение вируса герпеса в организме. Используется для уменьшения боли и ускорения заживления язв или волдырей у людей с ветряной оспой (ветрянка), опоясывающим лишаем, сыпью, которая может возникать у людей, перенесших ветряную оспу в прошлом, а также при вспышках генитального герпеса (время от времени вызывает образование язв вокруг гениталий и прямой кишки).
В результате исследования Центром по контролю и профилактики заболеваний (CDC), было установлено, что ацикловир проникает через плаценту, однако тератогенность (развитие врожденных пороков) не наблюдалась, но все же данных недостаточно для оценки риска менее распространенных дефектов или для получения надежных или окончательных выводов относительно безопасности этого препарата во время беременности.
По исследованиям Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) было отмечено, что женщины, принимающие ацикловир для лечения простого герпеса даже в период первого триместра беременности, не продемонстрировало риск для плода.
Австралийская администрация лекарственных средств (AU TGA) исследовала ограниченное количество беременных женщин и женщин детородного возраста, которые принимали пероральный ацикловир и установили, что это не привело к увеличению частоты пороков развития или других прямых или косвенных вредных воздействий на материнский плод. Исследования на животных показали увеличение частоты повреждений плода, значение которых для человека считается неопределенным.
Американский колледж акушеров и гинекологов (ACOG) рекомендует принимать ацикловир для лечения генитального герпеса, особенно рецидивирующего, с 36-ой недели беременности для избежания заражения новорожденного младенца. Но поскольку в результате не множественных исследований о нем мало предоставлено информации, то и применять его советуют с особой осторожностью, строго по назначению врача в точно указанной минимальной дозировке в кратчайшие сроки.
Также ACOG была предоставлена информация о том, что супрессивная терапия на поздних сроках беременности снижает частоту кесарева сечения у женщин с рецидивирующим генитальным герпесом за счет уменьшения частоты рецидивов во время беременности, но такое лечение не во всех случаях может защитить от передачи вирусной инфекции новорожденным.
Центр по контролю и профилактике заболеваний (CDC) в 2015 году пришли к выводу, что этот препарат можно использовать для лечения герпетических поражений у женщин на всех этапах беременности, но под четким контролем врача, соблюдая все его предписания по прописанным дозам, частоте и длительности приема, а также в случае самой острой необходимости и, как правило, польза для матери должна превышать риск для плода.
Применение ацикловира при кормлении грудью и воздействие на младенцев
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в результате исследований применения ацикловира у женщин в период грудного вскармливания установили, что он проникает в грудное молоко, но даже при самых высоких дозах для матери концентрация ацикловира в молоке составляет лишь около 1% от типичной детской дозы, и не ожидается, что она вызовет какие-либо побочные эффекты у младенцев, находящихся на грудном вскармливании. Местное нанесение ацикловира на небольшие участки тела матери вдали от груди не представляют опасности для младенца.
В результате заражения вирусом герпеса младенца от матери во время беременности новорожденным вводят ацикловир в дозах от 20 до 30 мг/кг внутривенно ежедневно по данным CDC. Дозировки, полученные с грудным молоком при высоких дозах для матери, составляют всего около 3-5% от этой дозы. Поскольку младенец получает дозы грудного молока перорально, а ацикловир перорально биодоступен только около 20%, системная доза, которую получает грудной младенец, составляет 1% или меньше от типичной детской дозы, в результате чего не были зафиксированы проявления побочных реакций у младенцев.
Также CDC и FDA были зарегистрированы несколько случаев по поводу приема перорального ацикловира у матерей кормящих грудью:
мать 4-месячного младенца не заметила никаких побочных эффектов у своего младенца, находящегося на грудном вскармливании, когда она принимала ацикловир в дозе 800 мг перорально 5 раз в день;
женщина, которой было 6 недель после родов, получала ацикловир 300 мг (5 мг/кг) внутривенно три раза в день в течение 5 дней. Образцы молока брали каждые 6 часов после последней дозы. Пиковый уровень составлял 7,3 мг/л, и препарат обнаруживался в молоке в течение 88 часов после последней дозы. Через 6 часов после приема последней дозы, вскармливаемый грудью ребенок получал через материнское молоко суточную дозу 1,1 мг/кг ацикловира, в случае такой терапии у матери в период лактации, также не отмечались негативные последствия у младенца.
В результате таких исследований Центр по контролю и профилактике заболеваний (CDC) и Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), пришли к выводу, что прием ацикловира для женщин в период лактации, считается приемлемым, но не должен приниматься бесконтрольно, дозу и длительность лечения ацикловиром должен устанавливать врач, с обязательным сопоставлением пользы для матери и возможных рисков для новорожденного.
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
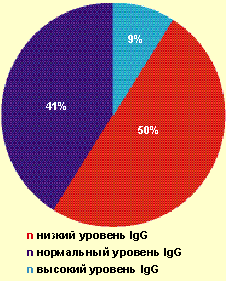 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
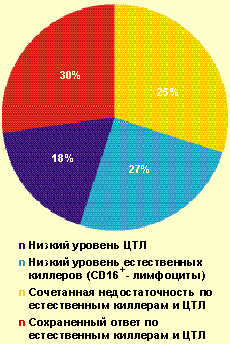 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва





