Новое в рекомендациях по лечению хламидийной инфекции во время беременности
Хламидийная инфекция может существенно осложнить беременность. С ней может быть связан риск таких неблагоприятных исходов беременности, как послеродовой эндометрит, преждевременные роды, рождение детей с низкой массой тела (W. A. Andrews et al., 2000).
Хламидийная инфекция может существенно осложнить беременность. С ней может быть связан риск таких неблагоприятных исходов беременности, как послеродовой эндометрит, преждевременные роды, рождение детей с низкой массой тела (W. A. Andrews et al., 2000).
По данным Центра по контролю заболеваемости США (U.S. Centers for Disease Control and Prevention, CDC), распространенность хламидийной инфекции у беременных женщин составляет от 2 до 24%. У 25–50% детей, рожденных инфицированными женщинами, развивается хламидийная инфекция глаз, у 10–20% — хламидийная пневмония (J. Schachter, 1995). Риск передачи инфекции новорожденному составляет около 70%.
Необходимость терапии урогенитального хламидиоза у беременных, если ее по разным причинам не удалось провести до беременности, не вызывает сомнений у специалистов. Единственное условие, которое следует неукоснительно соблюдать при выборе адекватной терапии беременных, это четкое следование признанным, т. е. соответствующим принципам доказательной медицины, рекомендациям. На самом деле любые назначения в современной практике должны соответствовать таким принципам, но когда речь идет о лечении беременных, эти требования должны соблюдаться неукоснительно — во избежание тяжелых последствий.
При освещении вопросов терапии хламидийной инфекции у беременных мы ориентировались на современные подходы к решению этой проблемы, изложенные в последних редакциях трех руководств — российском («Рациональная фармакотерапия заболеваний кожи и инфекций, передаваемых половым путем», под редакцией А. А. Кубановой, 2005 г.), европейском («Европейское руководство по ИППП», 2001 г.) и американском («Руководство по лечению ИППП» CDC, 2006 г.).
Хорошо известно, что основными антибиотиками, рекомендованными всеми мировыми руководствами для лечения хламидийной инфекции, являются тетрациклины и макролиды. Из фторхинолонов — только офлоксацин. Также известно, что препараты тетрациклинового ряда и фторхинолоны противопоказаны при беременности из-за патологического влияния на формирование зубов и костной ткани у плода. Таким образом, из рекомендованных для лечения беременных антибиотиков, обладающих противохламидийной активностью, остаются только макролиды.
Первым из макролидов появился эритромицин. Огромное число наблюдений, накопившееся почти за 60 лет существования эритромицина, показало его безопасность для плода. Этот антибиотик — один из немногих, разрешенных к применению у беременных и новорожденных. В связи с этим для лечения хламидийной инфекции у беременных женщин в качестве препарата первого выбора во всех рекомендациях долгое время фигурировал эритромицин.
При приеме любых макролидов могут наблюдаться побочные эффекты со стороны желудочно-кишечного тракта (тошнота, рвота, диарея) и печени (повышение активности трансаминаз, холестаз, желтуха), а также аллергические реакции.
Вопрос переносимости становится одним из основных при выборе препарата для лечения хламидийной инфекции у беременных.
Побочные эффекты, в основном со стороны желудочно-кишечного тракта, при приеме эритромицина развиваются у 15–100% больных, 12–33% больных из-за этого прекращают курс терапии (J. Kacmar, 2001). У беременных побочные эффекты после приема эритромицина наблюдаются особенно часто. Это заставляет искать новые методы терапии беременных препаратами, не уступающими по безопасности эритромицину. Проблема с назначением новых, даже относительно новых антибиотиков беременным объясняется тем, что специально клинические испытания на беременных никто по этическим соображениям не проводит. Даже если в экспериментах на животных препараты не обладали тератогенным или мутагенным действием, уходят многие годы на накопление данных о безопасности применения препаратов у беременных и кормящих женщин. Прогресс в этой области идет очень медленно, что тем не менее оправдано ввиду сложности проблемы и огромной ответственности, связанной с внесением коррекций в существующие рекомендации.
В последние 15 лет наиболее активным противохламидийным препаратом и основным средством для лечения различных форм урогенитальной хламидийной инфекции признан азитромицин. Именно этот антибиотик все упомянутые руководства относят к препаратам выбора при лечении хламидиоза. Этому способствуют уникальные фармакокинетические характеристики азитромицина: продолжительный период полувыведения, высокий уровень всасывания и устойчивость в кислой среде, способность этого антибиотика транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, а также возможность проникновения внутрь клетки. Благодаря тому, что высокая терапевтическая концентрация азитромицина в тканях достигается после однократного приема стандартной дозы антибиотика и сохраняется в местах воспаления не менее 7 сут, с появлением азитромицина впервые возникла возможность эффективного лечения больных хламидийной инфекцией путем однократного приема антибиотика внутрь. Излечение хламидийной инфекции после однократного приема азитромицина подтверждается самой высокой комплаентностью в сравнении со всеми другими антибиотиками, которые следует назначать не менее чем на 7 дней. Показано, что нарушение многодневных режимов лечения отмечают до 25% больных, а при развитии побочных эффектов этот показатель значительно возрастает. Таким образом, явным преимуществом азитромицина является возможность его назначения однократно, что особенно актуально у беременных.
Оригинальным и наиболее известным из препаратов азитромицина является сумамед, который используется в Российской Федерации с начала 90-х годов прошлого века. Именно в отношении этого препарата накоплен самый большой опыт по лечению самых разнообразных форм хламидийной инфекции.
Несмотря на общие требования, касающиеся использования в публикациях только международных названий препаратов, при описании эффективности применения лекарства, его переносимости представляется важным указывать, какой именно коммерческий препарат использовался в исследовании, потому что качество одних и тех же лекарств, выпускаемых различными производителями, может быть различным. Чтобы показать эффективность и переносимость именно своего продукта, многие фармацевтические компании, выпускающие дженерики, проводят сравнительные испытания своей продукции с оригинальным препаратом, каковым, как уже было отмечено выше, и является сумамед. С использованием сумамеда проведена основная масса фармакологических и клинических исследований азитромицина во всем мире, поскольку именно из субстанции, поставлявшейся той же компанией, которая производила сумамед, распространенный в странах Восточной Европы, в течение многих лет в США производили зитромакс, поставлявшийся в страны Западной Европы, Америки и Японию.
Согласно российскому руководству при хламидийной инфекции у беременных препаратами выбора служат:
Таким образом, из относительно новых макролидов в отечественных рекомендациях среди препаратов выбора присутствует азитромицин и джозамицин. Хотя в России нет пока национальных стандартов по лечению ИППП, наша страна стала одним из первых в мире государств, где азитромицин появился в официальных рекомендациях в качестве основного препарата для лечения хламидийной инфекции во время беременности.
В европейском руководстве среди основных препаратов фигурируют:
А в качестве альтернативных приводятся следующие схемы:
По мнению европейских коллег, несмотря на эффективность и безопасность азитромицина, наблюдения относительно безопасности его применения пока недостаточно длительны, чтобы рекомендовать его рутинное применение во время беременности. Правда, следует напомнить, что речь идет о Рекомендациях 2001 г., которые с тех пор не корректировались.
До недавнего времени и в американском руководстве азитромицин отсутствовал среди основных препаратов, рекомендуемых для лечения хламидийной инфекции у беременных. Еще в 2002 г. для лечения беременных, согласно Руководству по лечению ИППП — CDC, рекомендовали применять только эритромицин или амоксициллин. Но после российских специалистов и американцы пошли на изменение своих рекомендаций: новая редакция Руководства от 2006 г. уже рекомендует однократный прием азитромицина в качестве основной схемы лечения хламидийной инфекции у беременных. Эритромицин впервые был переведен в разряд альтернативных препаратов. Амоксициллин остался как препарат выбора наряду с азитромицином.
Можно ожидать, что скоро и Европа присоединится к российским и американским коллегам.
Хотелось бы прокомментировать некоторые процитированные выше рекомендации.
Итак, почему же азитромицин выходит на первое место при терапии хламидийной инфекции у беременных?
Все рекомендации, касающиеся лечения беременных, очень консервативны и не меняются десятилетиями, пока не накапливаются данные о безопасности нового лекарственного средства. Доклинические испытания на животных не показали какого-либо тератогенного эффекта азитромицина. Только этого недостаточно для разрешения его применения у беременных. Появление азитромицина как средства лечения хламидийной инфекции у беременных в некоторых признанных рекомендациях свидетельствует о том, что к настоящему времени по всему миру уже накопилось достаточное количество сведений о результатах применения азитромицина, как в ходе запланированных исследований, так и в результате случайного приема беременными, не знавшими, что они находятся в этом состоянии. Ни одного достоверного сообщения о негативном действии на плод азитромицина пока не получено. Все эти данные накапливались постепенно в разных странах, причем самый длительный опыт у исследователей из Хорватии, где и был впервые получен азитромицин.
По данным V. Simunic и соавторов, эффективность 1 г азитромицина при лечении хламидийной инфекции у беременных составила 92,1%, а семидневного курса эритромицина — 87,5%. При этом комплаентность и переносимость терапии азитромицином были гораздо лучше, а исходы беременности в группах достоверно не отличались. У женщин с отягощенным акушерско-гинекологическом анамнезом и наличием хламидийной инфекции после применения азитромицина в 10,5% случаях произошли преждевременные роды, в 7,9% — ранние выкидыши, в 2,6% — поздние выкидыши. В группе таких же беременных, получавших эритромицин, преждевременные роды, ранние выкидыши и поздние выкидыши наблюдали в 12,5, 8,4 и 4,1% случаев соответственно.
В другом исследовании (C. D. Adair et al., 1998) также был показан сравнимый терапевтический эффект азитромицина и эритромицина — 88,1 и 93,0%. Но переносимость курса лечения с применением азитромицина оказалась гораздо выше, чем при использовании эритромицина — желудочно-кишечные расстройства наблюдались у 11,9% пациенток, принимавших азитромицин (из них у 1 больной (2,4%) лечение пришлось отменить из-за развития рвоты через 4 ч после приема препарата), и у 58,1% больных, принимавших эритромицин (лечение были вынуждены прекратить 18,6% больных). Меньшая частота развития побочных эффектов при приеме азитромицина отчасти связана с однократным приемом этого препарата. Никаких патологических влияний проведенной терапии на новорожденных зафиксировано не было.
В исследовании M. R. Bush и соавторов (1994) побочные эффекты при приеме эритромицина отмечали у всех больных (15 пациентов), при назначении азитромицина — ни у одного из 15. Пятеро из 15 больных, принимавших эритромицин, не смогли полностью закончить лечение.
По данным Кохрановского обзора, показатель микробиологической излеченности у беременных женщин в результате применения всех указанных в руководствах антибиотиков колеблется в пределах 90%. В этом же обзоре, несмотря на небольшое количество данных, делается вывод, что беременные женщины лучше переносят азитромицин и поэтому лечение азитромицином может быть более эффективным. Проведенные исследования не позволили сделать вывод о том, что микробиологическая излеченность во время беременности гарантирует от последующего заболевания новорожденных или послеродовых проявлений хламидийной инфекции у женщин.
Амоксициллин относится к группе пенициллинов, в принципе не рекомендованных к применению при хламидиозе, но, по данным Кохрановского обзора, имеются сообщения о его успешном использовании при наличии хламидийной инфекции у беременных, хотя этот факт вызывает удивление. Он реже, чем эритромицин или азитромицин, вызывает побочные эффекты, которые заставляют прекращать лечение. Так, в исследовании J. Kacmar и соавторов (2001) сообщается о развитии побочных эффектов у 40% больных, принимавших азитромицин, и 17% — принимавших амоксициллин. Однако около 16% больных, принимавших амоксициллин, нарушали режим лечения, пропускав прием лекарства. Эффективность лечения составила 80% при приеме амоксициллина и 94,7% при приеме азитромицина (различия не являются статистически достоверными). Отсутствие долгосрочных исследований влияния применения амоксициллина на риск развития неонатальных инфекций не позволяет с уверенностью рекомендовать этот препарат для рутинной клинической практики. Длительное наблюдение за группой новорожденных и их матерей, во время беременности лечившихся амоксициллином от хламидийной инфекции, позволило бы клиницистам более широко применять эту схему лечения. Амоксициллин, без сомнения, может использоваться как альтернативный препарат для терапии беременных при непереносимости макролидов.
Всем пациенткам, получившим лечение эритромицином, который пока еще чаще используют у беременных, рекомендуется проводить повторное лабораторное исследование через 3 нед после окончания терапии, поскольку побочные эффекты могут вынуждать пациентку нарушать схему его применения.
В заключение мы еще раз хотели вернуться к проблеме изменения традиционных рекомендаций по лечению хламидийной инфекции у беременных. Это очень ответственное решение, требующее многолетних наблюдений. За последние годы единственным серьезным изменением в этой области явилось появление азитромицина среди препаратов выбора в российских и основных мировых рекомендациях. Конечно, этому способствовали многие особенности этого антибиотика, такие как продолжительный период полувыведения, высокий уровень всасывания и устойчивость в кислой среде, способность транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, возможность проникновения внутрь клетки, хорошая переносимость. Но основным препаратом для лечения урогенитальной хламидийной инфекции у беременных женщин азитромицин стал прежде всего благодаря низкой токсичности и безопасности для плода.
А. М. Соловьев, кандидат медицинских наук, доцент
М. А. Гомберг, доктор медицинских наук
МГМСУ, Москва
Актуальные проблемы лечения беременных с рецидивирующей хламидийной инфекцией
Специфические инфекционные заболевания полового тракта у беременных значительно увеличивают частоту материнских и перинатальных осложнений. Такая инфекция, как хламидиоз, ассоциированная с микоплазмами, цитомегаловирусная, герпесвирусная инфекции, а такж
Специфические инфекционные заболевания полового тракта у беременных значительно увеличивают частоту материнских и перинатальных осложнений. Такая инфекция, как хламидиоз, ассоциированная с микоплазмами, цитомегаловирусная, герпесвирусная инфекции, а также их сочетание с бактериальными поражениями являются одной из ведущих причин перинатальной смертности (Королева А. И., 2000; Стрижаков А. Н. и соавт., 2003). В последние годы возросло число хламидийной, вирусной, микоплазменной и смешанной инфекций, борьба с которыми представляет значительные сложности в связи с развивающейся устойчивостью микроорганизмов к антибиотикам и особенностями ответных реакций организма (Глазкова Л. К., 1999; Рюмин Д. В., 1999; Семенов В. М., 2000; Хрянин А. А., 2001; Johnson R. A., 2000).
По-прежнему высокой остается частота урогенитального хламидиоза у беременных, колеблющаяся от 3% до 74% по данным различных авторов (Асцатурова О. Р., 2001; Прилепская В. Н. и соавт., 1998; Семенов В. М., 2000; Hiltunen-Back E., 2001; Stamm W. E., 1999).
В настоящее время доказано, что Chlamydia trachomatis является облигатным паразитом человека. Заражение происходит при половом контакте, редко — бытовым путем (Плиева З. А., 2000; Morion R. S., Kinghom G. R., 1999).
Хламидийная инфекция ведет к прерыванию беременности, невынашиванию, развитию фетоплацентарной недостаточности, внутриутробному инфицированию (ВУИ) плода, послеродовым воспалительным заболеваниям, неонатальным инфекциям.
В I триместре беременности наиболее характерным осложнением является угрожающий выкидыш, неразвивающаяся беременность и спонтанный аборт. Во II и III триместрах угроза прерывания беременности имеет длительное течение, а токолитическая терапия дает, как правило, нестойкий эффект. Это связано с инфицированием амниона хламидиями, которое встречается у 65% беременных. Тельца Chlamydia trachomatis выявлены во всех тканевых структурах плаценты женщин с генитальным хламидиозом. Отмечено, что пораженные хламидиями клетки обнаружены в просвете капилляров ворсин хориона, что указывает на возможный гематогенный путь передачи инфекции от матери к плоду. В плацентах женщин с генитальным хламидиозом происходит нарушение иммунного гомеостаза с образованием патогенных иммунных комплексов (ПИК), включающих IgM, IgG, IgA и фиксирующих С3-фракцию комплемента как маркер патогенности. Показано, что фиксация ПИК на мембранных структурах плаценты приводит к разрушению мембран синцития и плацентарного барьера. Последнее вызывает развитие плацентарной недостаточности и повреждение фето-плацентарной системы.
В случаях инфицирования амниотических оболочек может развиться многоводие, специфическое поражение плаценты (плацентит), плацентарная недостаточность, гипотрофия и гипоксия плода. Истинные пороки развития плода не являются патогномоничными для хламидийной инфекции.
В процессе эхографического обследования беременных с внутриутробным инфицированием достоверно чаще встречаются следующие эхографические признаки: многоводие, маловодие, гиперэхогенная взвесь в околоплодных водах, изменения плаценты. При проведении ультразвуковой плацентографии у женщин с инфекционной патологией гениталий обнаруживаются следующие изменения: утолщение плаценты, разнородная эхогенность паренхимы плаценты, преждевременное «старение» плаценты, расширение межворсинчатых пространств, расширение субхориального пространства, утолщение/удвоение контура базальной пластинки. В 75% имеется сочетание двух или нескольких вариантов изменения эхографической структуры плаценты.
Следует отметить, что при наличии более двух эхографических маркеров у новорожденного в 82% наблюдений постнатально диагностируется внутриутробная инфекция.
Для беременных с хламидийной инфекцией и фетоплацентарной недостаточностью первичными ее проявлениями являются нарушения внутриплацентарного кровотока.
Механизмы ВУИ при хламидийной инфекции включают следующие пути распространения инфекции:
При отсутствии гипоксии плода и аспирации инфицированного содержимого родового канала риск развития тяжелой инфекции у новорожденного ниже, чем при длительном контакте плода с инфицированной средой во время беременности. Так, почти половина новорожденных от матерей с хламидиозом имеют клинически выраженную инфекцию.
К неонатальным проявлениям хламидийной инфекции относятся поражения кожи и слизистых (конъюнктивит), пневмония, отит, вульвит, уретрит. У недоношенных детей возможно развитие специфического миокардита после хламидийной пневмонии, описаны случаи хламидийного менингита и энцефалита.
В зависимости от пути заражения и инфицирующей дозы, проявления перинатальной хламидийной инфекции могут встречаться не только в первые 168 ч жизни новорожденного (ранний неонатальный период), но и реализовываться в течение первых месяцев жизни ребенка.
Основным методом борьбы с подобными осложнениями является своевременное проведение рациональной этиотропной антибиотикотерапии.
Пациенткам с бактериальными ИППП чаще всего назначают системную терапию антибактериальными препаратами с учетом предполагаемой или определяемой чувствительности возбудителя.
Общими положениями являются преимущественное использование макролидов как препаратов выбора для лечения хламидийной, микоплазменной и уреаплазменной инфекций у беременных, начало лечения после 20 нед гестации или в III триместре беременности.
Для лечения урогенитального хламидиоза в гинекологической практике используют тетрациклины, фторхинолоны и макролиды. Применение тетрациклинов и фторхинолонов во время беременности и лактации противопоказано из-за наличия неблагоприятных эффектов для эмбриона, плода и новорожденного.
Для лечения беременных с генитальными инфекциями применяются такие антибиотики группы макролидов, как эритромицин, спиромицин и джозамицин, использование которых с учетом срока гестации безопасно для матери и плода.
Одним из наиболее изученных с точки зрения безопасности у беременных является макролидный антибиотик джозамицин (Вильпрафен). Важное клиническое значение имеет его высокая активность против таких внутриклеточных патогенов, как C. trachomatis, M. hominis, M. genitalium, U. Ureallyticum. Джозамицин быстро и полностью всасывается из желудочно-кишечного тракта (ЖКТ), создавая максимальную концентрацию в плазме крови уже через 1 ч. Важным аспектом, определяющим успех лечения, является достижение высоких концентраций препарата в тканях по сравнению с плазмой крови. Способность джозамицина накапливаться преимущественно в фагоцитирующих клетках особенно важна для элиминации внутриклеточных возбудителей. Доказано, что фагоциты доставляют джозамицин в места локализации инфекционного агента, где действующее вещество освобождается в процессе фагоцитоза, причем концентрация джозамицина в очаге инфекции на 30% выше, чем в здоровых тканях. В отличие от ряда препаратов данного класса джозамицин не стимулирует двигательную функцию кишечника и не ингибирует такие важнейшие компоненты метаболической системы печени, как цитохром Р 450 и НАДФ-цитохром С-редуктазу. Таким образом, джозамицин отличают оптимальный спектр активности в отношении урогенитальных патогенов, благоприятная фармакокинетика и высокая безопасность, в том числе у беременных.
Следует отметить, что в настоящее время бактериостатический антибиотик эритромицин практически не используется для лечения урогенитального хламидиоза, так как его микробиологическая эффективность зачастую не превышает 30% (Асцатурова О. Р. и соавт., 2001; Страчунский Л. С., 1998; Ridgway G. L., 1995).
С целью выявления частоты генитальных инфекций, факторов риска их развития, приводящих к осложнениям беременности, родов и их исходов для новорожденного, было проведено обследование 5430 беременных на базе родильного дома и консультативно-диагностического центра при ГКБ № 7 с 1997 по 2005 г.
Контрольную группу составили 200 женщин с отсутствием генитальных инфекций в анамнезе и во время беременности, у детей которых не были диагностированы инфекционно-воспалительные заболевания в раннем неонатальном периоде.
Частота встречаемости заболеваний, передаваемых половым путем, составила 17,85% (969). Структура ИППП у беременных была представлена хламидийной (24,56%), микоплазменной (8,36%), уреаплазменной (3,1%), трихомонадной (4,85%), смешанной (59,13%) инфекциями.
Острые и обострения хронических вирусных заболеваний наблюдались в 10,24% (556 случаев) и были представлены герпетическими поражениями в 8,34%, цитомегаловирусной инфекцией — в 0,78% и папилломавирусной инфекцией — в 1,12%.
Высокая частота смешанных инфекций при хламидиозе, наличие малосимптомного и латентного его течения приводит к необходимости комплексной диагностики ИППП и нарушений микроценоза влагалища.
Ни один из современных методов диагностики хламидиоза не обеспечивает 100% надежности. Поэтому лабораторная диагностика должна основываться на сочетании минимум двух методов, одним из которых должен являться метод полимеразной цепной реакции (ПЦР).
Непосредственная идентификация элементарных телец (ЭТ) и ретикулярных телец (РТ) хламидий возможна при микроскопии мазков, окрашенных по Романовскому–Гимзе. Цитоплазматические включения определяются в виде микроколоний, окрашенных в темно-синий или розовый цвет (тельца Гальберштадтера–Провачека). Чувствительность цитологического метода обнаружения хламидий не превышает 10–12%. Метод позволяет оценить состояние микроценоза влагалища, количество лейкоцитов, выявить наличие дрожжеподобных грибов, влагалищных трихомонад.
Наиболее распространенный метод диагностики хламидийной инфекции — иммуноцитологический — основан на реакции прямой или непрямой иммунофлюоресценции (определение антигена С. trachomatis).
При его использовании к биологическому материалу добавляются меченые флюоресцинами моноклональные антитела. Полученные мазки оценивают под люминесцентным микроскопом. Чувствительность метода колеблется в пределах 65–90%, а специфичность — 85–90%. Главными недостатками метода являются его субъективность и низкая чувствительность.
Иммуноферментный анализ основан на идентификации антигенов хламидий путем связывания их антителами. Количественная оценка комплексов антиген-антитело проводится с помощью автоматизированного определения выраженности цветной реакции. Преимуществом метода является возможность определять растворимые антигены, время проведения (4–6 ч), недостатком — возможность получения ложноотрицательных и ложноположительных реакций.
ПЦР обладает преимуществами по сравнению с иммунологическими методами: высокая специфичность — 95%; максимальная чувствительность; быстрота проведения (4–5 ч). Недостатком ПЦР-диагностики хламидиоза является то, что метод амплификации ДНК не позволяет оценить жизнеспособность клетки, дает положительные результаты при малых количествах возбудителя и наличии отдельных фрагментов его генома. Несмотря на это первичным способом оценки элиминации хламидий должна являться ПЦР. При получении положительного результата показано проведение микробиологического исследования, а при невозможности последнего — повторная ПЦР через 5–6 нед.
Наиболее достоверным методом диагностики хламидиоза является сочетание культурального исследования и ПЦР.
К методам непрямой диагностики хламидийной инфекции относится определение уровня специфических антител. Накопление антител классов М, G и А происходит через разные промежутки времени и зависит от характера инфицирования (первичная инфекция, реинфекция). При первичном инфицировании вначале появляются IgM, затем — G, потом — А. При вторичном инфицировании отмечается быстрое нарастание антител классов G и А на фоне отсутствия IgM. Этот метод исследования позволяет определить стадию заболевания, оценить эффективность проводимого лечения, доказать хламидийную этиологию экстрагенитальных поражений.
Определение ДНК Chlamidia trachomatis проводили путем ПЦР. Материалами для исследований служили соскоб из цервикального канала, со слизистых, слюна, моча и кровь новорожденных. Все соскобы забирали с использованием одноразовых стерильных цитологических щеточек фирмы PathFinder (США). Использовали многоканальный амплификатор ДНК «Терцик™» и наборы реактивов к нему (АО «Петровакс», Институт иммунологии, Москва).
У 238 беременных острая хламидийная инфекция (длительность заболевания менее 2 мес) имелась у 79 (33,19%), хроническая (более 2 мес) — у 159 (66,8%). У большинства пациенток с хронической инфекцией (62%) имелись анамнестические данные, свидетельствующие о длительности заболевания более полугода и неадекватной предшествующей терапии.
Под нашим наблюдением в ходе проспективной части исследования находились 72 беременные со сроком гестации 29–41 нед, у 33 (45,83%) из которых предшествующая этиологическая терапия острой или хронической хламидийной инфекции была неэффективна, а также 28 (38,89%) женщин с хронической рецидивирующей инфекцией и 11 (15,28%) беременных, преждевременно прекративших ранее начатую терапию. До включения в исследование больные получали различную антибиотикотерапию: в первой подгруппе 16 (57,14%) беременных по поводу хламидийной инфекции принимали эритромицин по 1–3 г/сут, 9 — азитромицин по 0,25 г/сут, 8 — спирамицин по 9 млн ЕД/сут. Необходимо отметить неадекватность суточной дозы эритромицина и азитромицина для лечения хламидиоза.
Интересным представляется факт, что 9 из 11 беременных, прекративших начатое лечение самостоятельно (81%), получали эритромицин и спирамицин. При целенаправленном расспросе в ходе настоящего исследования удалось выяснить, что они мотивировали отказ от терапии «опасностью для ребенка» при приеме «таких высоких доз» антибиотика.
Всем пациенткам после разъяснения особенностей течения хламидийной инфекции, ее опасности для беременной и плода, необходимости проведения антибактериальной терапии и лечения, направленного на купирование осложнений беременности, действия препарата джозамицина (Вильпрафен) и схемы его применения была назначена терапия, включавшая прием 1 таблетки (500 мг) Вильпрафена 3 раза/сут на протяжении 10 дней. Всем половым партнерам больных проводилось обследование и лечение генитальных инфекций. После терапии Вильпрафеном беременные в течение 3-х дней фиксировали возможные побочные эффекты препарата (тошнота, рвота, боль в животе, изменение характера стула, метеоризм, сыпь, кожный зуд).
Контроль за эффективностью терапии осуществляли на основании результатов ПЦР через 4 нед после приема Вильпрафена. Лечение считали эффективным при отсутствии обнаружения генома Chlamydia trachomatis. При положительных результатах первой ПЦР выполняли культуральное исследование (или ПЦР через 5–6 нед).
Микробиологическая эффективность применения джозамицина у беременных с хламидийной инфекцией по результатам первого контрольного обследования составила 93,06%. В трех наблюдениях при положительных результатах первой ПЦР не обнаружено роста C. trachomatis на культуре клеток McCoy. В течение 3 мес наблюдения микробиологически верифицированная персистенция хламидий после лечения сохранялась у 2 женщин (2,78%).
По сравнению с данными, полученными в контрольной группе, при хламидиозе имеются значимые отличия в частоте акушерско-гинекологической патологии во время беременности (рис. 1).
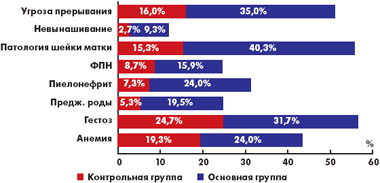 |
| Рис. 1. Осложнения беременности у женщин контрольной группы и с хламидийной инфекцией |
Осложнениями гестационного процесса, связанными с хламидийной инфекцией, считали угрозу прерывания беременности, преждевременные роды, фетоплацентарную недостаточность и задержку роста плода, эхографические маркеры внутриутробного инфицирования (изменение эхогенности плаценты, много- и маловодие, структурные дефекты развития плода). Кроме того, отмечена высокая частота сочетания хламидиоза с патологией шейки матки и инфекцией мочевыводящих путей.
После проведения лечения Вильпрафеном по указанной схеме (1500 мг/сут в течение 10 дней) зарегистрировано существенное снижение частоты осложнений беременности, родов, общей и инфекционной заболеваемости новорожденных (рис. 2).
 |
| Рис. 2. Частота осложнений беременности, родов и неонатальной заболеваемости после лечения хламидиоза Вильпрафеном |
Применение Вильпрафена для лечения урогенитального хламидиоза во время беременности, в том числе после неэффективной терапии другими антибиотиками, приводит к микробиологической излеченности у 97,22% пациенток. Важно отметить, что такие высокие показатели эффективности лечения достигнуты в группе женщин с рецидивирующей и хронической хламидийной инфекцией. Кроме того, применение джозамицина возможно вне зависимости от срока беременности.
Не было зарегистрировано отказов от рекомендованного лечения. Нежелательные явления на фоне приема Вильпрафена в виде тошноты отметили 2 беременные и в виде «тяжести» в животе — 1 женщина (всего 4,17%).
Особенностью хронической хламидийной инфекции является скудная симптоматика или полное отсутствие клинических проявлений заболевания, что приводит к поздней диагностике. В то же время нерациональная антибиотикотерапия не только обусловливает возникновение резистентности возбудителя, но и приводит к позднему началу адекватного лечения. Высокая частота ассоциированных с инфекцией осложнений требует проведения высокоинформативных методов диагностики хламидиоза и назначение этиотропной терапии в комплексном лечении беременных.
Частота перинатальных инфекций после использования Вильпрафена во время беременности снизилась в 2,4 раза. Не было отмечено случаев хламидийной пневмонии и генерализованной инфекции у новорожденных, матери которых получали терапию джозамицином.
Таким образом, у беременных с ИППП эхографические маркеры инфекции обнаруживаются почти в 30%. Частота фетоплацентарной недостаточности у этих женщин возрастает почти в 2 раза. Гемодинамические нарушения у беременных с восходящим инфицированием плода преимущественно регистрируются в плодово-плацентарном звене кровообращения.
Так как хроническая и рецидивирующая хламидийная инфекция приводит к изменениям фетоплацентарного комплекса, необходимо своевременно диагностировать хламидийные поражения и осуществлять комплексную терапию с учетом степени распространения процесса, срока беременности и наличия сопутствующих осложнений.
Лечение хламидийной инфекции у беременных с помощью джозамицина (Вильпрафена) уменьшает частоту материнских и перинатальных осложнений, имеет хорошую переносимость, обладает высоким удобством для соблюдения режима приема и психологического комфорта пациенток.
По вопросам литературы обращайтесь в редакцию.
П. В. Буданов, кандидат медицинских наук, доцент
ММА им. И. М. Сеченова, Москва