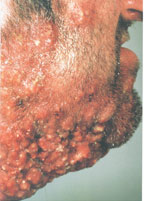
Лечение гидраденита
Хирургическое лечение гидраденита «сучье вымя» направлено на ликвидацию инфекционного очага, образующегося в потовых железах подмышечной области или в редких случаях, в паховой и околопупочной зоне.
Врачи по специализации
В хирургическом центре клиники GMS операции по поводу гидраденита проводятся амбулаторно, без необходимости госпитализации. Наши специалисты используют современные результативные техники, позволяющие быстро и безболезненно удалить патологический очаг, исключив вероятность рецидива.
Почему нужна операция
Гидраденит – воспалительно-гнойный процесс, затрагивающий апокриновые потовые железы. Возбудителем преимущественно выступает золотистый стафилококк, проникающий в железу на фоне микротравмы кожного покрова, сопутствующих кожных заболеваний и недостаточной личной гигиены. Также болезнь возникает вследствие аномальной анатомии потовой железы – суженный, извивающийся проток систематически блокируется сальными выделениями и ороговевшими частицами кожи, что приводит к рецидивирующему воспалительному процессу. Развивается инфильтрат с последующим расплавлением окружающих тканей.
Гидраденит отличается от других гнойно-воспалительных процессов кожи и подкожных структур, отсутствием некротического стержня. Золотистый стафилококк провоцирует некроз тканей потовой железы. После их разрушения заполненная гнойным содержимым и некротическими массами полость увеличивается. Инфильтрат из плотного становится мягким, а через истонченный кожный покров просвечивает гной.
Преимущества лечения гидраденита в GMS Hospital
В центре хирургии GMS лечение гидраденита проводится амбулаторно, в день обращения. Наши специалисты обладают многолетним опытом в области амбулаторной хирургии и проводят подобные вмешательства быстро, безопасно и с максимальным терапевтическим результатом. Лечение гидраденита в GMS Hospital – это:
Своевременно проведенная операция обеспечивает скорейшее заживление раны, предупреждает вероятность инфицирования глубоких тканей и развития опасных осложнений. Не стоит тянуть с визитом к врачу при появлении тревожных симптомов – запишитесь на консультацию хирурга уже сейчас, на сайте или по телефону.
Стоимость лечения гидраденита
Цены, указанные в прайс листе, могут отличаться от действительных. Пожалуйста, уточняйте актуальную стоимость по телефону +7 495 104 8605 (круглосуточно) или в клинике GMS Hospital по адресу: г. Москва, ул. Каланчёвская, 45.
Уважаемые клиенты! Каждый случай индивидуален и конечную стоимость Вашего лечения можно узнать, только после очного визита к врачу GMS Hospital.
Указаны цены на самые востребованные услуги со скидкой 30%, которая действует при оплате наличными или банковской картой. Вы можете обслуживаться по полису ДМС, оплачивать отдельно каждый визит, заключить договор на годовую медицинскую программу или внести депозит и получать услуги со скидкой. В выходные и праздничные дни клиника оставляет за собой право взимать доплату согласно действующего прейскуранта. Услуги оказываются на основании заключенного договора.
Принимаются к оплате пластиковые карты MasterCard, VISA, Maestro, МИР. Также доступна бесконтактная оплата картами Apple Pay, Google Pay и Android Pay.
с ведущими российскими и зарубежными медицинскими учреждениями
и передовые методики диагностики и лечения
Показания к операции
Показанием к хирургическому лечению, является:
Решение о возможности оперативного вмешательства в амбулаторных условиях хирург принимает исходя из особенностей клинической ситуации. В отдельных случаях, может потребоваться госпитализация.
Подготовка, диагностика
При осмотре хирург дифференцирует гидраденит от иных гнойных поражений кожи и мягких тканей, определяет стадию болезни. Для адекватной антибиотикотерапии проводится бакпосев гнойного отделяемого на микрофлору и чувствительность к антибиотикам. При затяжных и рецидивирующих патологиях назначается иммунограмма. Хирургическое вмешательство не предусматривает специфической подготовки. Все что нужно – сдать стандартный пакет анализов. Благодаря собственной лаборатории, ответы будут готовы в течение часа, после чего хирург проведет лечение.
Как проводится операция
Хирургическая тактика подбирается в зависимости от стадии болезни и особенностей ее течения. Существует три основных подхода к терапии гидраденита:
Для быстрейшего заживления назначают физиотерапевтические процедуры, а для предупреждения инфекции, проводится короткий курс массированной антибиотикотерапии.
Особенности реабилитационного периода
После вскрытия и дренирования полости инфильтрата на рану накладывается повязка с антисептиком, которую нужно ежедневно менять, до полного заживления раневой поверхности. Чтобы не допустить повторного развития болезни, нужно:
Если вы обнаружили у себя подозрительное уплотнение на коже, которое покраснело и болит, запишитесь на консультацию к хирургу. Гидраденит коварная патология, от которой застраховаться невозможно, но своевременное лечение быстро избавит от болезненных и дискомфортных проявлений и вернет здоровье. Запись на прием к специалистам центра хирургии GMS Hospital выполняется круглосуточно, онлайн или по телефону.
Смежные операции и методики
Это настоящий волшебник! Он смог моего супруга в буквальном смысле поставить на ноги. Муж перенес сложнейший инсульт и нам на выздоровление не давали вообще никаких надежд.
Хочу поблагодарить Алевтину Александровну за внимательное отношение, профессионализм и удачно проведённую операцию.
Благодарю Головенко Николая Олеговича! Спасибо!
Гидраденит
Общее лечение
Показано при хроническом течении, а также при наличии осложнений (синдром общей инфекционной интоксикации, регионарный лимфаденит и др.) – назначают антибиотики в средних терапевтических дозировках.
Антибиотики группы пенициллин
Антибиотики группы цефалоспоринов
Антибиотики группы макролидов
Антибиотики группы тетрациклина
Доксициклина гидрохлорид, моногидрат 100 мг — детям старше 12 лет с массой тела менее 50 кг в 1-й день — 4 мг/кг массы тела 1 раз в сутки, в последующие дни — 2 мг/кг массы тела 1 раз в сутки. Детям старше 12 лет с массой тела более 50 кг и взрослым — в первые сутки 200 мг однократно, затем по 100 мг 1 раз в сутки. Курс лечения — 10–14 дней.
Фторхинолоны
Антибиотики группы аминогликозидов
Гентамицина сульфат раствор для инъекций 40 мг (1 мл) — детям до 2 лет — 2–5 мг/кг/сут, детям старше 2 лет — 3–5 мг/кг/сут. Кратность введения 3 раза в сутки. Взрослым 3–5 мг/кг/сут, кратность введения 2–4 раза в сутки. Курс лечения 7–10 дней.
Антибиотики группы линкозамидов
Клиндамицин 150 мг — при приеме внутрь детям по 3–6 мг/кг 4 раза в сутки, взрослым по 150–450 мг 4 раза в сутки; при парентеральном введении детям 15–40 мг/кг/сут, взрослым — 600 мг — 2,7 г в сутки, кратность введения 3–4 раза в сутки. Курс лечения — 10 дней.
Наружное лечение
В начальной стадии на образующиеся узлы наносят 4-5 раз в день 50% раствор димексида с антибиотиком (доксициклином или рифампицином), в качестве альтернативы можно использовать чистый ихтиол, который 1-2 раза в сутки накладывают на очаг поражения в виде лепешек, прикрытых ватой, при этом ранее наложенный ихтиол смывается теплой водой. По периферии высыпаний проводят обработку кожи (от здоровой к поражённой) 1-2% борным (салициловым) спиртом 1 раз в день ежедневно в течение 3-4 недель. После вскрытия узла ихтиол может накладываться только на краевую зону инфильтрата. На центральную часть вскрывшегося гидраденита накладывают сложенную в 4-6 слоёв марлевую салфетку с гипертоническим раствором хлорида натрия. Салфетка фиксируется бинтованием или сетчатым бинтом и меняется 2 раза в день до момента полного отхождения гноя. После этого применяются мази, содержащие антибактериальные вещества и средства, стимулирующие регенерацию (метилурацил, тетрациклин, эритромицин, линкомицин, банеоцин и. т.д.).
Иммунобиологические средства
Назначают в случаях рецидивирующих, упорно протекающих форм заболевания:
При лечении заболеваний стафилококковой этиологии, сопровождающихся бактериемией и сепсисом, используют:
Режим
Мытье в бане, ванне или под душем воспрещается! Волосы в области расположения гидраденита рекомендуется состричь. Запрещается удаление волос путем их сбривания.
Диета
Хирургическое лечение
Абсцедирующий гидраденит лечится хирургическим путем. Производится вскрытие и дренирование абсцессов.
Физиотерапия
В начальной стадии целесообразно применение сухого тепла в форме грелки, мешочка с песком, освещения лампой Соллюкс, рефлектором Минина, УВЧ.
Критерии эффективности лечения
Отсутствие свежих высыпаний, разрешение существующих элементов.
Показания для госпитализации
Множественные высыпания, наличие осложнений (синдром общей инфекционной интоксикации, регионарный лимфаденит и др.), хроническое течение заболевания.
Наиболее частые ошибки в лечении
Применение антибактериальных препаратов системного действия без проведения микробиологического посева гнойного содержимого с определением чувствительности к антибактериальным препаратам.
Гидраденит
Гидраденит гнойный (гидроаденит, «сучье вымя») — острое гнойное воспаление потовых желёз.
Возбудителем, так же (см. фурункулы, карбункулы) является стафилококк, чаще всего золотистый стафилококк (Staph. aureus).
Раньше заболевание связывали с нечистоплотностью, опрелостями, расчёсами и сахарным диабетом. В настоящее время первое место среди причин развития гнойного гидраденита занимают микротравмы во время бритья.
Инфекция попадает в проток потовой железы через микротравму, возникающую при бритье, а применяемые антиперспиранты препятствуют потоотделению и вымыванию стафилококков наружу, способствуя развитию микробного воспаления непосредственно в железе.
В начале образуется плотный, умеренно болезненный узелок, затем образуется инфильтрат с отёчной, гиперемированной, болезненной кожей над ним. Инфильтрат распространяется как правило поперёк подмышечной впадины, после чего в её середине образуется участок кожного некроза, через который после этого выделяется гной белого цвета. Из-за характерного вида гнойника произошло народное название заболевания – «сучъё вымя».
Задачей операции является рассечение и иссечение поражённой потовой железы. В случае нерадикального иссечения железы, после стихания гнойного процесса формируются свищи и течение процесса приобретает хронический характер.
В условиях стационара отделения гнойной хирургии ГКБ29 производится оперативное лечение, как при остром гнойном, так и при хроническом гидрадените. Сроки госпитализации в случае острого процесса обычно не превышают 3х дней.
Более подробную информацию о длительности стационарного пребывания и необходимых (в рамках предоперационной подготовки) результатах амбулаторного дообследования для радикального оперативного лечения хронического гидраденита Вы можете получить у наших специалистов на амбулаторном приеме в КДЦ ГКБ29 ( с пн по пт с 10.00 до14.00).
Государственная клиническая больница №29 им. Н.Э.Баумана – это современная многопрофильная высокотехнологичная больница с уникальной полуторавековой историей и традицией, оказывающая высококачественную медицинскую помощь в круглосуточном режиме.
Принципы диагностики и лечения хронического рецидивирующего фурункулеза
В настоящее время существует тенденция к росту хронических бактериальных и вирусных заболеваний, для которых характерны непрерывно рецидивирующее течение и малая эффективность антибактериальной и симптоматической терапии. Одним из таких заболеваний яв
В настоящее время существует тенденция к росту хронических бактериальных и вирусных заболеваний, для которых характерны непрерывно рецидивирующее течение и малая эффективность антибактериальной и симптоматической терапии. Одним из таких заболеваний является хронический рецидивирующий фурункулез (ХРФ). Фурункул развивается в результате острого гнойно-некротического воспаления волосяного фолликула и окружающих его тканей. Как правило, фурункул является осложнением остеофолликулита стафилококковой этиологии. Фурункулы могут возникать как одиночно, так и множественно (так называемый фурункулез).
В случае рецидивирования фурункулеза диагностируется хронический рецидивирующий фурункулез. Как правило, он характеризуется частыми рецидивами, длительными, вялотекущими обострениями, толерантными к проводимой антибактериальной терапии. В зависимости от количества фурункулов, распространенности и выраженности воспалительного процесса ХРФ классифицируется по степени тяжести (Л. Н. Савицкая, 1987).
Тяжелая степень: диссеминированные, множественные, непрерывно рецидивирующие небольшие очаги со слабой местной воспалительной реакцией, не пальпируемыми или слегка определяющимися регионарными лимфатическими узлами. Тяжелое течение фурункулеза сопровождается симптомами общей интоксикации: слабостью, головной болью, снижением работоспособности, повышением температуры тела, потливостью.
Средняя степень тяжести — одиночные или множественные фурункулы больших размеров, протекающие с бурной воспалительной реакцией, с рецидивами от 1 до 3 раз в год. Иногда сопровождается увеличением регионарных лимфатических узлов, лимфангоитом, кратковременным повышением температуры тела и незначительными признаками интоксикации.
Легкая степень тяжести — одиночные фурункулы, сопровождающиеся умеренной воспалительной реакцией, с рецидивами от 1 до 2 раз в год, хорошо пальпируемыми регионарными лимфатическими узлами, без явлений интоксикации.
Чаще всего пациенты, страдающие фурункулезом, получают лечение у хирургов, в лучшем случае на амбулаторном этапе им проводится исследование крови на сахар, аутогемотерапия, некоторым назначают и иммуномодулирующие препараты без предварительно проведенного обследования, и в большинстве случаев они не получают положительного результата от проведенной терапии. Цель нашей статьи — поделиться опытом ведения больных с ХРФ.
Основным этиологическим фактором ХРФ считается золотистый стафилококк, который встречается, по разным данным, в 60–97% случаев. Реже ХРФ вызывается другими микроорганизмами — эпидермальным стафилококком (ранее считавшимся апатогенным), стрептококками групп А и В и другими видами бактерий. Описана вспышка заболеваемости фурункулезом нижних конечностей у 110 пациентов, являвшихся пациентами одного и того же педикюрного салона. Возбудителем данной вспышки являлся Mycobacterium fortuitium, причем этот микроорганизм был выявлен в ванночках для ног, используемых в салоне. В большинстве случаев ХРФ из гнойных очагов высеваются антибиотикорезистентные штаммы золотистого стафилококка. По данным Н. М. Калининой, St. aureus в 89,5% случаев резистентен к пенициллину и ампициллину, в 18,7% — резистентен к эритромицину и в 93% случаев чувствителен к клоксациллину, цефалексину и котримоксазолу. В последние годы отмечается достаточно широкое распространение метициллин-резистентных штаммов этого микроорганизма (до 25% пациентов). По данным зарубежной литературы, наличие на коже или на слизистой оболочке носа патогенного штамма St. aureus считается важным фактором развития заболевания.
ХРФ имеет сложный и до сих пор недостаточно изученный патогенез. Установлено, что дебют и дальнейшее рецидивирование заболевания обусловлены целым рядом эндо- и экзогенных факторов, среди которых наиболее значимыми считаются нарушение барьерной функции кожных покровов, патология ЖКТ, эндокринной и мочевыделительной систем, наличие очагов хронической инфекции различной локализации. По данным проведенных нами исследований, очаги хронической инфекции различной локализации выявляются у 75–99,7% пациентов, страдающих ХРФ. Наиболее часто встречаются очаги хронической инфекции ЛОР-органов (хронический тонзиллит, хронический гайморит, хронический фарингит), дисбактериоз кишечника с увеличением содержания кокковых форм. У больных хроническим фурункулезом патология ЖКТ (хронический гастродуоденит, эрозивный бульбит, хронический холецистит) определяется в 48–91,7% случаев. У 39,7% пациентов диагностируется патология эндокринной системы, представленная нарушениями обмена углеводов, гормонпродуцирующей функции щитовидной и половых желез. У 39,2% больных с упорно текущим фурункулезом имеется латентная сенсибилизация, у 4,2% — клинические проявления сенсибилизации к аллергенам домашней пыли, пыльцы деревьев и злаковых трав, у 11,1% — повышенная концентрация сывороточного IgE.
Таким образом, для большинства больных ХРФ характерны непрерывно рецидивирующее течение заболевания (41,3%) при тяжелой и средней тяжести течения фурункулеза (88%) и длительные обострения (от 14 до 21 дня — 39,3%). У 99,7% пациентов выявлены хронические очаги инфекции различной локализации. В 39,2% случаев определялась латентная сенсибилизация к различным аллергенам. Основным возбудителем является St. aureus.
В возникновении и развитии хронического фурункулеза, наряду с особенностями возбудителя, его патогенными, вирулентными и инвазивными свойствами, наличием сопутствующей патологии, большая роль отводится нарушениям нормального функционирования и взаимодействия различных звеньев иммунной системы. Иммунная система, призванная обеспечить биологическую индивидуальность организма и, как следствие, выполняющая защитную функцию при контакте с инфекционными, генетически чужеродными агентами, в силу разных причин может давать сбой, что ведет к нарушению защиты организма от микробов и проявляется в повышенной инфекционной заболеваемости.
Иммунная защита от бактерий-патогенов включает два взаимосвязанных компонента — врожденный (носящий преимущественно неспецифический характер) и адаптивный (характеризующийся высокой специфичностью к чужеродным антигенам) иммунитет. Возбудитель ХРФ при попадании в кожу вызывает «каскад» защитных реакций.
При ХРФ выявляются нарушения практически всех звеньев иммунной системы. По данным Н. Х. Сетдиковой, 71,1% больных фурункулезом имели нарушения фагоцитарного звена иммунитета, что выражалось в снижении внутриклеточной бактерицидности нейтрофилов, дефектах образования активных форм кислорода. Дефекты, приводящие к нарушению миграции гранулоцитов, могут приводить к хроническим бактериальным инфекциям, что продемонстрировали в своей работе Kalkman и соавторы в 2002 г. Дефекты утилизации патогенов внутри фагоцитов могут быть обусловлены разными причинами и иметь тяжелые последствия (так, например, дефект НАДФН-оксидазы приводит к незавершенному фагоцитозу и развитию соответствующей тяжелой клинической картины). Низкие показатели уровня сывороточного железа, возможно, могут обусловливать снижение эффективности оксидативного киллинга патогенных микроорганизмов нейтрофилами. Рядом авторов выявлено снижение общего количества Т-лимфоцитов периферической крови. Как правило, у больных ХРФ снижено количество CD4-лимфоцитов (у 20–50% пациентов) и повышено количество CD8-лимфоцитов (у 14–60,4% пациентов).
У 26–35% больных, страдающих хроническим фурункулезом, снижается количество В-лимфоцитов. При оценке компонентов гуморального иммунитета у больных фурункулезом выявляются различные дисиммуноглобулинемии. Наиболее часто встречаются снижение уровней IgG и IgM. Отмечено снижение аффинности иммуноглобулинов у больных ХРФ, причем выявлена корреляция между частотой встречаемости этого дефекта, стадией и тяжестью заболевания. Тяжесть нарушений лабораторных показателей коррелирует с тяжестью клинических проявлений фурункулеза.
Из вышесказанного следует, что изменения показателей иммунного статуса у больных ХРФ носят разноплановый характер: у 42,9% отмечено изменение субпопуляционного состава лимфоцитов, у 71,1% — фагоцитарного и у 59,5% — гуморального звена иммунной системы. В зависимости от выраженности изменений в показателях иммунного статуса больных ХРФ можно разделить на три группы: легкой тяжести, средней и тяжелого течения, что коррелирует с клиническим течением заболевания. При легком течении фурункулеза у большинства больных (70%) показатели иммунного статуса находятся в пределах нормы. При средней и тяжелой степени преимущественно выявляются изменения фагоцитарного и гуморального звеньев иммунной системы.
Диагностика и лечение ХРФ
Исходя из вышеуказанных патогенетических особенностей ХРФ алгоритм диагностики должен включать в себя выявление очагов хронической инфекции, диагностику сопутствующих заболеваний, оценку лабораторных параметров состояния иммунной системы (рис.).
В нашем институте был разработан план обследования больных ХРФ.
Тактика лечения больных ХРФ определяется стадией заболевания, сопутствующей патологией и иммунологическими нарушениями. В стадии обострения ХРФ требуется проведение местной терапии в виде обработки фурункулов антисептическими растворами, антибактериальными мазями, гипертоническим раствором; в случае локализации фурункулов в области головы и шеи или наличия множественных фурункулов — проведение антибактериальной терапии с учетом чувствительности возбудителя. В любой стадии заболевания необходима коррекция выявленной патологии (санация очагов хронической инфекции, лечение патологии ЖКТ, эндокринной патологии и т. д.). При выявлении у больных ХРФ латентной сенсибилизации или при наличии клинических проявлений аллергии необходимо в период поллинации добавлять к лечению антигистаминные препараты, назначать гипоаллергенную диету, проводить хирургическое вмешательство с премедикацией гормональными и антигистаминными препаратами.
В последнее время в комплексной терапии больных ХРФ все чаще используют препараты, оказывающие корригирующее действие на иммунную систему.
Разработаны показания к назначению иммуномодуляторов в зависимости от доминирующего типа нарушений иммунного статуса и степени заболевания. Так, в стадии обострения ХРФ рекомендовано применение следующих иммуномодуляторов.
В период ремиссии возможно назначение следующих иммуномодуляторов.
Применение ликопида целесообразно также при вялотекущем, непрерывно рецидивирующем фурункулезе. При упорном рецидивировании ХРФ на фоне изменений гуморального звена иммунитета показано назначение препаратов иммуноглобулина для внутривенного введения (октагам, габриглобин, интраглобин). В некоторых случаях целесообразно комбинированное применение иммуномодулирующих препаратов (например, при обострении фурункулеза возможно назначение полиоксидония, в дальнейшем, при выявлении дефекта аффинности иммуноглобулинов, добавляется галавит и т. д.).
Несмотря на значительные успехи, достигнутые в области клинической иммунологии, эффективное лечение ХРФ остается достаточно сложной задачей. В связи с этим требуется дальнейшее изучение патогенетических особенностей этого заболевания, а также разработка новых подходов к терапии ХРФ.
В настоящее время продолжается поиск новых иммуномодулирующих препаратов, способных оказывать положительное влияние на течение воспалительного процесса при фурункулезе. Проводятся клинические испытания новых отечественных иммуномодуляторов, таких, как серамил, неоген. Серамил является синтетическим аналогом эндогенного иммунорегуляторного пептида — миелопептида-3 (МП-3). Серамил применялся в составе комплексной терапии больных ХРФ как в стадии обострения, так и в стадии ремиссии по 5 мг № 5 внутримышечно. После лечения препаратом отмечались нормализация уровня В-лимфоцитов, а также снижение уровня СD8-лимфоцитов. Выявлено значительное удлинение сроков ремиссии заболевания (до 12 мес у 30% пациентов).
Таким образом, из вышеизложенного следует, что ХРФ протекает под воздействием сложного комплекса этиологических и патогенетических факторов и его нельзя рассматривать только как местное воспаление. Больным с ХРФ необходимо проводить всестороннее обследование с целью выявления возможных очагов хронической инфекции, которые являются источником септицемии и при нарушении элиминации микробов в крови в результате снижения иммунологической реактивности организма приводят к возникновению фурункулов. Так как назначение иммунокорригирующих препаратов может вызвать обострение основного заболевания, мы считаем, что лечение больных необходимо начинать с санации выявленных очагов инфекции.
Вопрос о назначении иммунокорригирующих препаратов должен решаться индивидуально, с учетом стадии заболевания, наличия сопутствующей патологии и типа иммунологического дефекта. При выявлении у больного сенсибилизации к различным аллергенам лечение фурункулеза необходимо проводить на фоне противоаллергенной терапии.
Н. Х. Сетдикова, доктор медицинских наук
К. С. Манько
Т. В. Латышева, доктор медицинских наук, профессор
Гнойный гидраденит и микробиом
Гнойный гидраденит и микробиом
Клиническая значимость микробиома при суппуративном гидрадените: систематический обзор
Введение
Гнойный гидраденит – это хронический, приводящий к рубцеванию акнеподобный аутовоспалительный процесс, который возникает в области подмышечных ямок, паха, вокруг сосков и ануса. Диагноз ставится при осмотре. Лечение зависит от стадии – ред.
1. Введение

Сложная роль микробиома была исследована при различных кожных заболеваниях, включая псориаз, атопический дерматит и другие заболевания PSU, такие как угри [6,7,8]. В этом обзоре мы внимательно изучаем существующую литературу относительно того, как микробиом кожи в ГГ-коже отличается от микробиома здоровой кожи, провоцирует ли он или усиливает болезнь, как он изменяется в ответ на терапию и можно ли манипулировать им, чтобы изменить течение болезни.
2. Материалы и методы
Обзор литературы, относящейся к гнойному гидрадениту и микробиому кожи, был проведен в PubMed, Science Direct и Google scholar. Использовались следующие термины в медицинских предметных рубриках (MeSH): «гидраденит», «гнойник», «угри», «инверсия», «патофизиология», «микробиом», «кожный», «кишечник», «кишечный», «дисбактериоз», «биопленка», «антибиотик», «бактерии», «грибы», «пробиотик», «биомаркер». Использовались логические операторы «И» и «ИЛИ». Были включены геномные исследования, изучающие изменения в составе или характеристиках микробиома кожи, в исследованиях на людях или животных. Кроме того, были также включены исследования, изучающие роль оси кишечник–кожа в ГГ, а также влияние диеты или антибиотиков на модуляцию микробиомов кожи ГГ и риск заболевания, прогрессирование и исход. Поиск охватывал статьи, опубликованные в период с января 1990 года по июль 2021 года, и ограничивался статьями, опубликованными на английском языке. Кроме того, были также проведены ручной поиск и анализ цитирования соответствующих исследований для выявления исследований, которые не были охвачены поиском в электронной базе данных.
Исследования были исключены, если они непосредственно не исследовали связь между микробиомом кожи и ГГ. Более конкретно, статьи, основной целью которых было исследование состава кожи или микробиома кишечника при метаболическом синдроме или его компонентов, не были включены. Статьи, написанные не на английском языке, рецензии, редакционные письма и комментарии были исключены.
3. Результаты
3.1. Микробиота человека
Микробиота человека описывает сложный набор микроорганизмов, которые колонизируют кожу и несколько слизистых оболочек, включая желудочно-кишечный тракт, дыхательные пути и мочеполовые пути. Эти микроорганизмы образуют сложную и дискретную экосистему, которая поддерживает комменсальные отношения с нормальной физиологией хозяина. Кроме того, изменения микробиоты замысловато вовлечены в несколько болезненных процессов через модуляцию метаболизма и иммунитета. Величина и разнообразие микробиоты человека по сравнению с соматическими клетками обширны. По последним оценкам, соотношение бактериальных клеток на клетку человека составляет 1,3, и, по оценкам, в организме человека одновременно обитает 500–1000 видов бактерий [9,10]. Эти оценки не учитывают грибки и вирусы. Кроме того, микроорганизмы демонстрируют значительное разнообразие, каждый из которых имеет несколько генетически уникальных подвидов. В совокупности каталог микробного генома (микробиома) превышает приблизительно 20 000 генов человека на несколько порядков [11,12]. Микробиом человека не статичен, а развивается в ответ на широкий спектр элементов хозяина, включая возраст, образ жизни, диету, эндокринные факторы и основные заболевания. Кроме того, сообщается о значительной степени межиндивидуальной неоднородности даже при отсутствии заболевания [13]. Эти факторы демонстрируют динамичный характер экосистем микробиома человека, которые эволюционировали совместно, чтобы адаптироваться к постоянно меняющимся физиологическим условиям хозяина. Они также усложняют наше понимание изменений в микробиоме, которые причинно связаны с заболеванием или отражают текущую патологию. Изменения в составе микробиоты человека (или дисбиоз) были связаны с несколькими заболеваниями, начиная от воспалительных заболеваний кишечника, злокачественных новообразований, астмы, диабета 1 и 2 типа и заканчивая большим депрессивным расстройством [14,15,16,17,18,19].
3.2. Исследование микробиома кожи
Последнее десятилетие стало свидетелем всплеска исследований микробиома, обусловленного методологическими достижениями в этой области. Двумя основными подходами к исследованию микробиома, основанными на секвенировании, являются метатаксономика и метагеномика [20]. Метатаксономика включает целенаправленную амплификацию и секвенирование маркерных генов, которые специфически консервативны для разных таксонов, таких как ген рибосомной 16S РНК у бактерий и внутренний транскрибируемый спейсер 1 (ITS1) у грибов. Эти гены характеризуются гипервариабельными областями, которые позволяют идентифицировать виды, и содержат консервативные области, на которые могут быть нацелены универсальные праймеры [21]. Метатаксономические методы позволяют быстро и экономично идентифицировать микроорганизмы. Однако они обладают рядом недостатков. Они не могут захватывать вирусные последовательности, а секвенирование ампликонов с коротким считыванием не может обеспечить разрешение на уровне видов. Кроме того, некоторые исследования выявили ограничения секвенирования 16S рРНК для обнаружения бактерий [22,23].
Метагеномика основана на случайном секвенировании микробной ДНК без предварительного выбора конкретных локусов. Этот метод позволяет производить сборку геномов de novo и свободен от предвзятости амплификации, поскольку он секвенирует весь генетический материал в данном образце. Важно отметить, что метагеномные подходы позволяют оценивать относительную численность различных царств и позволяют проводить оценку микроорганизмов с высоким разрешением на уровне видов и штаммов [24]. Они представляют собой значительные преимущества перед подходами на основе ампликонов и объясняют растущую популярность анализов на основе метагеномики. Метагеномные исследования требуют большого количества считываний, требуют выравнивания с эталонным геномом для классификации и могут захватывать большое количество считываний из организма-хозяина [25].
Также доступны дополнительные подходы multi-omics. Эти методы дополняют данные секвенирования транскриптомными, протеомными и метаболомными данными для улучшения профилирования микробных сообществ [26]. Подробный обзор подходов к микробным мультиомикам представлен Franzosa et al. [27]. Хотя такие подходы выходят за рамки данной статьи, они обеспечивают прямое понимание функциональной активности микробиоты на транскрипционном и метаболическом уровнях, что подтверждается протеомными и метаболомными исследованиями в кишечнике человека [28,29]. По мере дальнейшего развития методов интеграции многомерных наборов данных ожидается улучшение понимания биологии микробиоты в отношении здоровья и болезней, что будет способствовать прогрессу в области открытия биомаркеров или разработки методов лечения.
Кожа человека представляет собой уникальную среду с низкой микробной биомассой, высоким риском заражения и широким разнообразием микробиоты в сочетании с местными микроорганизмами. Эти элементы требуют важных соображений при микробных исследованиях, чтобы избежать систематической ошибки. И исследователям, и клиницистам важно понимать, что сопоставимость исследований микробиома может быть ограничена несколькими элементами. К ним относятся отбор образцов и методологические различия между исследованиями, а также лабораторные факторы во время экстракции ДНК и последующей обработки [30,31,32,33,34]. Kong et al. рассмотрены стандарты исследования микробиома кожи и выделены несколько факторов и подводных камней, которые следует учитывать при проведении или интерпретации исследования микробиома кожи [35].
3.3. Состав и разнообразие микробиома кожи человека
Кожа, являясь крупнейшим контактом тела с внешней средой, является домом для множества симбиотических и комменсальных микроорганизмов. Микробиота кожи управляет несколькими ключевыми гомеостатическими процессами, включая защиту от патогенов, развитие иммунной системы и расщепление природных продуктов посредством двунаправленного метаболического обмена с клетками-хозяевами [36,37]. Нарушение естественного баланса между комменсальными и патогенными микробами может привести к кожным или даже системным заболеваниям, поэтому далее представлено подробное понимание свойств здорового микробиома кожи.
Метагеномные исследования кожи также позволяют с высоким разрешением исследовать бактериальные сообщества кожи на уровне разнообразия штаммов. Различные бактериальные штаммы могут отличаться по трансмиссивности, вирулентности, устойчивости к антибиотикам и метаболизму. Следовательно, анализ разрешения деформации может иметь значение для здоровья и болезней. Oh et al. применили анализ штаммов к обычным кожным комменсалам Cutibacterium acnes и Staphylococcus epidermidis. Они показали, что различия в распределении штаммов S. epidermidis в первую очередь обусловлены анатомическим сайтом, тогда как распределение штаммов Cutibacterium acnes является индивидуально-специфичным, а не сайт-специфичным [39].
3.4. Перекрестные помехи между микробиотой кожи и иммунной системой
Иммунная система играет центральную роль в поддержании комменсальных микроорганизмов кожи и устранении патогенных микробов. Между врожденными и адаптивными звеньями иммунной системы, кератиноцитами и микробиотой кожи происходит активное взаимодействие. Кератиноциты экспрессируют рецепторы распознавания патогенов, которые распознают и связываются с ассоциированными с патогенами молекулярными структурами, вызывая микробицидные и провоспалительные реакции врожденного иммунитета для устранения или сдерживания вредных патогенов [48]. Эпителиальные клетки кожи продуцируют широкий спектр антимикробных пептидов (AMPs), включая несколько белков (дефензины, кателицидины и другие), которые обладают антибактериальной, противогрибковой и антипаразитарной активностью [49,50]. Комменсалы кожи участвуют в развитии и регуляции кожного адаптивного иммунитета [51]. Неонатальный период представляет собой решающее окно для установления иммунной толерантности к комменсальным микробам. Симбиоз хозяина и комменсала в коже человека зависит от регуляторных Т-клеток [52]. После начального периода иммунной толерантности кожные комменсалы вызывают отчетливые эффекты на иммунную систему посредством передачи сигналов интерлейкина-1, при этом индукция эффекторных Т-клеток происходит в отсутствие классического воспаления [53]. Таким образом, микробиом кожи играет решающую роль в индукции и формировании иммунитета хозяина, обеспечивая устойчивую толерантность к безвредным антигенам, процесс, называемый «гомеостатическим иммунитетом» [54]. И наоборот, когда кожные комменсалы вводятся системно, например, при нарушении кожного барьера, возникает классический воспалительный ответ. Это демонстрирует, как отношения микробиом-хозяин зависят от контекста, от комменсального до патогенного и в зависимости от факторов хозяина, и как нарушение регуляции диалога хозяин-микробиом может приводить к хроническим воспалительным ответам хозяина.
3.5. Кожный дисбиоз
3.6. Кожный дисбактериоз при суппуративном (гнойном) гидрадените (ГГ)
Несколько исследований охарактеризовали перекос микробиома кожи, которые отличают ГГ. Секвенирование следующего поколения (NGS), нацеленное на 16S рРНК, использовалось в различных контекстах заболевания. Краткое изложение основных исследований с использованием этого метода представлено в таблице 1.
Таблица 1. Исследования с использованием секвенирования нового поколения, нацеленного на 16S рРНК, для раскрытия микробиома в различных типах образцов пациентов с гнойным гидраденитом (ГГ).
Кожа при ГГ, по-видимому, имеет микробиом, отличный от микробиома здоровой кожи, и который в подавляющем большинстве населен анаэробными грамотрицательными бактериями [68]. Различия в микробиоме ГГ можно обнаружить даже при отсутствии клинически наблюдаемых поражений [69]. Тестирование дифференциальной численности генов (которое относится к статистическому методу исследования значимости численности конкретных видов бактерий в двух разных экосистемах) показало значительные различия между пораженной и здоровой (контрольной) кожей, а также между пораженной и непораженной кожей [70]. Однако сравнение неповрежденной и здоровой кожи не показывает существенной разницы в численности видов бактерий [71]. Функциональный анализ также подтверждает значительные метагеномные различия между пораженной и здоровой контрольной кожей, а также между пораженной и неповрежденной кожей, но не между неповрежденной и здоровой контрольной кожей [71]. Микробиом может варьироваться даже в зависимости от типа поражения ГГ, при этом Staphylococcus lugdunensis ассоциируется с узелками и абсцессами, полимикробными анаэробами с хроническими гнойными поражениями и анаэробными актиномицетами с тяжелыми гнойными поражениями [72].
Другие недостатки кожного иммунного ответа ГГ на патогенные организмы включают снижение концентрации антимикробного пептида дермцидина, который естественным образом обнаруживается в человеческом поте [78,79]. Дермцидин также обнаруживается в более низких концентрациях в плазме, а также в пораженной коже пациентов с акне, по сравнению с контрольной группой, и увеличивается при лечении низкими или стандартными дозами изотретиноина, ретиноида, который с переменным успехом использовался для лечения ГГ [80,81,82,83,84].
Еще одним возникающим патогенным фактором при различных кожных заболеваниях, включая ГГ, является биопленка [85]. Биопленки представляют собой микробные агрегаты, взвешенные в самостоятельно производимой суспензии внеклеточных полимерных веществ [86]. Гистологическая оценка кожи ГГ показывает, что она залита биопленкой [87]. У 10 пациентов с ГГ, кожа которых была поражена воспаленными узелками, у двух из них были обнаружены биопленки, что позволяет предположить, что бактерии, связанные с биопленкой, связаны не только с хроническими поражениями, такими как синусовые пути, но и с острыми поражениями, такими как узелки [88]. Непораженная ГГ кожа подмышек также демонстрирует присутствие биопленки, подтверждая гипотезу о том, что ГГ является заболеванием бактериальной биопленки [89].
Определенные процессы способствуют склонности кожи ГГ к размещению биопленки. Показано, что S. epidermidis, обычно не вирулентный комменсал в здоровой коже, обладает склонностью к планктонному росту и образованию биопленки как в пораженной, так и в не пораженной ГГ коже [90]. Эта бактерия является распространенной CNS у пациентов с ГГ [91]. Обеспокоенность вызывает S. epidermis в пораженной коже, которая демонстрирует устойчивость к антибиотикам, рекомендованным в руководствах, таким как тетрациклины и клиндамицин [90,92]. Потенциал образования биопленок других CNS, таких как Staphylococcus lugdunensis, также повышается в пораженной ГГ коже по сравнению с непораженными, контрольными и эталонными штаммами [93].
Было обнаружено, что пациенты с ГГ с идентифицированными биопленками имеют повышенную концентрацию CD4 + клеток по сравнению со здоровым контролем (с биопленкой или без нее) и пациентами с ГГ без биопленки. Эти данные свидетельствуют о том, что биопленки могут стимулировать производство регуляторных Т-клеток, что приводит к усилению иммуномодулирующего ответа [89]. С другой стороны, здоровые пациенты имеют тенденцию удерживать биопленки, в которых преобладают кокки [94]. Это говорит о том, что состав биопленки частично определяет гомеостаз кожи.
Следующим шагом в расшифровке сложности ГГ как болезни PSU является исследование состава фолликулярного микробиома. Метатаксономические исследования генов бактериальной 16S рРНК и эукариотической 18S рРНК, проведенные при кожных биопсиях, показали, что фолликулы пораженной кожи содержат большое количество видов Corynebacterium, Porphyromonas и Peptoniphilus, в то время как Acinetobacter и Moraxella преобладают в непораженной коже [64]. Как вид, C. acnes и C. striatum значительно более многочисленны в фолликулах здоровых людей по сравнению с пораженной кожей [64]. Богатство видов бактерий, по-видимому, не отличается между ГГ и здоровым контролем [64].
Рассмотрена роль отдельных видов бактерий в патологии ГГ [95]. Однако с клинической точки зрения важно признать, что некоторые организмы, такие как Actinomyces schaalii, могут усугублять болезненное состояние, вызывая образование абсцесса, что может быть не связано с ГГ и PSU в целом [96]. Узелки, вторичные по отношению к глубокому дерматофитозу у пациентов с ГГ, также могут быть ошибочно приняты за злокачественную трансформацию хронически пораженной кожи ГГ, что является известной ассоциацией [97,98,99]. Быстрая идентификация таких патогенов, включая медленнорастущие организмы, такие как Actinomyces neuii, имеет важное значение для предотвращения искажающей симптоматики [100].
3.7. За пределами микробиома кожи
Хотя ГГ проявляется в коже, другие микробиомы, такие как микробиом кишечника, обладают потенциалом опосредовать заболевание, облегчая системные воспалительные пути, поддерживаемые осью кишечник – кожа [101]. Эта патофизиологическая ось была охарактеризована при атопическом дерматите, псориазе и розацеа [102, 103, 104]. Кишечная микробиота может влиять на микробиоту кожи, приводя к кожному дисгомеостазу, который в конечном итоге может привести к кожной патологии, включая PSU-патологию, такую как прыщи [101].
В соответствии с другими патофизиологическими теориями дисбактериоз кишечника может также усиливать ГГ, опосредуя воспаление. Было высказано предположение, что при кишечном дисбиозе (потенциально вызванном диетой с высоким содержанием жиров) повышаются воспалительные цитокины, такие как Il-1β, Il-17 и TNF-α. В конечном итоге это приводит к повышению уровня матриксных металлопротеиназ и, как следствие, образованию поражений ГГ у восприимчивых людей [105].
Методы амплификации 16S рРНК образцов фекалий использовались для сравнения кишечного и кожного микробиома пациентов с ГГ и здоровых контрольных субъектов [106,107]. Заслуживает внимания Робинсониелла (Robinsoniella), которая была обнаружена исключительно на лицах пациентов с ГГ [106], характерная черта ГГ, характерная для ревматоидного артрита и анкилозирующего спондилита [106]. Похоже, что разнообразие кишечных видов может быть уменьшено у пациентов с ГГ в соответствии с другими воспалительными состояниями, такими как воспалительное заболевание кишечника (ВЗК) [108].
Косвенное свидетельство особой роли микробиома может быть получено из сопутствующего заболевания. Например, количество Faecalibacterium prausnitzii было истощено у пациентов с сопутствующим ГГ и ВЗК, но не у пациентов, страдающих исключительно ГГ [109]. Относительное обилие F. prausnitzii, по-видимому, не уменьшается по сравнению со здоровым контролем. Обогащение подвидов F. prausnitzii было связано с другими воспалительными дерматозами, включая атопический дерматит [110].
Микробиом кишечника может также распутать молекулярные процессы, связывающие ГГ с ожирением, что является значительным фактором риска заболевания [111]. На мышиных моделях сообщалось о положительной корреляции между количеством Firmicutes в микробиоме кишечника и массой тела, в то время как Bacteroides spp. отрицательно коррелируют с массой тела. Относительное количество Lactobacillus также увеличивается у мышей, набирающих вес за счет диеты с высоким содержанием жиров [112]. Установленные факторы риска ГГ, такие как ожирение, могут затем оказывать прямое влияние на микробиом кожи, образуя петлю обратной связи. Было показано, что S. aureus, Enterococcus и Proteus с большей вероятностью будут культивироваться при ГГ с ожирением, чем у худых пациентов с ГГ [113]. Висцеральное ожирение сопровождается системным субклиническим провоспалительным состоянием. Частично это опосредуется IL-16, IL-1 и TNF-α. Также существуют важные различия в микробиоме кишечника, связанные с ожирением и метаболическим синдромом, которые следует рассматривать как факторы, влияющие на метагеномные исследования ГГ [114].
Дополнительным серологическим свидетельством, подтверждающим роль микробиома в воспалительном заболевании, является наличие у пациентов с ГГ антител против Saccharomyces cerevisiae ( ASCA s ), которые также связаны с жировой массой тела [116,117]. Было высказано предположение, что положительность ASCA может быть связана со специфическим основным генотипом ГГ, поскольку это антитело было связано с пациентами с болезнью Крона, несущими специфические варианты NOD2 [118,119].
3.8. Нацеливание на микробиом как метод лечения
Нацеливание на микробиом представляется логичным вариантом ведения пациентов с ГГ. Характеристика микробиома кожи с использованием геномных методов может иметь прямое применение у постели больного. Это было проиллюстрировано на примере пациента, страдающего коморбидными устойчивыми угрями молниеносного происхождения и ГГ, которого успешно лечили антибиотиками таргетного действия после выявления микробиома пораженной кожи с помощью NGS [120]. Антибиотики также успешно применялись для индукции ремиссии ГГ у пациентов с синдромальными формами заболевания [121].
Туннели представляют собой еще одну проблему в медицинском управлении ГГ. Их значимость отражена в системе стадирования Херли (часто используемая статическая оценка тяжести), поскольку их наличие отличает пациентов с ГГ средней и тяжелой степени от легкой формы заболевания. Было показано, что рифампицин исключительно эффективно препятствует планктонному росту и устраняет биопленку в туннелях пациентов с ГГ [90,93]. Многообещающие результаты были получены после введения триамцинолона в синусовые тракты. Однако окончательным лечением синусовых путей остается хирургическое иссечение [122].
Несмотря на важность антибиотиков для лечения пациентов, страдающих ГГ, резистентность к антибиотикам у пациентов с ГГ является значительной и продолжает расти. Распространенность устойчивости к антибиотикам может достигать 84,7% к тетрациклинам, 69,3% к рифампицину и 65,7% к клиндамицину [123]. Первые представляют собой антибиотики, рекомендованные для лечения ГГ европейскими, британскими и американскими руководящими принципами [92]. Помимо разумного использования антибиотиков и своевременного введения биологических препаратов для предотвращения повторных обострений, могут быть приняты другие меры для снижения устойчивости к антибактериальным препаратам. Например, смывки с антимикробными препаратами могут изменять устойчивость поражений ГГ к антибиотикам, особенно к цефалоспоринам [124].
Уместно учитывать, что антибиотики, в том числе тетрациклины (считающиеся препаратами первой линии для лечения ГГ), могут способствовать ремиссии заболевания не только за счет их бактериостатического или бактерицидного действия, но также благодаря своим дополнительным противовоспалительным и антиколлагенолитическим свойствам [125]. Такие наблюдения подчеркивают лежащую в основе воспалительную природу ГГ и повышенный риск других коморбидных метаболических заболеваний (включая метаболический синдром), характеризующихся хронической воспалительной реакцией слабой степени [126]. Идентификация молекулярных медиаторов ГГ может позволить перепрофилировать лекарство посредством выяснения взаимодействия лекарство-ген, открывая путь для новых таргетных терапевтических агентов [127].
3.8.2. Кишечный микробиом и диета
Помимо использования антибиотиков, изменение кишечного микробиома может изменить траекторию заболевания. Использование пробиотиков для лечения ГГ было предложено в качестве потенциального варианта лечения путем восстановления микробиома кожи, пополнения запасов Cutibacterium spp., Corynebacterium и Staphylococcus и, таким образом, восстановления здорового микробиома, который менее распространен среди грамотрицательных анаэробов [68,128].
Послеоперационное диетическое ограничение пивных дрожжей у пациентов со специфическими IgG к Saccharomyces cerevisiae также привело к ремиссии заболевания. Интересно, что пациенты испытывают рецидив заболевания при повторном контакте с одноклеточным грибком [129]. Исключение из рациона Saccharomyces cerevisiae в течение более длительного периода также способствовало ремиссии заболевания у пациентов с ГГ [130].
Как было описано ранее, ожирение и ГГ тесно связаны, причем пациенты с ГГ, страдающие ожирением, имеют отчетливый фенотип ГГ [131]. Было показано, что у мышей, выращенных на диете с высоким содержанием жиров, наблюдается повышенная локальная выработка воспалительных цитокинов, таких как TNF-α, IL-1β и IL-6. Эти цитокины не были обнаружены повышенными у тех же мышей на 8-й неделе диеты с высоким содержанием жиров. Однако уровни сывороточного TNF-α и IFN-γ были повышены на 12 неделе и, как было обнаружено, положительно коррелировали с весом [112]. Это говорит о том, что диета может изменять микробиом кишечника и местные воспалительные цитокины, в то время как ожирение, которое неразрывно связано с диетой, может способствовать более системным формам воспаления.
Биомаркеры определяются как «объективные признаки медицинского состояния, наблюдаемые за пределами пациента и которые можно измерить точно и воспроизводимо» [132]. Биомаркеры могут помочь прогнозировать и диагностировать состояние пациентов. Они были ценными инструментами при лечении других воспалительных заболеваний кожи, таких как псориаз. Однако они еще не были подробно охарактеризованы и подтверждены при ГГ [133]. Микробиом кожи может действовать как биомаркер [134].
3.9.1. Прогностический биомаркер
Микробиом может выступать в качестве прогностического биомаркера ГГ. Пациенты с тяжелой формой болезни (стадия Херли III) имеют большее количество видов бактерий [91]. Выделение бактерий, таких как Streptococci, Enterobacteriaceae и облигатно-анаэробных грамотрицательных палочек, также связано с более тяжелым заболеванием [91]. Аналогичным образом были установлены умеренные, но значимые положительные корреляции между тяжестью заболевания ГГ и относительной численностью смешанных анаэробов. Умеренно отрицательная корреляция была обнаружена для основных комменсалов кожи, включая Cutibacterium и Corynebacterium spp. [69]. Противоречивые результаты были получены в отношении корреляции тяжести ГГ и S. aureus [69,91,135].
Положительность ASCA также была связана с тяжелой болезнью (стадия Херли 3) [116]. Присутствие бактериальной ДНК в периферической крови связано со значительно более высокими уровнями провоспалительных цитокинов, таких как TNF-α, IL-1β и IL-17, но не коррелирует с тяжестью заболевания [67].
3.9.2. Биомаркер риска
3.9.3. Фармакодинамический биомаркер
Микробиом демонстрирует потенциал в качестве фармакодинамического биомаркера. В небольшом когортном исследовании было обнаружено, что пациенты с ГГ средней и тяжелой степени, которые переносят S. aureus назально, с большей вероятностью будут испытывать вспышки ГГ, которые приводят к отказу от терапии адалимумабом на 12 неделе, чем те, кто не переносит бактерию (OR 8.67, p = 0.014) [136].
4. Обсуждение
Между микробиомом, воспалением и ГГ существует сложная взаимосвязь (рис. 1). ГГ как воспалительное состояние подвержено влиянию дисбактериоза кожного или кишечного. В различных исследованиях изучалась взаимосвязь между болезнью и микробиомом с использованием ряда методов отбора проб и обнаружения. Помимо подчеркивания стремления исследователей ГГ к полному пониманию патофизиологии ГГ, они также выдвигают на первый план важность глобальной гармонизации методологии выборки в исследованиях ГГ [137].
Рисунок 1. События, приводящие к кожному дисбиозу у пациентов с гнойным гидраденитом (ГГ).
Помимо своей роли в патофизиологии, микробиом потенциально может быть целевым вариантом лечения для изменения траектории заболевания. Было показано, что большинство антибиотиков, используемых для лечения ГГ, обладают противовоспалительными свойствами. Однако отсутствуют исследования в отношении изменения микробиома после терапии антибиотиками или любого терапевтического вмешательства [138]. Использование модификации диеты в качестве терапевтического вмешательства при лечении заболевания имеет ряд преимуществ, включая отсутствие связанных с этим негативных эффектов и низкое финансовое бремя для пациента. Уход за пациентами с ограничительной диетой должен контролироваться диетологами, которые идеально знакомы с ГГ и его лечением как часть многопрофильной команды, обеспечивающей индивидуальный уход за пациентами с ГГ. Как указано выше, достижения в области геномных технологий могут облегчить доведение результатов исследования до использования в лечении, направляя ведение сложных случаев ГГ. Помимо своих терапевтических функций, микробиом потенциально может служить биомаркером заболевания для облегчения классификации заболеваний, стратификации пациентов и мониторинга реакции на лечение. Однако для выявления и проверки таких инструментов требуются дальнейшие исследования. Кроме того, микробиом также может помочь уточнить ассоциации генотип-фенотип, что является еще одним пробелом в нашем понимании ГГ [139].
Исследования, представленные в этом обзоре, предоставляют убедительные доказательства нарушения регуляции микробиома пораженной кожи при ГГ. Однако нельзя предполагать прямую причинно-следственную связь, и возникает ряд вопросов. Прежде всего, не до конца понятна роль непоражающей кожной микробиоты в патогенезе ГГ. Более конкретно, характеристика эволюции микробного состава и численности во время перехода от непораженной кожи к поврежденной должна дать представление о причинных траекториях, ведущих к ГГ. Можно предположить, предшествовали ли изменения микробиоты развитию ГГ, представляя, таким образом, латентную или доклиническую стадию заболевания. Альтернативно, возможно, что наблюдаемый кожный дисбиоз при ГГ частично отражает адаптивную микробную реакцию на острое воспаление при активных поражениях ГГ. С физиологической точки зрения вполне вероятно, что микробиота способствует причинно-следственной связи, прогрессированию и поддержанию ГГ на сложном фоне иммунного ответа хозяина. Эти факторы вместе определяют последующую клиническую картину и реакцию на терапию.
В заключение, ГГ представляет собой сложное состояние, с изменениями, предшествующими клиническим признакам и симптомам, и различающимися в зависимости от поражения и анатомического расположения. Возможные будущие исследования могут быть направлены на изучение того, связано ли воздействие окружающей среды (гигиеническая гипотеза) в детстве с дисбактериозом и траекторией заболевания в дальнейшей жизни. Элегантное объединяющее патофизиологическое объяснение ГГ еще не установлено. Раскрытие роли микробиома в ГГ приблизит нас на шаг к этой цели.
Дополнительная информация:
Литература
Будьте здоровы!
ССЫЛКИ К РАЗДЕЛУ О ПРЕПАРАТАХ ПРОБИОТИКАХ