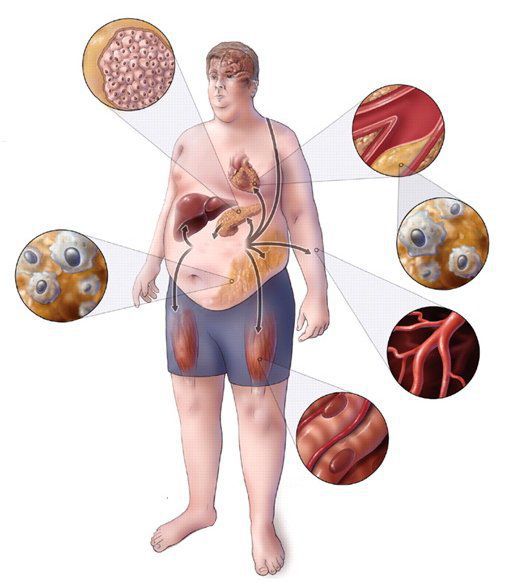
Метаболический синдром: симптомы и диагностика нарушений обмена веществ
Метаболический синдром (МС) – это комплекс патологий, которые увеличивают риск возникновения сердечно-сосудистых заболеваний, инсульта и инфаркта.
Симптомы метаболического синдрома
По сути, метаболический синдром не является самостоятельным заболеванием. Это группа симптомов, которые часто встречаются вместе и увеличивают риск других – еще более тяжелых – нарушений.
Тревожные тенденции
Еще недавно метаболическим синдромом страдали преимущественно пожилые люди (старше 60 лет). Картина существенно изменилась за последние 20 лет. Динамика показала, что эта проблема молодеет и становится актуальной для более юного населения. В ряде стран доля взрослого населения, страдающая от этих симптомов, достигает 25%.
У метаболического синдрома есть еще одно название – «синдром нового мира». Дело в том, что преимущественно от ожирения и связанных с ним патологий страдают люди, ведущие малоподвижный образ жизни (а это касается преобладающего числа жителей больших городов), употребляющие большое количество быстрых углеводов и трансжиров. В результате во всем мире наблюдается всплеск сердечно-сосудистых заболеваний и диабета.
Метаболический синдром затрагивает как развитые страны (где высокотехнологичное производство избавило население от необходимости много двигаться), так и развивающиеся (большому проценту населения которых приходится экономить на продуктах питания и потреблять больше быстрых углеводов – макарон, хлеба, картофеля, кукурузы).
Есть и другая тенденция последних лет. От метаболического синдрома стали страдать женщины репродуктивного возраста. С чем это связано, до конца неясно. Предположительно, могут негативно влиять оральные контрацептивы.
Только представьте: за последние 20 лет число людей с метаболическим синдромом в мире выросло более чем на 100 млн – то есть на треть.
Особенно остро стоит проблема детского ожирения, а с ним и детского МС. Ученые связывают рост детского ожирения с частым отказом от грудного вскармливания. Грудное вскармливание исключает раннее введение прикорма, которое может привести к нездоровому увеличению веса. Потребление белка и общего количества энергии выше у детей, вскармливаемых смесями, что приводит к увеличению массы тела у младенцев. Также кормление смесью несколько увеличивает уровень инсулина, что в свою очередь способствует отложению жира и раннему развитию жировых клеток (адипоцитов).
Таким образом, быстрая прибавка в весе в младенческом возрасте связана с ожирением в детстве. Грудное вскармливание может помочь «запрограммировать» человека на поддержание здорового веса во взрослом возрасте.
В чем причины?
Метаболический синдром имеет наследственную предрасположенность, которая, однако, в большей степени тоже объясняется внешними факторами. Люди, выросшие в одной семье, с большей вероятностью будут иметь схожие пищевые привычки и одинаковое отношение к спорту. Если на родительском столе бывает огромное количество быстрых углеводов и жиров и мало – овощей, зелени и фруктов, у ребенка с детства закладываются нездоровые отношения с едой. Так же и со спортом: ребенок с большей вероятностью будет активным, если у него активные родители.
Факторы риска
Осложнения
Диагностика метаболического синдрома
Диагностика МС состоит из визуального осмотра у врача и лабораторных и инструментальных исследований. В первую очередь врач оценивает абдоминальное ожирение. Но одного лишнего веса для постановки диагноза недостаточно. Оцениваются и другие симптомы и результаты анализов. Также важно обнаружить причину ожирения. Лишний вес может быть следствием эндокринных нарушений, гормональных сбоев или иных патологий.
Другой важный критерий при постановке диагноза – артериальное давление. При метаболическом синдроме оно обычно повышено.
ЭКГ – требуется, чтобы проверить работу сердца и вовремя обнаружить патологии, если заболевание уже запущенно.
Ангиография. Сложное исследование, которое позволяет оценить состояние сосудов. Проводится только по назначению врача.
Диагностика метаболического синдрома – непростая комплексная задача, которая осложняется разнообразием форм заболевания, его причинами и способами коррекции. Также это состояние опасно тем, что долгие годы человек не ощущает себя больным. Самочувствие начинает страдать, когда появляются значительные отклонения в работе организма и развиваются осложнения. Ни один человек не может ощутить повышенный уровень глюкозы в крови или нарушение обмена холестерина. О себе дают знать только уже очень серьезные проблемы, вызванные этими нарушениями, – например, гнойное воспаление пальцев ног или сердечный приступ.
Международная классификация болезней не выделяет метаболический синдром как отдельное заболевание, это целый комплекс заболеваний.
Ни один диагноз нельзя поставить самостоятельно, но любое отклонение в результатах исследований – повод не откладывать поход к врачу.
Лечение
В более запущенных формах может потребоваться применение препаратов, снижающих инсулинорезистентность, и лечащих артериальную гипертонию.
Что такое метаболический синдром? Причины возникновения, диагностику и методы лечения разберем в статье доктора Чернышев А. В., кардиолога со стажем в 32 года.
Определение болезни. Причины заболевания
Метаболический синдром (синдром Reaven) представляет собой симптомокомплекс, сочетающий в себе абдоминальное ожирение, инсулинорезистентность, гипергликемию (повышенное содержание глюкозы в крови), дислипидемию и артериальную гипертензию. Все эти нарушения связаны в одну патогенетическую цепь. Кроме того, такой синдром часто сочетается с гиперурикемией (избытком мочевой кислоты в крови), нарушением гемостаза (свёртываемости крови), субклиническим воспалением, синдромом обструктивного апноэ-гипопноэ сна (остановкой дыхания во сне). [4]
Метаболический синдром – хроническое, распространённое (до 35% в российской популяции), полиэтиологическое заболевание (возникающее по многим причинам), в котором главная роль принадлежит поведенческим факторам (гиподинамия, нерациональное питание, стресс). Имеет значение также наследственная предрасположенность к артериальной гипертензии, атеросклероззависимым заболеваниям и сахарному диабету второго типа. [5]
Практикующим врачам важно выделять группу риска метаболического синдрома. К данной группе относятся пациенты с начальными признаками заболевания и его осложнениями: артериальная гипертензия, углеводные изменения, ожирение и повышенное питание, ишемическая болезнь сердца, атеросклеротические заболевания периферических и мозговых артерий, нарушение пуринового обмена, жировая болезнь печени; синдром поликистозных яичников; постменопаузальный период у женщин и эректильная дисфункция у мужчин; гиподинамия, злоупотребление алкоголем, табакокурение, наследственная отягощенность по сердечно-сосудистым и обменным заболеваниям. [3] [7]
Симптомы метаболического синдрома
Клинические проявления метаболического синдрома соответствуют симптомам его составляющих:
Если изменения составляющих синдрома Reaven носят субклинический характер (что встречается довольно часто), то и течение заболевания носит асимптомный характер.
Патогенез метаболического синдрома
Инсулинорезистентность — первопричина развития метаболического синдрома. Представляет собой нарушение утилизации глюкозы в органах-мишенях (поперечнополосатой мускулатуре, липоцитах и печени), связанное с дисфункцией инсулина. Инсулинорезистентность уменьшает усвоение и поступление в клетки скелетной мускулатуры глюкозы; стимулирует липолиз и гликогенолиз, что приводит к липидным и углеводным патологическим изменениям. Кроме того, инсулинорезистентность усиливает секрецию инсулина, в результате чего возникает компенсаторная гиперинсулинемия и активация эндокринных систем (симпатоадреналовой, ренин-ангиотензин-альдостероновой) с формированием артериальной гипертензии, дальнейшим нарушением метаболических процессов, гиперкоагуляции, субклинического воспаления, дисфункции эндотелия и атерогенеза. Эти изменения, в свою очередь, способствуют усилению инсулинорезистентности, стимулируя патогенетический «порочный круг».
Классификация и стадии развития метаболического синдрома
Чёткой классификации и стадийности метаболического синдрома не существует. Его деление некоторыми авторами на полный, включающий все составляющие синдрома, и неполный представляется необоснованным. Несмотря на это, выраженность симптомов, количество компонентов синдрома Reaven и наличие осложнений оказывают влияние на стратификацию риска и выбор тактики лечения у конкретного пациента. Для этого следует учитывать:
В зависимости от индекса массы тела (ИМТ), который рассчитывается делением веса (кг) на рост (м 2 ), классифицируются следующие типы массы тела (МТ):
Второй тип ожирения является более патогенным в плане риска возникновения сердечно-сосудистых заболеваний и сахарного диабета. Это связано с ожирением внутренних органов, в том числе печени (висцеральное ожирение, неалкогольная жировая болезнь печени), снижением сатурации крови кислородом из-за перехода дыхания на грудной, поверхностный тип и эндокринной активностью висцеральной жировой ткани с патологическим изменением выработки адипокинов (лептин, грелин, адипонектин). Выявлена чёткая корреляция между увеличением абдоминальной жировой ткани и индекса массы тела с риском сопутствующих заболеваний. Считается, что риски начинают нарастать при увеличении окружности талии (ОТ) >80 см у женщин и 94 см у мужчин, а при ОТ >88 см и 102 см соответственно риск возрастает значительно.
Центральным патологическим звеном метаболического синдрома является изменение углеводного обмена. Концентрацию глюкозы оценивают в капиллярной крови (норма 1
жен. >1,2
Осложнения метаболического синдрома
Диагностика метаболического синдрома
Для диагностики метаболического синдрома необходимо выявить у пациента основной признак — абдоминальное ожирение по измерению ОТ (>80 см у женщин и >94 см у мужчин) и хотя бы два дополнительных критерия, которые включают в себя:
В клинических условиях нужно дифференцировать метаболический синдром от механического сочетания факторов риска, например артериальной гипертензии, избыточной массы тела без признаков абдоминального ожирения и повышения уровня ОХ крови, что встречается довольно часто (до 30%). В сомнительных случаях рекомендовано дополнительное определение инсулинорезистентности по следующим методикам:
Лечение метаболического синдрома
Лечение метаболического синдрома следует разделить на немедикаментозное и медикаментозное.
Медикаментозное лечение метаболического синдрома, в зависимости от наличия тех или иных его компонентов, может включать гиполипидемические, антигипертензивные препараты, медикаменты для снижения инсулинорезистентности, постпрандиальной гипергликемии и веса.
Основными препаратами, которые используют при лечении артериальной гипертензии у больных синдромом Reaven и сахарным диабетом, являются ингибиторы ангиотензинпревращающего фермента, сартаны и агонисты имидазолиновых рецепторов. Однако для достижения целевого уровня артериального давления часто необходимо сочетание различных классов медикаментов, таких как пролонгированных блокаторов медленных кальциевых каналов, высокоселективных бета-адреноблокаторов и тиазидоподобных диуретиков (индапамид) в сочетании с медикаментами первой линии. [10]
При неэффективности монотерапии статинами целесообразно присоединение эзетрола в дозе 10 мг/сут, который препятствует всасыванию ОХ в кишечнике и может усиливать снижение ХС-ЛПНП на 15-20%.
Фибраты — ещё один класс липидснижающих препаратов. Они расщепляют богатые триглицеридами жировые частицы, снижают синтез свободных жирных кислот и повышают ХС-ЛПВП путём увеличения распада ЛНП. Это приводит к значительному уменьшению триглицеридов (до 50%), ХС-ЛПНП (до 20%) и увеличению ХС-ЛПВП (до 30%). Фибраты также имеют плейотропные эффекты: снижают концентрацию мочевой кислоты, фибриногена и улучшают инсулиночувствительность, однако их положительное влияние на прогноз пациентов не доказано. Наиболее эффективный и безопасный препарат этой группы — фенофибрат 145 мг/сут.
Для снижения инсулинорезистентности препаратом выбора является метформин, который обладает доказанным положительным эффектом на тканевую инсулинорезистентность через усиление поглощения глюкозы тканями-мишенями. Метформин уменьшает скорость всасывания углеводов в тонкой кишке, оказывает периферическое анорексигенное действие, уменьшает продукцию глюкозы печенью, улучшает транспорт глюкозы внутри клеток. Положительное воздействие метформина (1500-3000 мг/сутки) на конечные точки обусловлено снижением инсулинорезистентности, системными метаболическими эффектами (снижение веса, липидных нарушений, факторов свёртываемости крови и т.д.). [9]
При наличии у пациента с синдромом Reaven сахарного диабета второго типа могут применяться современные классы сахароснижающих препаратов, такие как аналог глюкагоноподобного пептида-1, ингибитор дипептидилпептидазы-4 и ингибитор натрийзависимого переносчика глюкозы второго типа. Представитель последнего класса эмпаглифлозин (Джардинс) в исследовании EMPA-REG OUTCOME (2016 год) снизил сердечно-сосудистую смертность у больных сахарным диабетом второго типа на 36%.
Медикаментозная коррекция морбидного ожирения показана, если немедикаментозное лечение не приводит к снижению массы тела более чем на 5% от исходного. Препараты для лечения ожирения делятся на аноретики центрального действия (сибутрамин), и средства, воздействующие на желудочно-кишечный тракт, например орлистат (Ксеникал).
Препарат для снижения аппетита сибутрамин в меньшей степени воздействует на дофаминовые и холинергические процессы, но уменьшает потребление жиров и углеводов, что приводит к похудению и улучшает жировой и углеводный метаболизм. Артериальное давление и частота сердечных сокращений при этом повышается только на 5%.
Орлистат является ингибитором желудочной и панкреатической липаз, вследствие чего треть пищевых триглицеридов не всасывается и снижается их концентрация в крови, что приводит к уменьшению калоража пищи и веса. Кроме того, снижается артериальное давление, уровень глюкозы и инсулинорезистентности.
В медицинской практике лечение метаболического синдрома зависит от наличия и выраженности его компонентов. В таблице ниже показана тактика подбора терапии при вариантах синдрома Reaven, которые встречаются наиболее часто.
Метаболизм кишечных газов и его роль в возникновении гастроинтестинальных симптомов
Резюме. Патофизиологические механизмы нарушения метаболизма кишечных газов и их значение в возникновении гастроинтестинальных симптомов все еще дискутабельны. Состав газовой смеси отличается в различных отделах желудочно-кишечного тракта. Основным источником газовой смеси желудка считается воздух, который попадает при глотании. Газовый состав кишечника в значительной степени определяется физиологией микрофлоры, заселяющей его. Характер питания рассматривается как фактор, в значительной степени определяющий газообразование. Результаты ряда исследований свидетельствуют о различии микробного состава у здоровых добровольцев и пациентов с функциональными заболеваниями кишечника. Дальнейшее изучение механизмов газообразования в кишечнике позволит более эффективно воздействовать на основные патогенетические механизмы заболевания, приводящие к возникновению симптомов, связанных с газообразованием.
Введение
Метаболизм кишечных газов представляет собой сложный и строго регулируемый процесс, включающий продукцию, потребление, выделение и утилизацию газа различными отделами кишечника. Несмотря на то что интерес к этой гастроэнтерологической проблеме постоянно возрастает, патофизиологические механизмы нарушения метаболизма кишечных газов и их значение в возникновении гастроинтестинальных симптомов все еще дискутабельны.
На сегодняшний день в англоязычной литературе все чаще упоминается термин «симптомы, связанные с газами» (gas-related symptoms). Это понятие подразумевает наличие у пациента неспецифических жалоб, возникающих вследствие избытка полостных газов в кишечнике (Chang L. et al., 2001). К таким симптомам можно отнести вздутие живота, флатуленцию (выделение газов), отрыжку воздухом, ощущение растяжения живота и абдоминальный дискомфорт. Эти симптомы продолжают оставаться наиболее частыми проявлениями функциональных заболеваний кишечника, а также некоторых органических поражений желудочно-кишечного тракта (ЖКТ). Дальнейшее изучение физиологии и патофизиологии газообразования в кишечнике позволит приблизиться к пониманию механизмов возникновения таких симптомов, что даст возможность более эффективно воздействовать на основные патогенетические механизмы заболевания.
Механизмы образования кишечных газов
Состав газовой смеси отличается в различных отделах ЖКТ. Основным источником газовой смеси желудка считается воздух, который попадает при заглатывании как во время приема пищи, так и отдельно (Azpiroz F. et al., 2007).
Что касается газового состава кишечника, то он в значительной степени определяется физиологией микрофлоры, заселяющей тот или иной сегмент кишечника. Процессы бактериального гидролиза пищевых ингредиентов и образования газов наиболее интенсивно протекают в толстой кишке, поскольку в норме именно там определяется наибольшее количество микроорганизмов (Gasbarrini A. et al., 2007). Газовая смесь кишечника на более чем 99% состоит из 5 газов, не обладающих запахом — азота, кислорода, углекислого газа, водорода и метана, содержание которых варьирует в широких пределах (таблица) (Lembo T. et al., 1999).
| Кишечный газ | Нижняя граница | Верхняя граница |
|---|---|---|
| Азот | 11 | 92 |
| Кислород | 0 | 11 |
| Углекислый газ | 3 | 54 |
| Водород | 0 | 86 |
| Метан | 0 | 56 |
Другие газы, обладающие запахом, такие как аммиак, индол, скатол, летучие амины (путресцин, кадаверин) и короткоцепочечные жирные кислоты присутствуют только в следовых количествах и составляют не более 1% общей газовой смеси кишечника (Hahn B. et al., 1998; Lembo T. et al., 1999). Свободные индол и скатол образуются в кишечнике вследствие бактериальной ферментации триптофана. Часть индола всасывается в кровь и метаболизируется печенью с образованием индоксила и индоксил сульфата. Последний выделяется с мочой в виде калиевой соли, которая получила название «индикан» (Губський Ю.І., 2000). Аммиак также образуется из аминокислот под воздействием ферментов кишечной микрофлоры в результате дезаминирования. Путресцин и кадаверин образуются микроогранизмами путем декарбоксилирования соответственно орнитина и лизина. Короткоцепочечные жирные кислоты (уксусная, пропионовая, масляная, изовалериановая и др.) являются продуктом деградации полисахаридов (Binder H.J., 2010).
Долгое время стереотипно считалось, что именно такие продукты распада аминокислот, как индол и скатол являются первичными компонентами газов с неприятным запахом. Однако в последних исследованиях установлено, что за характерный запах человеческих фекалий ответственны компоненты, в состав которых входит сера — сульфид водорода, диметилсульфид и метантиол (Houghton L.A. et al., 2006).
Еще одним механизмом поступления газов в просвет кишечника может быть их диффузия из кровяного русла. Поскольку образование водорода, углекислого газа и метана может приводить к снижению парциального давления азота в просвете до величин, значительно меньших, чем в крови, то этот газ может диффундировать из сосудистого русла в просвет кишечника (Gasbarrini A. et al., 2009).
Утилизация газов ЖКТ осуществляется за счет таких процессов, как отрыжка, выделение естественным путем, бактериальное потребление и выделение с выдыхаемым воздухом. Последние два механизма требуют особого внимания. Некоторые бактерии не выделяют, а наоборот, потребляют газы, ранее образованные в кишечнике. Так, архебактерии (Methanobrevibacter smithii, Methanosphaera stadtmanae и другие Methanobacteriales) в процессе анаэробного дыхания окисляют молекулярный водород с образованием метана, сульфатредуцирующие бактерии родов Desulfomaculum, Desulfovibrio, Desulfomonas используют водород из просвета кишечника для формирования конечного продукта энергетического обмена — сульфида водорода. Ацетогенные бактерии (некоторые виды клостридий) могут потреблять водород при восстановлении диоксида углерода с формированием уксусной кислоты (Готтшалк Г., 1982; Климнюк С.І. та ін., 2004). Бактерии рода Campylobacter (в том числе Helicobacter pylori) содержат мембранные гидрогеназы, что позволяет им использовать молекулярный водород в дыхательной цепи для аккумуляции энергии (Olson J.W., Maier R.J., 2002; Maier R.J., 2005).
Роль кишечных газов в формировании гастроинтестинальных симптомов
Механизмы, лежащие в основе вздутия и растяжения до сих пор полностью не изучены, однако в настоящее время предполагается, что в патогенезе формирования данных симптомов вовлечено множество факторов, среди которых повышенное газообразование, уменьшение потребления внутрипросветного газа, нарушение моторики ЖКТ и выделения газа, висцеральная гиперчувствительность, нарушение мышечной активности стенки живота. Сейчас хорошо известна зависимость газообразования от характера питания. Так, даже у здоровых лиц некоторые фрукты и овощи (в частности бобовые и фасоль), пшеничная мука, овес, картофель и зерновые, содержащие олигосахариды, не перевариваются ферментами в верхних отделах ЖКТ и, таким образом, становятся доступным субстратом бактериальной ферментации (Gasbarrini A. et al., 2009), что может приводить к вздутию живота.
Повышенное потребление продуктов с высоким содержанием так называемых пищевых волокон (растительная клетчатка, пектин, рафиноза) также может стать источником повышенного газообразования даже у здоровых лиц.
Что качается взаимосвязи между избыточным содержанием кишечного газа и вздутием живота у пациентов с функциональными заболеваниями кишечника, то этот вопрос до сих пор остается открытым. Использование техники отмывания кишечных газов продемонстрировало, что объем газов у пациентов с синдромом раздраженной кишки (СРК) сходный с таковым у здоровых лиц (Caldarella M.P. et al., 2002). В то же время некоторые исследования, основанные на количественном определении кишечных газов при помощи обычной рентгенографии, доказали повышенное содержание газов у пациентов с СРК по сравнению с контролем (Koide A. et al., 2000). В ряде работ продемонстрировано значительное повышение экскреции водорода и метана выдыхаемым воздухом у пациентов с СРК по сравнению с контролем (King T.S. et al., 1998). Хотя в других исследованиях указывается на иные возможные причины возникновения вздутия живота у пациентов с функциональными заболеваниями кишечника, как то: нарушение распределения газов в кишечнике без изменения их объема (Harder H. et al., 2003) и смещение диафрагмы (Accarino A. et al., 2009).
Такая неоднозначность мнений побудила нас к формированию собственного виденья представленной проблемы. Так, при обследовании 51 пациента с диагнозом СРК и диареей (Римские критерии ІІІ) у 21 из них установлен высокий уровень водорода в выдыхаемом воздухе натощак, причем выраженность вздутия живота у таких пациентов имела сильную корреляционную связь с уровнем экскреции водорода (r=0,81; p Коментарі