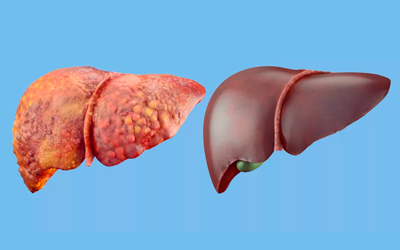
Как восстановить организм после длительного запоя
Клиника «Алко Центр» продолжает цикл публикаций на тему алкоголизма, его лечения и борьбы с зависимостью.
Все случаи уникальны, рекомендуем позвонить по телефону +7(495)773-03-43 и получить консультацию врача.
Продолжительное употребление алкогольных напитков приводит к сильной интоксикации, из-за которой происходят серьезные нарушения в работе внутренних органов. Также появляется похмельный синдром. Некоторым хватает и пары часов, чтобы прийти в чувство, н это касается случаев, когда человек просто перебрал со спиртным. А вот запойным алкоголикам понадобится больше времени и комплексный подход к проблеме.
В последнем случае лучше обратиться к наркологу, он сделает выход из запоя менее болезненным.
Нужна неотложная помощь – обращайтесь в «Алко-Центр»
Звоните по телефону горячей линии +7 (495) 773-03-43 и наши врачи проведут курс экстренной помощи при интоксикации организма продуктами распада алкоголя и наркотических веществ.
Вывод из запоя
Экстренная процедура детоксикации организма
Кодирование
Срочная блокировка тяги к алкогольным напиткам
Реабилитация
Комплексная реабилитация, дающая 100% результат
Что делать после длительного запоя: восстановление
С последствиями запоя в домашних условиях справиться можно, но только в том, если такое состояние длилось не больше недели. В противном случае потребуется срочная госпитализация в наркологическую клинику, где больному окажут экстренную помощь и поставят капельницу.
Методы восстановления организма зависят от:
Первый шаг на пути к вытрезвлению – это детоксикация, то есть очищение организма с помощью капельницы. Внутривенное введение лекарственных средств позволяет быстрее вывести из крови токсины, а также продукты распада этилового спирта.
Для достижения большего эффекта рекомендуется проведение процедуры в условиях стационара. Тогда нарколог подберет состав капельницы с учетом результатов анализов, а также физиологических особенностей пациента. К тому же это снижает риск развития осложнений.
Очищающие растворы подбираются персонально для каждого больного. Это позволяет максимально быстро устранить негативные последствия после продолжительного употребления алкогольных напитков.
Для детоксикации в домашних условиях назначается курс сорбентов, коррекция режима питания и обильное питье.
Мозг и нервная система
Скорость их восстановления зависит от факторов:
Из-за проблем со спиртным нарушается работа мозга и периферической нервной системы. Алкоголики сталкиваются с частичной или полной потерей памяти, рассеянностью, тремором конечностей.
Для приведения в норму функционирования этих органов алкоголикам назначаются ноотропы (Пирацетам, Ноотропил) в комплексе с препаратами, которые оказывают седативное действие (Глицин, Грандаксик). Дополнительно выписываются лекарства для улучшения кровообращения и укрепления сосудов.
Поможет справиться с последствиями пьянок и полноценный сон. Если он нарушен, то врач назначает сильнодействующие снотворные.
Сердечно-сосудистая система
Запои становятся причиной развития аритмии, резких скачков артериального давления, увеличения количества сокращений миокарда. Преодолеть это можно только при условии своевременного обращения к врачу-наркологу, поскольку самостоятельно справиться с подобной симптоматикой не получится. Это касается тех случаев, когда прерывание продолжительных пьянок вызывает различного рода депрессии и подавленное состояние.
Нормализация сердечно-сосудистой системы проводится с помощью таких лекарств:
Почки
Периодическое распитие спиртных напитков приводят к серьезным сбоям в функционировании почек. В результате этого возникают боль в пояснице, почечная недостаточность, в урине возникает осадок.
Схема лечения подбирается персонально исходя из запущенности состояния. Длится оно от двух до трех месяцев.
Поддержать результат поможет дробное питание, обильное питье, а также умеренная физическая активность.
Печень
Чтобы печень восстановилась и начала работать нормально следует придерживаться ряда рекомендаций:
Желудочно-кишечный тракт
Нормализовать функционирование желудочно-кишечного тракта поможет соблюдение рекомендаций:
Употребление кисломолочных продуктов в большом количестве, так как минимизируют негативное влияние этанола на организм и способствует его выведению. Пить больше жидкости: зеленые чаи, морсы, компоты, минеральная вода без газа.
При соблюдении этих мер вернуться к нормальному образу жизни получится быстрее. Если делать это под наблюдением врача-нарколога.
Питание после продолжительного запоя
Первые пару дней лучше вовсе придерживаться голодовки. После можно начинать вводить постные блюда: вареные овощи, супы, каши, куриный бульон и кисломолочные продукты.
Во время выхода из запоя у алкоголиков наблюдаются такие симптомы похмелья, как:
Чтобы улучшить самочувствие, обратитесь за помощью в наркологическую клинику. А вот самолечением заниматься не стоит, поскольку это может быть чревато тяжелыми и необратимыми последствиями. Лучше следовать курсу лечения, который назначил врач и чаще гулять на свежем воздухе.
Как долго длится восстановление после запоя
Срок лечения алкоголика зависит от:
Если терапия была подобрана верно и больной соблюдает все рекомендации врача, то период восстановления может длится около 30 дней.
Что делать с похмельем
С похмельем помогут справиться и народные методы. После продолжительных пьянок нужен комплексный подход, а поэтому можно комбинировать методы терапии. Так, при развитии похмельного синдрома помогут:
Если не знаете, что делать после длительного запоя, то стоит сразу обратиться к наркологу, а не пытаться лечиться по советам из Интернета.
Алкогольная интоксикация печени
Содержание:
Воздействие алкоголя на печень
После попадания в желудок, этанол проникает в кровоток, затем в гепатобилиарную систему, где происходит распад и нейтрализация. Для переработки синтезируется масса ферментов, которые преобразуют спирт в простые соединения — воду и углекислый газ. Промежуточным продуктом распада является ацетальдегид — токсичное вещество. Печень здорового человека быстро выводит продукты метаболизма. Изношенный орган больного алкоголизмом при систематическом употреблении спиртного не справляется, замедляя вывод метаболитов и задерживая часть токсинов в тканях. Следствие — наступление ацетальдегидной интоксикации, требующей применения инфузионных вливаний детоксицирующих препаратов.
Алкогольное отравление печени может появиться не только у закоренелых алкоголиков. Любой человек, принявший спиртное в большом количестве, подвержен токсическому влиянию. К группе риска относят: 
По статистике, более чем 40% людей, после распития спиртного, страдают интоксикацией. У 78% зависимых, развивается цирроз, у 14% гепатоцеллюлярная карцинома или рак печени.
Стадии и симптомы
Отравление самой крупной железы опасно, так как вызывает нарушение жизнеобеспечения организма. Тяжелее всего воспринимаются крупные дозы алкоголя. Выделяют три этапа опьянения в зависимости от количества выпитого и соответствующие им степени интоксикации.
Содержание спирта свыше 5 промилле — смертельное отравление, необходима срочная медицинская помощь, без которой через 2-3 часа наступает летальный исход.
Симптомы, на которые следует обратить внимание: 
При тяжелых поражениях, моча приобретает темно-коричневый цвет, так как в нее попадают кровяные клетки.
Алкогольный токсикоз печени — серьезное отравление, которое невозможно вылечить без помощи врача, необходимо обращение в специализированную клинику. Чем раньше пациент получит помощь, тем меньше риск необратимых последствий.
Распространенные последствия
Регулярное потребление спиртосодержащих напитков, независимо от крепости, наносит вред всему организму. Самое страшное последствие — хроническое отравление. Распространенные осложнения потребления алкоголя.
Диагностика и методы терапии
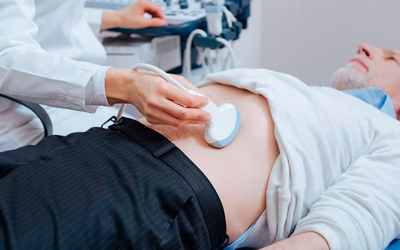
После сбора анамнеза, выяснения длительности периода употребления и проведения лабораторных анализов, УЗИ брюшной полости, допплерографии, врач прописывает назначение. При необходимости, дополнительно назначают МРТ, биопсию тканей. Прописывают комплексную терапию, сочетающую выведение токсических веществ, устранение сопутствующих патологий, возобновление функциональности гепатобилиарной системы.
Медикаментозная терапия включает мероприятия по дезинтоксикации, предусматривает прием гепатопротекторов, антиоксидантов, мультивитаминных комплексов, седативных препаратов. Также больным назначают диету со сбалансированным содержанием белков и микроэлементов. Длительность курса напрямую зависит от степени поражения органа и наличия сопутствующих заболеваний.
Обязательное условие — полный отказ от спиртных напитков в любом виде, включая спиртосодержащие лекарственные средства.
Методы детоксикации, медикаментозного лечения в специализированном медицинском центре помогают вывести токсины из организма и нормализовать работу гепатобилиарной системы. После выписки из учреждения, человек должен воздержаться даже от слабоалкогольных напитков, принимать прописанные врачом препараты для полного выздоровления и восстановления гепатоцитов.
Алкогольная болезнь печени
Актуальность проблемы

Что такое алкогольная болезнь печени?
Алкогольная болезнь печени – это совокупность поражений печени, развивающихся на фоне злоупотребления спиртными напитками, включающая накопление жира в гепатоцитах (стеатоз, жировой гепатоз), воспаление (гепатит) и цирроз.
Точной статистики по заболеваемости в России нет, однако есть данные, что факторы риска имеют около 40 % населения.
Причины развития
Основная причина развития АБП – злоупотребление спиртным. Опасными считаются дозы, превышающие 30 мл водки (коньяка, виски), 150 мл вина или 250 мл пива в день для женщин и 60 мл водки (коньяка, виски), 300 мл вина или 500 мл пива в день – для мужчин. Факт злоупотребления несложно определить с помощью специального опросника (CAGE). Об этом свидетельствуют не менее двух положительных ответов на следующие вопросы:
Дополнительными факторами риска поражения печени являются:
Механизмы поражения печени
Ключевую роль в поражении печени алкоголем играет этанол и его более токсичное производное – ацетальдегид. Можно выделить несколько механизмов поражения.
Следствием воспаления является разрушение гепатоцитов (цитолиз), их гибель (некроз) и разрастание соединительной ткани (фиброз). Прогрессирующий фиброз приводит к нарушению нормального долькового строения печени – циррозу, а в дальнейшем к первичному раку – гепатоцеллюлярной карциноме.
Симптомы болезни
АБП может протекать бессимптомно. Вместе с тем, симптомы алкогольного поражения печени могут быть неспецифическими. К ним относятся такие жалобы, как тяжесть или боль в правом подреберье, вздутие живота, нарушение стула, тошнота и др.
Кроме печени в патологический процесс могут вовлекаться и другие органы и системы. В частности, может отмечаться атрофия мышц плечевого пояса, нарушение чувствительности в конечностях (полинейропатия), заболевания сердца (кардиомиопатия), поджелудочной железы (панкреатит).
Диагностика заболевания
Лабораторные методы
Лабораторными симптомами прежде всего являются
Ультразвуковое исследование
При ультразвуковом исследовании (УЗИ) можно обнаружить увеличение размеров печени (гепатомегалию), ее неоднородность и повышенную эхогенность. В качестве методов визуализации, кроме УЗИ, используются компьютерная томография (КТ) и магнитно-резонансная томография (МРТ).
Биопсия
Диагноз и стадия поражения могут быть точно определены при биопсии. Неинвазивной альтернативой биопсии является эластография. Она представляет собой свовремный метод диагностики, позволяющий оценить эластичность ткани органа с помощью ультразвукового датчика.
Профилактика болезни
Основным методом профилактики АБП является употребление спиртного в дозах, не превышающих безопасные, или полный отказ от него.
В случае, когда алкогольная болезнь печени уже имеет место, требуется лечение. В целях профилактики прогрессирования воспаления и фиброза, развития цирроза и рака, лечение необходимо начинать на самых ранних стадиях.
Методы лечения АБП
Можно выделить медикаментозные и немедикаментозные подходы к терапии.
Медикаментозные
Немедикаментозное лечение требует полного отказа от алкоголя.
Медикаментозные
Лекарство для лечения алкогольной болезни печени должно оказывать антиоксидантное действие, подавлять воспаление и препятствовать прогрессированию фиброза. Таким препаратом является Фосфоглив*, продемонстрировавший все эти эффекты в клинических исследованиях. Его следует принимать по 2 капсулы 3 раза в день во время еды, не разжевывая, запивая небольшим количеством жидкости. Продолжительность курса обычно составляет 3 месяца.
При подозрении на развитие болезни печени следует обратиться к врачу.
Eric S Orman, Gemma Odena and Ramon Bataller. Alcoholic liver disease: Pathogenesis, management, and novel targets for therapy // Journal of Gastroenterology and Hepatology. 2013; 28 (Suppl. 1): 77–84 3
Mukamal K.J. et al. Roles of drinking pattern and type of alcohol consumed in coronary heart disease in men // N Engl J Med. 2003; 348: 2: 109-118. 4
R. S. O’Shea, S. Dasarathy, A. J. McCullough et al. Alcoholic Liver Disease. AASLD Practice guidelines // Hepatology. 2010; 51 (1): 307-328. 5
The Physician’s Guide to Helping Patients with Alcohol Problems. Rockville: National Institute on Alcohol Abuse and Alcoholism (NIAAA) // NIH publication. 1995: 95-3769. 6
Фосфоглив* —
1. Настоящая информация основана на исследованиях, проводимых ООО «Ипсос Комкон», и действительна по состоянию на декабрь 2016 года
2. Распоряжение правительства РФ от 28 декабря 2016 г. № 2885-р «Об утверждении перечней жизненно необходимых и важнейших лекарственных препаратов для медицинского применения на 2017 год»
3. Ивашкин В.Т., Бакулин И.Г., Богомолов П.О., Мациевич М.В. и др., 2017 г.
4. Бакулин И.Г., Бохан Н.А., Богомолов П.О., Гейвандова Н.И. и др., 2017 г.
5. Буеверов А.О., 2014 г.
6. Филимонкова Н.Н., Воробьева Ю.В., Топычканова Е.П., 2013 г.
7. Новикова Т.И., Новиков В.С., 2011 г.
8. Приказ МЗ РФ от 10.11.2011 г. № 1340н «Об утверждении Перечня лекарственных средств, отпускаемых по рецептам врача (фельдшера) при оказании дополнительной бесплатной медицинской помощи отдельным категориям граждан, имеющим право на получение государственной социальной помощи»
9. Приказ Минздрава РФ от 09.11.2012 N 772н «Об утверждении стандарта специализированной медицинской помощи при других заболеваниях печени»
10. Инструкция по медицинскому применению
11. И.Г. Никитин, И.Е. Байкова, В.М. Волынкина и соавторы, 2009г.
Как помочь печени с помощью диеты?
Роль печени в работе организма трудно переоценить. Она участвует в пищеварении, детоксикации организма и других процессах. Это орган, который способен самостоятельно восстанавливаться, но для поддержания его здоровья важно включить в рацион определенные продукты. Врач-иммунолог, специалист по питанию Алена Парецкая расскажет о 12 самых полезных продуктах, которые нужно включать в рацион.
№1. Кофе
Кофе – спорный продукт. В исследовании, опубликованном в 2013 году, было доказано, что ежедневное употребление кофе снижает риск развития хронических заболеваний печени и их обострений. В первую очередь, речь идет о жировой болезни печени и онкопатологиях.
В другом исследовании ученые обозначили механизм этого положительного влияния на печень: основной механизм – это влияние на ферменты печени и предотвращение накопления жира в ее тканях. Еще один механизм – действие антиоксидантов на печень, укрепляющих ее защитные свойства и противостоящие онкопатологиям. Но важно отметить, что речь идет о регулярном, но умеренном употреблении кофе.
№2. Овсянка
Это источник полезной клетчатки, которая участвует в пищеварении и поддерживает его. Известно, что клетчатка овсянки полезна для печени, ведь в ней содержатся бета-глюканы.
Одно из исследований показало, что эти вещества активируют иммунную систему, подавляют воспаление, а также помогают контролировать диабет и предотвращают ожирение.
В другом исследовании, проведенном на грызунах, отмечается, что бета-глюканы помогает уменьшить количество жира, которые хранятся в печени. Однако чтобы говорить о пользе для человека, необходимы дополнительные клинические исследования.
Добавьте в рацион овсяные хлопья, которые требуют варки. Продукты быстрого приготовления, с содержанием сахара и прочих ингредиентов не приносят особой пользы для организма.
№3. Зеленый чай
Одно из исследований предположило, что зеленый чай снижает риск рака печени. Однако исследование было проведено в малочисленной группе участников. Поэтому для однозначных заверений и утверждений, необходимы дополнительные исследования.
№4. Чеснок
Чеснок стимулирует работу печени. Ряд исследований, проведенных в 2016 году, показывает, что чеснок помогает снизить массу тела и предотвратить набор лишнего веса и ожирение, что, в свою очередь, можно рассматривать как предрасполагающий фактор для развития жировой болезни печени.
№5. Ягоды
Черника, малина, клюква содержат большое количество антиоксидантов – полифенолов, защищающих печень от повреждений. Учитывая большое содержание витаминов, минералов и прочих веществ известна польза ягод для поддержания работы иммунитета.
№6. Виноград
В винограде и его косточках содержатся антиоксиданты, которые положительным образом отражаются на здоровье и работе организма и печени в частности. Известно, что регулярное употребление винограда помогает контролировать воспалительные реакции и предотвращать повреждение печени.
Специалисты рекомендуют включать в рацион свежий виноград, а также качественный сок, который оказывается полезным.
№7. Грейпфрут
Это весьма полезный продукт, содержащий несколько групп антиоксидантов, которые помогают защищать печень от повреждений, стимулируя восстановление и регенерацию клеток.
Соединения, содержащиеся в этом фрукте, уменьшают накопление жира в печени, а также стимулируют работу ферментов, которые стимулируют похудение и снижают риск развития жировой болезни печени.
№8. Растительная пища
Все разнообразие овощей и фруктов можно рассматривать как полезную пищу для здоровья печени. В обзоре 2015 года был опубликован перечень растительных продуктов, полезных для печени:
№9. Жирные сорта рыбы
Жирный сорта рыбы – основной источник Омега-3 кислот, которые контролируют воспалительные реакции в организме и участвуют в обменных процессах. Эта группа жиров положительна для полноценной работы печени и профилактики многочисленных заболеваний. Их главная роль – накопление лишних жиров и поддержание нормального уровня ферментов в печени.
Согласно рекомендациям врачей, есть жирную рыбу нужно 2 и более раз в неделю. Для тех людей, которые по каким-либо причинам не могут включать в рацион жирные сорта рыбы, рекомендовано принимать добавки с рыбьим жиром.
№10. Орехи
Включение в рацион орехов – простой и действенный способ поддержать здоровье печени и защитить ее от многочисленных болезней. В их составе большое количество ненасыщенных жирных кислот, витаминов и антиоксидантов.
В рацион рекомендовано включать грецкие орехи, миндаль, которые помогут сохранить здоровье печени. Но стоит помнить, что чрезмерное употребление орехов может оказаться вредным, ведь они высококалорийны.
№11. Оливковое масло
Включение в рацион оливкового масла без термической обработки помогает снизить окислительный стресс и улучшить функцию печени. Объяснить такое положительное влияние можно большим содержанием ненасыщенных жирных кислот.
Какие продукты вредны для печени
Общие рекомендации специалистов однозначны – сбалансированное питание, содержащее все необходимые минералы, витамины и прочие вещества помогают поддерживать здоровье печени. Тем не менее есть продукты, которые могут негативно повлиять на работу печени и их необходимо ограничивать в рационе:
1. Жирное
В эту группу продуктов можно отнести: жареное, фастфуд, полуфабрикаты, снеки и прочие закуски.
2. Крахмалистые продукты
В эту группу можно отнести: хлеб, макаронные изделия, сладкая и сдобная выпечка.
3. Сахар
Чрезмерное употребление сладостей нагружает печень, поэтому целесообразно снизить эту нагрузку.
4. Соль
Это основной источник натрия и калия, которые необходимы для нормальной работы организма. Однако чрезмерное употребление соли также оказывается вредным. Консервы, копчености и соленья содержат большое количество соли.
5. Алкоголь
Пожалуй, это самый вредный продукт для печени. И каждому важно подумать об ограничении и умеренном употреблении алкоголя.
Печень – уникальный орган, отвечающий за множество обменных процессов и защитных реакций. Ее клетки способны к регенерации и восстановлению, однако хроническое патологическое воздействие приводит к болезням, со всеми вытекающими последствиями.
Поддержать здоровье печени, особенно при наличии факторов риска и предрасположенности к болезням можно путем составления правильного рациона.
Чем лечить печень после длительного приема алкоголя
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20%. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение алкогольной болезни печени (АБП) определяется в первую очередь паттерном употребления спиртных напитков. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет. Возможности терапии АБП ограничены. При гепатите тяжелого течения, наряду с коррекцией трофологического статуса, назначаются преднизолон и пентоксифиллин. Для лечения хронических форм АБП в настоящее время применяются средства для лечения алкогольной зависимости. Эффективность препаратов метаболического (гепатопротективного) действия ставится под сомнение, хотя в отдельных исследованиях получены обнадеживающие результаты.
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20%. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение алкогольной болезни печени (АБП) определяется в первую очередь паттерном употребления спиртных напитков. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет. Возможности терапии АБП ограничены. При гепатите тяжелого течения, наряду с коррекцией трофологического статуса, назначаются преднизолон и пентоксифиллин. Для лечения хронических форм АБП в настоящее время применяются средства для лечения алкогольной зависимости. Эффективность препаратов метаболического (гепатопротективного) действия ставится под сомнение, хотя в отдельных исследованиях получены обнадеживающие результаты.
Последствия злоупотребления алкоголем представляют собой общемировую проблему, включающую не только органную патологию, но также несчастные случаи и преступления, связанные с состоянием опьянения. Так, в Европе 11% летальных исходов у мужчин и 1,8% у женщин рассматриваются в ассоциации с алкоголизмом [1]. Если анализировать структуру поражений внутренних органов, то доминирующую позицию среди них занимает именно алкогольная болезнь печени (АБП), ведущая к развитию цирроза печени и гепатоцеллюлярной карциномы [2]. Несмотря на то, что в последние годы на пути изучения патогенеза поражения печени достигнуты серьезные успехи, лечение тяжелых форм АБП в определенной мере «законсервировалось», не давая основания говорить о революционном прорыве в ближайшем будущем. Тем не менее, определенные направления в терапии АБП можно расценивать как перспективные, причем это относится не только к методам, которые не вышли пока за рамки экспериментальных, но и к давно известным средствам, открывающим новые грани в процессе углубленного изучения.
Естественное течение АБП: от стеатоза к циррозу
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20% [3, 4]. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение АБП определяется в первую очередь паттерном употребления спиртных напитков: постоянным или перемежающимся типом пьянства; периодами запоев, сменяющихся абстиненцией; нарастанием или сокращением суточной дозы алкоголя Учитывая обстоятельство, что большинство пациентов обращаются за медицинской помощью на поздних стадиях, оптимальной моделью наблюдения служат больные после трансплантации печени [5].
Генетическая предрасположенность к АБП также служит предметом активного изучения. Недавние исследования выявили значимую корреляцию определенных аллельных вариантов адипонутрина (PNPLA3) и прогрессированием фиброгенеза [6, 7]. Более того, генетический полиморфизм адипонутрина ассоциирован и с развитием ГЦК [8]. В то же время попытки идентифицировать генетические маркеры предрасположенности к АБП, в том числе полиморфизм генов, участвующих в метаболизме этанола, пока не увенчались успехом [9].
В ретроспективном исследовании S. Naveau, включавшем более 2000 злоупотребляющих алкоголем пациентов, по данным биопсии печени у 34% выявлен цирроз, у 9% — активный гепатит, у 46% — стеатоз печени с наличием или отсутствием фиброза, а у 11% патологические изменения печени отсутствовали [10]. По данным T. Poynard, вероятность развития цирроза нарастает с возрастом, достигая при регулярном употреблении высоких доз алкоголя 50% к 61 году, причем у женщин сроки формирования цирроза короче [11]. Суммируя опубликованные результаты ретроспективных исследований, можно констатировать, что среди госпитализированных алкоголиков частота обнаружения цирроза составляет около 20% [2].
Стеатоз обычно предшествует образованию соединительной ткани, но влияние аккумуляции жира в печени на фиброгенез изучено недостаточно [2, 13, 14]. Долгосрочная выживаемость пациентов с алкогольным стеатозом в отсутствии воспаления и фиброза сопоставима с таковой у трезвенников. Если сравнивать течение неалкогольной жировой болезни печени (НАЖБП) и АБП, можно констатировать более высокие темпы прогрессирования последней. В течение 10 лет у больных алкогольным стеатозом значительно чаще развивается цирроз (21% vs. 1%) и наблюдаются летальные исходы (74% vs. 25%) [15]. Интересно, что у больных алкогольным циррозом повышен риск аутоиммунных заболеваний [16]. Можно предположить, что ацетальдегид, образующийся в разных тканях под действием алкогольдегидрогеназы, образует прочные комплексы с белками, выступающие в роли неоантигенов.
Цирроз печени рассматривается в качестве причины смерти 25% алкоголиков, занимая первое место среди летальных исходов [1, 2, 15]. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Это состояние проявляется желтухой, в тяжелых случаях энцефалопатией и гипокоагуляцией, и требует обязательного отражения в диагнозе, так как принципиально меняет прогноз и подходы к лечению.
Недавно завершенные исследования, основанные на биопсийном материале, убедительно продемонстрировали, что у подавляющего большинства пациентов с тяжелым алкогольным гепатитом имеется исходный цирроз или септальный фиброз печени [9, 18]. Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет [2].
В то время как ожирение является общепризнанным коморбидным фактором стеатоза, имеются также сведения о его влиянии на развитие алкогольного гепатита и фиброза печени. В качестве ключевых патогенетических факторов называются инсулинорезистентность и гипергликемия [19]. С другой стороны, небольшие дозы этанола способствуют замедлению прогрессирования неалкогольной жировой болезни печени [20].
Лечение АБП: акцент на абстиненцию
К вопросу о безопасной дозе алкоголя
Необходимость обсуждения лимита употребляемого алкоголя, превышение которого ведет к повреждению печени, в аспекте лечения АБП определяется тем, что соблюдение пациентом полной абстиненции является важной, но зачастую недостижимой целью. Так, в США 67–81% больных возобновляют прием алкоголя в течение одного года [21]. В последние годы дозу этанола часто измеряют в «дозах» (drinks), равных 10–14 г чистого этанола. «Доза» примерно соответствует бокалу пива, фужеру сухого вина или рюмке крепкого напитка. Показано, что прием ≤ 2 «доз» в день для мужчин и ≤ 1 «дозы» в день для женщин не ассоциировано с повышенной вероятностью развития органной патологии по сравнению с трезвенниками [2]. Другие исследования демонстрируют сходные результаты. Согласно метаанализу G. Corrao, употребление > 25 г этанола в день увеличивает относительный риск цирроза печени [22]. В итальянском исследовании Dionysos у лиц, ежедневно принимающих ≥ 30 г этанола, цирроз наблюдался в 2,2% случаев, тогда как у непьющих — в 0,08%. Риск цирроза экспоненциально возрастал по мере увеличения доз алкоголя, достигая 13,5% у употребляющих > 120 г в день [23].
Средства для лечения алкогольной зависимости
Ввиду того, что большинство пациентов нарушают предписанный режим абстиненции, в последние годы активно изучаются препараты, снижающие потребность в алкоголе: налтрексон, акампрозат, топирамат, баклофен и др. Наибольшее число исследований на сегодняшний день выполнено с агонистом баклофеном, продемонстрировавшим эффективность и безопасность при тяжелых формах АБП [24].
Метадоксин, зарегистрированный в ряде европейских стран для лечения алкогольной интоксикации, в нескольких небольших исследованиях значимое снижение употребления алкоголя, что сопровождалось редукцией биомаркеров АБП (трансаминазы, γ-глутамилтранспептидаза, средний объем эритроцитов) [25]. Сходные результаты получены в исследовании внутривенной формы глицирризиновой кислоты. Интересно, что соблюдение предписанного режима абстиненции коррелировало со снижением сывороточного уровня фактора некроза опухоли-α [26].
Коррекция трофологического статуса
Нутритивная поддержка наиболее важна для больных тяжелым алкогольным гепатитом, хотя и при других формах АБП у большинства пациентов наблюдаются те или иные формы нарушения трофологического статуса [2]. В исследовании С. Mendenhall et al. показано, что у пациентов, самостоятельно принимающих пищу с энергетической ценностью более 3000 ккал в сутки, отмечалась нулевая летальность, в то время как из потреблявших менее 1000 ккал в сутки умерло более 80% [27]. Несмотря на безусловную ценность этих данных, нельзя игнорировать высокую вероятность более тяжелого течения гепатита у больных второй группы, к типичным проявлениям которого относится анорексия [28].
Общие рекомендации по коррекции трофологического статуса у больных тяжелым алкогольным гепатитом предусматривают суточное потребление 1500–2500 ккал. Диета должна быть сбалансирована по содержанию основных нутриентов и витаминов, ограничение белка показано лишь в случаях его индивидуальной непереносимости. Следует помнить о преимуществе перорального приема пищи над зондовым и парентеральным; последнее назначается только при невозможности физиологического питания (повторная рвота, нарушения сознания).
Как отмечалось выше, избыточная масса тела и ожирение тоже способствуют прогрессированию повреждения печени ввиду общности ряда патогенетических звеньев алкогольного и неалкогольного стеатогепатита [10, 29], что необходимо учитывать при разработке программы лечения.
Кортикостероиды применяются для лечения тяжелого алкогольного гепатита на протяжении более 40 лет. Наиболее хорошо изучена схема с пероральным преднизолоном 40 мг в сутки в течение одного месяца, с одномоментной отменой или постепенным снижением дозы. Хотя многочисленные исследования весьма разнородны по дизайну и отбору пациентов, метаанализ показал достоверное повышение краткосрочной выживаемости по сравнению с больными, не получавшими преднизолон [14]. Оценка эффективности терапии обычно осуществляется с помощью индекса Лилле (Lille), который рассчитывается через семь дней лечения по формуле:
R = 3,19 — 0,101 (возраст в годах) + 0,147 (альбумин в день поступления, ) + 0,0165 (сывороточный билирубин, мкмоль) + 0,206 (наличие почечной недостаточности — 0 или 1) + 0,0065 (сывороточный билирубин в день поступления, мкмоль) + 0,0096 (протромбиновое время, с)
Индекс Лилле = Exp ® /[1 +Exp ® ]
Значение индекса Лилле > 0,45 указывает на неэффективность преднизолона и 75%-ю вероятность летального исхода в течение шести месяцев. С почти пятикратным ростом летальности сопряжено также отсутствие снижения уровня сывороточного билирубина, по меньшей мере, на 25% за аналогичный срок стероидной терапии [30]. У этой когорты больных дальнейшее применение преднизолона нецелесообразно, с учетом повышения риска инфекционных осложнений, особенно легочного аспергиллеза [31]. В упомянутом метаанализе выделены три группы пациентов в зависимости от реакции на преднизолон: с полным, частичным и нулевым ответом. Краткосрочная выживаемость в этих группах составила 91%, 79% и 53%, соответственно [14].
В первом сообщении о применении пентоксифиллина при тяжелом алкогольном гепатите были представлены обнадеживающие результаты, свидетельствующие о существенном снижении риска гепаторенального синдрома (ГРС) [32]. Большое рандомизированное контролированное исследование STOPAH, включавшее более 1000 пациентов, не продемонстрировало преимущество пентоксифиллина перед плацебо в отношении краткосрочной выживаемости [33]. Хотя необходимо принимать во внимание, что из исследования были исключены наиболее тяжелые больные — с ГРС, сепсисом и манифестной энцефалопатией — целесообразность применения пентоксифиллина представляется сомнительной.
Комбинация преднизолона и пентоксифиллина не выявила преимуществ по сравнению с монотерапией преднизолоном [13]. Таким образом, на сегодняшний день улучшение прогноза больных тяжелым алкогольным гепатитом, резистентных к кортикостероидам, возможно только путем выполнения срочной трансплантации печени [14].
Метаболические препараты («гепатопротекторы»)
Международные гепатологические ассоциации не рекомендуют применение лекарственных средств данной группы при АБП, что обусловлено слабой доказательной базой.
В исследовании J. Mato пероральное применение в дозе 1200 мг в сутки на протяжении двух лет сопровождалось более низкой летальностью или потребностью в трансплантации печени по сравнению с группой плацебо у больных компенсированным и субкомпенсированным алкогольным циррозом (класс, А и В по ) — 12% и 29% (p = 0.04), соответственно. Количество пациентов, прекративших и продолживших употребление алкоголя, было сопоставимо в обеих группах [35].
Результаты недавно опубликованного исследования и соавторов указывают на более низкую частоту ГРС у больных, получавших комбинацию преднизолон + по сравнению с монотерапией преднизолоном (p = 0.035). Показатели летальности в группах при этом статистически значимо не различались [28].
и соавторы представили результаты парентерального применения глицирризиновой кислоты у пациентов с алкогольным стеатогепатитом. Помимо отмеченного выше позитивного влияния на алкогольную зависимость, констатировано значимое снижение активности трансаминаз и уровня сывороточного билирубина [26].
L- ускоряет метаболизм аммиака, уменьшая проявления печеночной энцефалопатии. Показано, что препарат обладает способностью улучшать биохимические параметры у пациентов с хронической патологией печени, в том числе АБП [36]. Не исключено, что этот эффект обусловлен дезинтоксикацией обладающего универсальным цитотоксическим действием аммиака.
Неудовлетворительные результаты лечения тяжелых форм АБП служат основанием для разработки новых подходов, базирующихся на ключевых патогенетических механизмах. К находящимся на разных стадиях изучения, относятся модулирование иннатного иммунного ответа, подавление кишечной бактериальной и эндотоксиновой транслокации, блокирование апоптоза и активация фарнезоидного Х рецептора. В качестве многообещающего направления рассматривается технология индукции плюрипотентных стволовых клеток [37].
История медицины свидетельствует о том, что именно элиминация этиологического фактора определяет успех лечения большинства болезней, в том числе в эпидемиологическом ракурсе. Так, широкое внедрение в клиническую практику антигеликобактерной терапии позволило значимо снизить распространенность язвенной болезни желудка и двенадцатиперстной кишки, а противовирусных препаратов — эффективно контролировать заболеваемость гепатитом С. Казалось бы, в отношении АБП и других заболеваний решение проблемы лежит на поверхности: абстиненция ведет к выздоровлению или, по крайней мере, резкому снижению риска фатальных последствий. Однако этот постулат вызывает, по крайней мере, два вопроса: 1) что делать с больными, которые хотят, но не могут отказаться от алкоголя вследствие зависимости; 2) какой тактики ведения следует придерживаться в случае прогрессирования патологических изменений, несмотря на абстиненцию. Следовательно, весьма актуальным остается вопрос о медикаментозном лечении АБП, особенно тяжелых ее форм — гепатита и цирроза. Достижения в этой области не столь грандиозны, как в других разделах гепатологии. Многие лекарственные средства, на которые ранее возлагались надежды, основанные на результатах экспериментальных и пилотных данных, не оправдали их в рандомизированных контролированных исследованиях; показательным примером могут служить эссенциальные фосфолипиды. Тем важнее выбрать из относительно небольшого терапевтического арсенала препараты, проверенные временем и зарекомендовавшие себя с позиций доказательной медицины.
European Association for the Study of Liver. EASL clinical practical guidelines: management of alcoholic liver disease. J. Hepatol. 2012; 57: 399–420.
Mathurin P., Bataller R. Trends in the management and burden of alcoholic liver disease. J. Hepatol. 2015; 62(1S): S..
Lefkowitch of alcoholic liver disease. Clin. Liver Dis. 2005; 9: 37–53.
Lucey M., Mathurin P., Morgan hepatitis. N. Engl. J. Med. 2009; 360: 2758–2769.
DiMartini A., Dew M.A., Day N. et al. Trajectories of alcohol consumption following liver transplantation. Am. J. Transplant. 2010; 10: 2305–2312.
Stickel F., Buch S., Lau K. et al. Genetic variation in the PNPLA3 gene is associated with alcoholic liver injury in Caucasians. Hepatology. 2010; 53: 86–95.
Trépo E., Gustot T., Degré D. et al. Common polymorphism in the PNPLA3/adiponutrin gene confers higher risk of cirrhosis and liver damage in alcoholic liver disease. J. Hepatol. 2011; 55: 906–912.
Liu Y.L., Patman G.L., Leathart J.B. et al. Carriage of the PNPLA3 rs738409 C >G polymorphism confers an increased risk of fatty liver disease associated hepatocellular carcinoma. J. Hepatol. 2014; 61: 75–81.
Bataller R., North K. Brenner polymorphisms and the progression of liver fibrosis: a critical appraisal. Hepatology. 2003; 37: 493–503.
Naveau S., Giraud Borotto E. et al. Excess weight risk factor for alcoholic liver disease // Hepatology. 1997; 25: 108–111.
Poynard T., Mathurin P., Lai C.L. et al. A comparison of fibrosis progression in chronic liver diseases. J. Hepatol. 2003; 38: 257–265.
Song M., Chen T., Prough alcohol consumption causes liver injury in male mice through enhanced hepatic inflammatory response. Alcohol. Clin. Exp. Res. 2016; 40(3): 518–528.
Mathurin P., Louvet A., Duhamel A. et al. Prednisolone with vs. without pentoxifylline and survival of patients with severe alcoholic hepatitis: a randomized clinical trial. JAMA. 2013; 310: 1033–1041.
Mathurin P., Moreno C., Samuel D. et al. Early liver transplantation for severe alcoholic hepatitis // N. Engl. J. Med. 2011; 365: 1790–1800.
S., Franzmann M., Andersen I.B. et al. Longterm prognosis of fatty liver: risk of chronic liver disease and death. Gut. 2004; 53: 750–755.
Raynard B., Balian A., Fallik D. et al. Risk factors of fibrosis in liver disease. Hepatology. 2002; 35: 635–638.
Dunn W., Sanyal A.J., Brunt E.M. et al. Modest alcohol consumption is associated with decreased prevalence of steatohepatitis in patients with fatty liver disease (NAFLD) J. Hepatol. 2012; 57: 384–391.
Miller W.R, Walters S.T., Bennett effective is alcoholism treatment in the United States? J. Stud. Alcohol. 2001; 62: 211–220.
Corrao G., Bagnardi Zambon A., Torchio P. of alcohol intake in relation to risk of liver cirrhosis. Alcohol Alcohol. 1998; 33: 381–392.
Bellentani S., Saccoccio G., Costa G. et al. Drinking habits as cofactors of risk for alcohol induced liver damage. The Dionysos Study Group. Gut. 1997; 41: 845–850.
Vuittonet C.L., Halse M., Leggio L et al. Pharmacotherapy for alcoholic patients with alcoholic liver disease. Am. J. Health Syst. Pharm. 2014; 71(15): 1265–1276.
Leggio L., Kenna G.A., Ferrulli A. et al. Preliminary findings on the use of metadoxine for the treatment of alcohol dependence and alcoholic liver disease. Hum. Psychopharmacol. 2011; 26: 554–559.
Никитин И.Г, Байкова И.Е., Волынкина В.М. и др. Опыт использования глицирризиновой кислоты в лечении пациентов с алкогольной болезнью печени. Росс. журн. гастроэнтерол. гепатол. колопроктол. 2009; 19(1): 53–58.
Mendenhall C., Roselle G.A., Gartside P., Moritz T. Relationship of protein calorie malnutrition to alcoholic liver disease: A reexamination of data from two Veterans Administration Cooperative Studies. Alcoholism: Clinical and Experimental Research. 1995; 19(3): 635–641.
Tkachenko P, Maevskaya M, Pavlov A et al. Prednisolone plus S- in severe alcoholic hepatitis. Hepatol Int. 2016 Jun 23.
Diehl and alcoholic liver disease. Alcohol. 2004; 34: 81–87.
Louvet A., Naveau S., Abdelnour M. et al. The Lille model: a new tool for therapeutic strategy in patients with severe alcoholic hepatitis treated with steroids. Hepatology. 2007; 45: 1348–1354.
Gustot T., Maillart E., Bocci M. et al. Invasive aspergillosis in patients with severe alcoholic hepatitis. J. Hepatol. 2014; 60: 267–274.
Thursz M., Richardson P., Allison M.E. et al. Steroids or pentoxifylline for alcoholic hepatitis: results of the STOPAH trial. Hepatology. 2014; 60: LB1.
E., Thevenot T., Piquet M.A. al. Glucocorticoids plus in severe alcoholic hepatitis. N. Engl. J. Med. 2011; 365: 1781–1789.
Грюнграйф К., Й. Эффективность гранул L- при лечении хронических заболеваний печени. Сучасна гастроентерология. 2008; 2: 59–66.
Saberi B, Dadabhai AS, Jang YY Current Management of Alcoholic Hepatitis and Future Therapies. J Clin Transl Hepatol. 2016; 4(2): 113–122.
Рисунок. Схема стадийного течения алкогольной болезни печени (по P. Mathurin, R. Bataller, 2015, с изменениями).