Спастика – что это такое? Как и зачем с ней бороться?
В результате перенесенных инсультов или травм у пациентов могут наблюдаться судороги и спазмы мышц. Например, травма позвоночника может привести к судорогам в ногах, руках, шейном отделе. Обычно спазмы проявляют себя ночью, но нередко затрудняют жизнь и в дневное время. Эти непроизвольные сокращения мышц и называются спастикой или спастическим синдромом.
Что такое спастика простыми словами?
В нормальном состоянии механизм сокращения и расслабления мышц доведен до автоматизма. Все процессы работают безупречно благодаря слаженной работе конечностей, спинного мозга и головного мозга. Но инсульт или травма приводят к гибели клеток, которые отвечают за передачу сигналов двигательным нейронам спинного и головного мозга. В итоге тормозящие импульсы не доходят до адресата – координация нарушается.
Другими словами, мышцы ног или рук потеряли связь с мозгом, но при этом они продолжают накапливать энергию. Но эта энергия обязательно должна быть израсходована – это и происходит в виде болезненных судорог. Поскольку прямых команд от мозга мышцы не воспринимают, спазмы могут произойти в любую минуту.
Спастика: хорошо или плохо?
Механизмы формирования спастического синдрома до сих пор недостаточно изучены из-за своей сложности и многогранности. Спастика проявляется не у всех. И в ее наличии, и в ее отсутствии есть свои плюсы и минусы.
Спастика удерживает мышцы в тонусе и способствует их хорошему кровоснабжению. Многие врачи очень положительно оценивают спастику – это означает, что ноги или руки все еще можно восстановить, и человек снова сможет ходить. Даже несмотря на болевые ощущения, многие пациенты с радостью воспринимают, что их ноги (или руки) «работают», хоть и самопроизвольно. По крайней мере, на первом этапе реабилитации роль спастики является однозначно положительной. Но в дальнейшем усиление спастического синдрома приводит к серьезным сложностям в восстановлении.
Как не запустить спастику?
Если в первые недели реабилитации предпринять необходимые меры против усиления спастики, то можно снизить возможные негативные последствия. По крайней мере, удастся добиться такого состояния, чтобы комфортно передвигаться и жить нормальной жизнью. Для этого нужно:
Методы лечения
Полностью избавиться от спастического синдрома не удастся, но можно сделать так, чтобы судороги как можно меньше тревожили и не мешали в обычной жизни. Существует несколько направлений лечения:
ЛФК и лежание на животе с подушкой под грудь – это самые простые и одновременно самые эффективные средства против усиления спастики. У такого лечения нет побочных эффектов и рисков. К тому же если человек с инвалидностью сам покупает технические средства реабилитации, то можно получить от государства компенсацию их стоимости через социальные службы. Подробную информацию вы можете уточнить у наших консультантов.
Спастичность скелетных мышц
Спастичность – это состояние повышенного мышечного тонуса. Движения пациента при этом становятся скованными, человеку трудно передвигаться, говорить, совершать любые движения.
Во избежание постановки некорректного диагноза обращайтесь за консультацией к квалифицированным врачам Юсуповской больницы, которая оборудована современной медицинской аппаратурой. Здесь Вы можете пройти полную диагностику и получить адекватное лечение.
Спастичность скелетных мышц при неврологических заболеваниях
Спастичность скелетных мышц возникает вследствие многих неврологических заболеваний, в частности, рассеянного склероза, спинальной и черепно-мозговой травм, детского церебрального паралича, инсульта.
К спастичности скелетных мышц могут приводить:
Все вышеперечисленные заболевания могут привести к тяжелым осложнениям и последствиям. Поэтому при малейших недомоганиях обязательно необходимо обращаться за медицинской помощью. Чем раньше диагностируется заболевание, тем легче оно поддается лечению.
Лечение всех неврологических заболеваний – процесс непростой и достаточно длительный. Только опытный и высококвалифицированный врач может установить истинную причину недуга и назначить правильное и эффективное лечение.
Спастичность и ригидность
Ригидность – это устойчивое повышение тонуса мышц и сопротивления при попытке сделать какое-либо движение. Пациент не может согнуть и разогнуть конечности. В отличие от спастичности, ригидность остается постоянной во всем объеме пассивного движения.
Ригидность возникает по причине поражения среднего мозга, а также черной субстанции. Данное состояние является основным признаком болезни Паркинсона.
Спастичность ног при центральном параличе
Люди с центральным параличом имеют поражения головного мозга. При поражении тех участков клеток, которые отвечают за тонус мышц, возникает спастичность мышечных тканей конечностей. При врожденном центральном параличе деформация конечностей появляется не сразу, а постепенно.
Спастичность при множественном склерозе
На фоне множественного склероза развиваются два вида спастичности – сгибательная и разгибательная. В первом случае колени и бедра сгибаются и прижимаются к груди. Во втором случае у пациентов наблюдается непроизвольное выпрямление ног.
Спастичность при травмах головы
При травмах головного мозга и повреждениях мозжечка, среднего мозга и ствола мозга наблюдается изменение тонуса мышц, что проявляется нарушениями рефлексов, чувствительности и движений.
Спастичность языка
Спастичность языка подразумевает нарушение тонуса мускулатуры не только самого языка, но также и лица, шеи, губ. В данном случае у пациентов язык оттянут назад, его спинка изогнута и приподнята вверх, кончик языка при этом не выражен. Иногда язык может быть «жалом» вытянут вперед.
Повышение тонуса круговой мышцы рта приводит к плотному смыканию губ, либо, напротив, рот может быть приоткрыт. Во втором случае также наблюдается повышенное слюнотечение.
Доктора Юсуповской больницы оказывают медицинскую помощь пациентам при любой тяжести заболевания. В больнице применяют современные инновационные методы терапии, позволяющие сгладить симптоматику патологии и во многих случаях вовсе избавить пациентов от недуга.
Шкала спастичности Ашфорта
«Жесткость» мышц или спастичность, опытный врач может без труда определить во время осмотра. Если доктор легко может согнуть и разогнуть ногу или руку пациента, то все показатели эластичности и степени напряженности мышц в норме. Если врач ощущает мышечное сопротивление, то имеет место, повышенный мышечный тонус. Его оценку проводят по шкале спастичности Ашфорта, имеющей следующую структуру:
Каким бы ни был показатель спастичности мышц, доктора Юсуповской больницы помогут каждому пациенту снизить или вовсе избавиться от подобной симптоматики и улучшить качество их жизни.
Запишитесь на прием к врачам Юсуповской больницы.
Постинсультная спастичность
В России более миллиона больных, перенесших инсульт. Более чем у половины из них остаются после него двигательные нарушения, которые существенно снижают качество жизни и способствуют стойкой инвалидности (инвалидизации) пациентов [1]: чаще всего это гемип
В России более миллиона больных, перенесших инсульт. Более чем у половины из них остаются после него двигательные нарушения, которые существенно снижают качество жизни и способствуют стойкой инвалидности (инвалидизации) пациентов [1]: чаще всего это гемипарез или монопарез конечности с повышением мышечного тонуса по типу спастичности [1, 2, 9, 20].
Патогенез постинсультной спастичности
Спастичность выявляется при исследовании пассивных движений в паретичной конечности как повышенное сопротивление (сокращение) мышцы при ее быстром растяжении. Развитие спастичности при центральном парезе конечности связывается со снижением тормозных влияний на спинальные мотонейроны и интернейроны, что приводит к увеличению числа импульсов, достигающих альфа-мотонейронов в ответ на растяжение мышцы. Снижение тормозных влияний на спинальные мотонейроны и интернейроны объясняется комбинированным поражением пирамидных и экстрапирамидных путей внутри головного мозга вследствие инсульта, при этом важную роль в развитии спастичности отводят повреждению кортико-ретикуло-спинального тракта [2, 16, 20].
В экспериментальных исследованиях показано, что изолированное поражение пирамидного пути не вызывает спастичности, а приводит лишь к парезу в дистальных отделах конечностей, особенно утрате тонких движений руки. В случаях поражения головного мозга при инсульте обычно возникает поражение не только пирамидного пути, но и других двигательных путей, таких как кортико-ретикуло-спинальный тракт, что и сопровождается спастичностью. Поэтому постинсультная спастичность рассматривается как комбинированное поражение пирамидных и экстрапирамидных структур внутри головного мозга [2, 16, 20]. Экстрапирамидная система внутри головного мозга может быть повреждена вследствие поражения самих базальных ганглиев или приходящих либо исходящих от них путей.
В развитии церебральной спастичности при поражении головного мозга большую роль играет ослабление тормозных влияний преимущественно на альфа-мотонейроны, обеспечивающих движение антигравитационных мышц; это объясняет появление характерных проявлений постинсультного спастического гемипареза: приведение плеча, сгибание руки в локтевом и лучезапястном суставах, приведение бедра, разгибание колена и подошвенное сгибание в голеностопном суставе [2, 16, 20].
У больных инсультом спастичность обычно нарастает в паретичных конечностях в течение нескольких недель и месяцев, сравнительно редко (чаще всего при восстановлении двигательных функций) наблюдается спонтанное уменьшение спастичности. Во многих случаях у больных инсультом спастичность ухудшает двигательные функции, способствует развитию контрактуры и деформации конечности, затрудняет уход за обездвиженным больным и иногда сопровождается болезненными мышечными спазмами [2, 5, 9, 11, 20].
Если постинсультный парез сохраняется в течение длительного времени (несколько месяцев и более), то могут возникнуть структурные изменения сегментарного аппарата спинного мозга (укорочение дендритов альфа-мотонейронов и коллатеральный спрутинг афферентных волокон, входящих в состав задних корешков), которые способствуют прогрессированию спастичности [16]. Также развиваются вторичные изменения в паретичных мышцах, сухожилиях и суставах, которые усиливают двигательные расстройства и сопротивление, возникающее в мышце при ее растяжении, что необходимо учитывать при оценке мышечного тонуса в паретичных или парализованных конечностях [16, 20].
Восстановление утраченных двигательных функций максимально в течение двух-трех месяцев с момента инсульта, в дальнейшем темпы восстановления снижаются значительно. Через год после развития инсульта маловероятно уменьшение степени пареза, однако возможно улучшение двигательных функций и уменьшение инвалидности путем тренировки равновесия и ходьбы, использования специальных приспособлений для передвижения и снижения спастичности в паретичных конечностях [1, 2, 9, 11, 20].
Лечение постинсультной спастичности
Лечение постинсультной спастичности направлено на улучшение функциональных возможностей паретичных конечностей, ходьбы, самообслуживания больных. К сожалению, в части случаев возможности лечения спастичности ограничиваются только уменьшением боли и дискомфорта, связанного с высоким мышечным тонусом, облегчением ухода за парализованным пациентом или устранением имеющегося косметического дефекта, вызванного высоким мышечным тонусом [2, 11, 20].
Один из наиболее важных вопросов, который приходится решать при ведении больного с постинсультной спастичностью, сводится к следующему: ухудшает или нет спастичность функциональные возможности больного? В целом, функциональные возможности конечности у больного с постинсультным парезом конечности хуже при наличии выраженной спастичности, чем при ее легкой степени. Вместе с тем у части больных при выраженной степени пареза спастичность в мышцах ноги может облегчать стояние и ходьбу, а ее снижение может привести к ухудшению двигательной функции и даже к падениям [2, 11, 16, 20]. Перед лечением постинсультной спастичности необходимо определить возможности лечения у конкретного больного (улучшение двигательных функций, уменьшение болезненных спазмов, облегчение ухода за пациентом и др.) и обсудить их с пациентом и/или его родственниками. Возможности лечения во многом определяются сроками с момента заболевания и степенью пареза, наличием когнитивных расстройств [2, 11, 16, 20]. Чем меньше сроки с момента развития инсульта, вызвавшего спастический парез, тем более вероятно улучшение от лечения спастичности, потому что оно может привести к существенному улучшению двигательных функций, предотвратив формирование контрактур и повысив эффективность реабилитации в период максимальной пластичности центральной нервной системы. При длительном сроке заболевания менее вероятно существенное улучшение двигательных функций, однако можно значительно облегчить уход за больным и снять дискомфорт, вызванный спастичностью. Чем меньше степень пареза в конечности, тем более вероятно, что лечение спастичности улучшит двигательные функции [16, 20].
Лечебная гимнастика представляет наиболее эффективное направление ведения больного с постинсультным спастическим гемипарезом, она направлена на тренировку движений в паретичных конечностях и предотвращение контрактур [1, 2, 16, 20]. Однако больным, имеющим выраженную спастичность в сгибателях верхних конечностей, не следует рекомендовать интенсивные упражнения, которые могут значительно усилить мышечный тонус (например, сжимание резинового кольца или мяча, использование эспандера для развития сгибательных движений в локтевом суставе).
В качестве методов физиотерапии используются лечение положением, обучение пациентов стоянию, сидению, ходьбе (с помощью дополнительных средств и самостоятельно), бинтование конечности, применение ортопедических аппаратов, тепловые воздействия на спастичные мышцы, а также электрическая стимуляция определенных мышечных групп (например, разгибателей пальцев кисти или передней большеберцовой мышцы [4]).
Массаж мышц паретичных конечностей, имеющих высокий мышечный тонус, возможен только в виде легкого поглаживания. Напротив, в мышцах-антагонистах можно использовать растирание и неглубокое разминание в более быстром темпе.
Иглорефлексотерапия относительно часто используется в нашей стране в комплексной терапии больных, имеющих постинсультный спастический гемипарез, однако контролируемые исследования, проведенные за рубежом, не показывают существенной эффективности этого метода лечения [8].
У больных, перенесших инсульт и имеющих локальную спастичность в паретичных мышцах, можно использовать ботулинический токсин типа А или ботулотоксин (Ботокс, Диспорт). Использование ботулинического токсина показано, если у больного, перенесшего инсульт, имеется мышца с повышенным тонусом без контрактуры, а также отмечаются боль, мышечные спазмы, снижение объема движений и нарушение двигательной функции, связанные со спастичностью этой мышцы [2–4, 17, 20]. Действие ботулинического токсина при внутримышечном введении вызвано блокированием нервно-мышечной передачи, обусловленным подавлением высвобождения нейромедиатора ацетилхолина в синаптическую щель.
Клинический эффект после инъекции ботулинического токсина отмечается спустя несколько дней и сохраняется в течение 2–6 месяцев, после чего может потребоваться повторная инъекция. Лучшие результаты отмечаются при использовании ботулинического токсина в ранние сроки (до года) с момента заболевания и легкой степени пареза конечности. Применение ботулинического токсина может быть особенно эффективно в тех случаях, когда имеется эквино-варусная деформация стопы, вызванная спастичностью задней группы мышц голени, или высокий тонус мышц-сгибателей запястья и пальцев, ухудшающий двигательную функцию паретичной руки [20]. В контролированных исследованиях доказана эффективность Диспорта при лечении постинсультной спастичности в руке [3].
В качестве побочных эффектов от использования ботулотоксина могут быть кожные изменения и боли в месте инъекции. Они обычно самостоятельно регрессируют в течение нескольких дней после инъекции. Возможна значительная слабость мышцы, в которую введен ботулотоксин, а также слабость в мышцах, расположенных близко к месту инъекции, локальная вегетативная дисфункция. Однако мышечная слабость обычно компенсируется деятельностью агонистов и не приводит к ослаблению двигательной функции. Ограничение широкого применения ботулинического токсина в клинической практике во многом вызвано его высокой стоимостью.
Хирургические операции для уменьшения постинсультной спастичности используются редко, они возможны на четырех уровнях — на головном мозге (электрокоагуляция бледного шара, вентролатерального ядра таламуса или мозжечка), спинном мозге (селективная задняя ризотомия), периферических нервах (рассечение периферических нервов) и мышцах или их сухожилиях [2, 16, 20].
С помощью специальной помпы интратекально при постинсультной спастичности может использоваться баклофен [10, 13, 19]. Использование баклофеновой помпы в сочетании с лечебной гимнастикой, физиотерапией улучшает скорость и качество ходьбы больных с постинсультной спастичностью, способных к самостоятельному передвижению [10]. Имеющийся 15-летний клинический опыт применения баклофена интратекально у больных, перенесших инсульт, свидетельствует о высокой эффективности этого метода в уменьшении не только степени спастичности, но и болевых синдромов и дистонических расстройств [19]. Отмечено положительное влияние баклофеновой помпы на качество жизни больных, перенесших инсульт [13]. Широкое применение этого метода терапии в клинической практике ограничивает его высокая стоимость.
Лечение пероральными антиспастическими средствами
В клинической практике для лечения постинсультной спастичности наиболее часто используются пероральные антиспастические лекарственные средства [5, 11, 12, 16]. Применяемые внутрь антиспастические средства, уменьшая мышечный тонус, могут улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить действие лечебной физкультуры и вследствие этого предупредить развитие контрактур. При легкой степени спастичности применение миорелаксантов может привести к значительному положительному эффекту, однако при выраженной спастичности могут потребоваться большие дозы миорелаксантов, применение которых нередко вызывает нежелательные побочные эффекты [2, 5, 11, 20]. Лечение миорелаксантами начинают с минимальной дозы, затем ее медленно повышают для достижения эффекта. Антиспастические средства обычно не комбинируют. В нашей стране для лечения постинсультной спастичности наиболее часто используют баклофен (Баклосан), тизанидин (Сирдалуд) и толперизон (Мидокалм).
Баклофен (Баклосан) оказывает антиспастическое действие преимущественно на спинальном уровне. Препарат представляет аналог гамма-аминомасляной кислоты (ГАМК); он связывается с пресинаптическими ГАМК-рецепторами, приводя к уменьшению выделения возбуждающих аминокислот (глутамата, аспартата) и подавлению моно- и полисинаптической активности на спинальном уровне, что и вызывает снижение спастичности. Препарат оказывает также умеренное центральное анальгезирующее действие. Баклофен используется при спинальной (спинальная травма, рассеянный склероз) и церебральной спастичности различного генеза [5, 11, 16]. Начальная доза составляет 5–15 мг/сут (в один или три приема), затем дозу увеличивают на 5 мг каждый день до получения желаемого эффекта; препарат принимают во время еды. Максимальная доза баклофена для взрослых составляет 60–75 мг/сут. Побочные эффекты чаще проявляются сонливостью, головокружением в начале лечения, хотя в дальнейшем могут ослабевать. Иногда возникают тошнота, запор, диарея, артериальная гипотония; требуется осторожность при лечении больных пожилого возраста, перенесших инсульт.
Тизанидин (Сирдалуд) — миорелаксант центрального действия, агонист альфа-2-адренергических рецепторов. Препарат снижает спастичность вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот и активацией глицина, снижающего возбудимость интернейронов спинного мозга. Тизанидин (Сирдалуд) обладает также умеренным центральным анальгезирующим действием. Препарат эффективен при церебральной и спинальной спастичности, а также при болезненных мышечных спазмах [5, 11, 12, 15, 16, 20]. Начальная доза препарата составляет 2–6 мг/сут в один или три приема, средняя терапевтическая доза — 12–24 мг/сут, максимальная доза — 36 мг/сут. В качестве побочных эффектов могут возникать сонливость, сухость во рту, головокружение и незначительное снижение артериального давления, что ограничивает использование препарата при постинсультной спастичности [15].
Толперизон (Мидокалм) — мышечный релаксант центрального действия, который близок к лидокаину по химической структуре и стабилизирует мембраны нервных клеток. Толперизон снижает активность спинальных нейронов, участвующих в формировании спастичности, путем ограничения потока натрия через мембрану нервных клеток. Наиболее часто используется по 300–450 мг/сут в два или три приема. Около 40 лет толперизон успешно применялся при лечении спастичности различного генеза, были проведены небольшие исследования, показавшие его эффективность при церебральной спастичности [7, 14].
Недавно было проведено плацебо-контролируемое исследование [18], в котором показана эффективность, безопасность и хорошая переносимость толперизона у больных, перенесших инсульт и имеющих спастичность в паретичных конечностях. В многоцентровое исследование (два центра в Германии и один центр в Болгарии) было включено 120 больных (43 мужчины и 77 женщин) в возрасте от 20 до 78 лет (средний возраст — 63 года) с постинсультной спастичностью. Больные перенесли инсульт в сроки от 3 месяцев до 30 лет (в среднем 3,3 года с момента инсульта) и имели спастичность, выраженность которой достигала 2 баллов и более по шкале Эшуорта в одной или нескольких мышечных группах. У большинства (111 из 120) больных наблюдался гемипарез со спастичностью в верхней и нижней конечности, средняя степень спастичности составила 3 балла по шкале Эшуорта. По основным клиническим характеристикам группа больных, которые принимали толперизон, не отличалась от группы плацебо. В течение четырех недель больные получали толперизон или плацебо, доза которых подбиралась врачом для получения максимального эффекта и могла достигать от 300 до 900 мг толперизона. Далее больные продолжали принимать толперизон или плацебо в течение еще двух месяцев (восьми недель).
Главной целью исследования было изучение влияния толперизона на выраженность спастичности по шкале Эшуорта через 4 недели лечения (в сравнении с плацебо). Дополнительные цели исследования включали изучение влияния толперизона на ежедневную двигательную активность (по пятибалльной шкале), ходьбу в течение двух минут, максимальное расстояние при ходьбе (при спастичности в нижних конечностях), индекс Бартел, общее впечатление врача и больного о лечении.
Результаты проведенного исследования показали, что толперизон достоверно (р
В. А. Парфенов, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва
Чем лечить спастику ног
В настоящее время для лечения мышечной спастичности предлагается все больше потенциально терапевтических методов. Для выбора нужной методики очень важно иметь представление о различных элементах спастического состояния мышц.
Рефлекторная дуга вызывает рефлекс растяжения. Этот рефлекс начинается с альфа мотонейронов, расположенных в передних рогах спинного мозга. Альфа-мотонейроны посылают аксоны через периферические нервы, чтобы соединиться с концевой пластинкой мышечной клетки при помощи нервно-мышечного перехода. Обратная связь мышечной активации вырабатывается в мышечных волокнах и тельцах Гольджи.
Информация подается обратно в мотонейроны с помощью сенсорных нейронов. Сенсорные нейроны связывают рефлекторную дугу с мотонейронами в спинном мозге, либо в моносинапсе, либо в полисинапсе через интернейроны.
а) Ригидность мышц у пациентов со спастичностью в положении сидя. В повседневной клинической практике диагностика и проверка спастичности выявляется сопротивлением пассивному движению и увеличению сухожильных рефлексов. Это в полной мере соответствует широко распространенному определению спастичности: «. двигательное расстройство представляет собой нарушение, характеризующееся зависящим от скорости возрастанием тонических рефлексов растяжения (мышечного тонуса), повышением сухожильных рефлексов, что является результатом гипервозбудимости рефлекса растяжения как одного из компонентов синдрома верхнего мотонейрона».
Важно понимать, как результаты клинического обследования сопоставляются с результатами более объективных методов оценки. Поэтому мы должны исследовать различные методы оценки ригидности при растяжении спастических мышц.
Ригидность можно разделить по увеличению:
1. Пассивной жесткости сухожилий, суставов, мышц.
2. Внутренней скованности сократившихся мышечных волокон.
3. Жесткости, обусловленной рефлексом растяжения.
Для выделения важности различных компонентов, краткое пассивное растяжение может быть применено к изометрической мышце во время различной произвольной деятельности. У здоровых лиц и пациентов со спастикой, такие исследования могут быть выполнены путем введения четко определенных угловых движений в суставе, а затем расчета изменений в силе и /или изменения в электрической активности мышц.
На рисунке ниже показано увеличение угла движения голеностопного сустава в спастичной и контралатеральной конечностях у пациента с гемиплегией после выполнения пассивного тыльного сбигания. Общий прирост увеличения угла подвижности является суммой рефлекс-опосредованной и нерефлекторно-опосредованной подвижности. Нерефлекторное увеличение объема движения измеряется при непрерывной электрической стимуляции большеберцового нерва, иннервирующего подошвенные сгибатели. Электрическая стимуляция активирует рефлекс растяжения.
Рефлекторный объем движения (общий объем движения минус нерефлекторный объем движения) превышает нерефлекторный объем движения почти в два раза в контралатеральной и спастической конечностях. Рефлекторный и нерефлекторный объем движений в спастической конечности выше, чем в противоположной здоровой конечности.
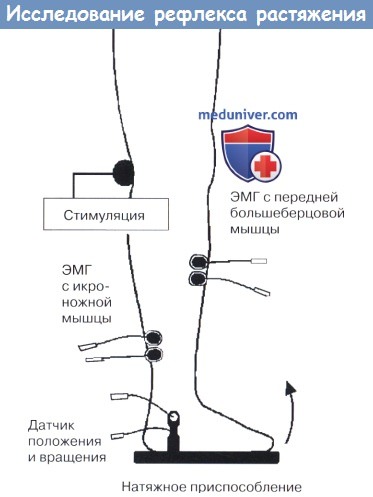
Ноги установлены на платформу. Колебания и положение стопы измеряются с платформы.
Чтобы выявить рефлекс растяжения, двигатель, подключенный к платформе (не показано), вращает голеностопный сустав.
Механическое значение рефлекса растяжения определяется путем выявления изменений показателей угла сустава.
Рефлекс растяжения также может быть записан путем регистрации потенциала действия через биполярные электроды ЭМГ, расположенные над исследуемой мышцей.
Для измерения нерефлекторного компонента ригидности подошвенных сгибателей рефлекс растяжения должен быть подавлен во время растяжения.
Это может быть сделано путем стимуляции большеберцового нерва в подколенной ямке. 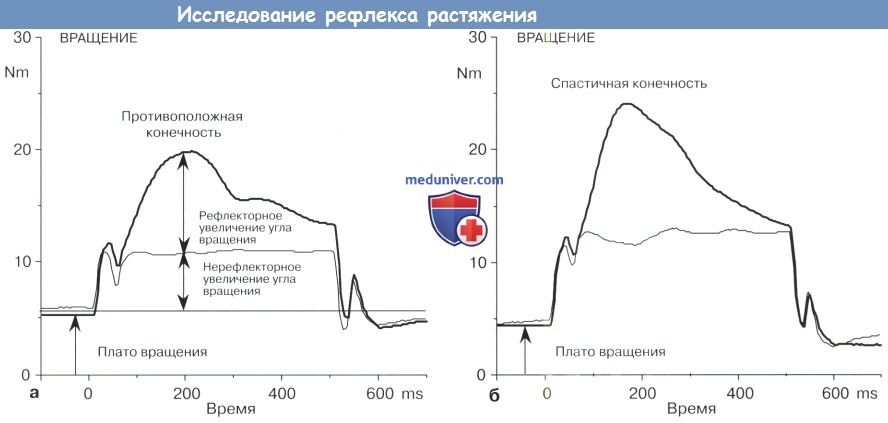
А противоположная конечность.
Б Спастичная конечность.
Электрическая стимуляция большеберцового нерва (10 Гц) вызвала подошвенное сгибание и рефлекс растяжения подавлен в течение нерефлекторного измерения угла движения.
б) Нерефлекторный/мышечный компонент. Часть колебаний связана со свойствами коллагеновых тканей (пассивные свойства) и сократительного аппарата в растянутых мышцах (внутренние свойства). Совокупность этих свойств определяется как нерефлекторные свойства.
Пассивная жесткость сустава при спастичности увеличивается до сотен процентов в зависимости от исследуемого сустава, положения сустава, группы пациентов и применяемого метода. У пациентов с гемиплегией, во время пассивной тыльной флексии стопы пассивная ригидность увеличивается на 50%. При измерении пассивной жесткости через три месяца после инсульта, в пораженной конечности определяется увеличение пассивной ригидности на 39%. Имеет место небольшая корреляция между повышенной пассивной ригидностью и такими факторами, как объем движения, шкала Ashworth, и шкала Fugl-Meyer.
Это означает, что ранние изменения механического ответа на растягивание в подошвенных сгибателях происходят без учета уровня инвалидизации. Изменение пассивной жесткости может быть связано с изменениями в коллагеновой ткани, сухожилиях, суставной сумке, и мышцах, что может приводить к клинически выраженным контрактурам. Изменения в области ахиллова сухожилия, скорее всего, укажут на увеличение ригидности, но нельзя исключать того, что изменения в других коллагеновых тканях или мышечных волокнах не приведут к повышенной ригидности.
Изменения в мышечных волокнах должны проявляться ригидностью. Sinkjaer обнаружил значительное увеличение внутренней ригидности тыльной флексии лодыжки при спастичности, а у пациентов с гемиплегией наблюдал увеличение ригидности подошвенных сгибателей на 20%. Эти данные согласуются с физиологическими, морфометрическими и гистохимическими исследованиями, демонстрирующими специфические для спастических мышц изменения мышечных волокон. Пациенты особенно чувствительны к этому типу увеличения рефлекторной реакции, если мышцы были относительно обездвижены.
Изменения в мышцах голени в результате обездвиживания или иммобилизации в укороченном положении, которые были продемонстрированы в экспериментах на животных, могут считаться полезной моделью для измерений в паретических «гиперактивных» мышцах.
Несмотря на это, причины патологических изменений в механических свойствах сократительных элементов спастических мышц, также как и изменения соединительной ткани (например, в сухожилии) по-прежнему обсуждаются. Ряд авторов, отметивших рост пассивной и внутренней ригидности, сообщают о том, что спастичности может способствовать периферический нерефлекторно опосредованный процесс.
в) Рефлекс-опосредованный механический мышечный ответ. В активной мышце рефлекс растяжения в значительной степени способствует ответу на общее механическое растяжение у здоровых испытуемых. Как у здоровых, так и демонстрирующих спастичность испытуемых при низком и среднем уровне сжатия, рефлекс-опосредованный механический ответ составляет около 50% от общего ответа в подошвенных сгибателях стопы. У пациентов с умеренно выраженной мышечной спастичностью, рефлекс-опосредованная ригидность в подошвенных сгибателях лодыжки не изменилась по сравнению со здоровой контрольной группой.
У пациентов с повреждением спинного мозга, методом системной идентификации, отделяющим нерефлекторный и рефлекторный компоненты, было показано увеличение нерефлекторной ригидности, а также увеличение рефлекторной ригидности в разгибателях голеностопного сустава со слабо выраженными контрактурными изменениями.
Все группы пациентов имели клинические признаки спастичности, по шкале Ashworth.
Повышенный мышечный тонус вызван не только увеличением нерефлекторных свойств (пассивные и внутренние мышечные компоненты). Гипотеза заключается в том, что пациенты со спастикой не в состоянии препятствовать механически прочным рефлексам растяжения в связи с нарушениями функции спинного мозга и нисходящим контролем в спокойной клинической ситуации.
Повышение рефлекса растяжения в расслабленной спастической мышце и при слабом сокращении может быть вызвано снижением постсинаптического и пресинаптического торможения и/или изменениями в подавлении после активации. Этих ингибирующих механизмов, как принято считать, достаточно, чтобы расслабить мышцы у здоровых субъектов. Так, если мышцы здоровых людей сделать более активными, и снять эти ингибирующие механизмы — рефлекторная ригидность выражается полностью, так же как и у пациентов со спастичностью с расслабленными, «раскованными» мышцами.
г) Нейрофизиология повышенного мышечного тонуса и высокого рефлекса растяжения мышц в покое при спастичности. В покое у здорового человека, двигательные нейроны спинного мозга (альфа-мотонейроны) «молчат» и далеки от порога запуска. Причиной является ограниченная активность в основном возбуждающем пути к двигательным нейронам (в кортикоспинальных клетках моносинаптическая передача на мотонейроны выполняется на низкой скорости), и что еще более важно, свой вклад может также внести тоническая активность от нисходящих и периферических ингибирующих путей.
В дополнение к этому активность гамма мотонейронов и, следовательно, чувствительных мышечных веретен, необходимых для растяжения, также низкая. Следовательно, при значительном растяжении может быть возбуждено только ограниченное количество мышечных волокон. Центральный эффект Iа-афферентов на альфа-мотонейроны снижается пресинаптическим торможением, преобладающим у пациентов в покое. Было показано, что при спастичности чувствительность мышечных веретен к растяжению не увеличивается. Таким образом, нет оснований поддерживать мнение, что повышенная активность гамма-мотонейронов должна играть важную роль в мышечной спастичности (так называемая гамма-спастичность).
По данным некоторых исследований, передача в различных путях торможения недостаточна, по крайней мере, у некоторых пациентов со спастикой. Это включает взаимное Ia-торможение, Ib-торможение и рецидивирующее ингибирование. Сниженная передача, предположительно приводит к повышенной возбудимости альфа-мотонейронов, что может быть фактором, способствующим спастичности по крайней мере, в отдельных случаях.
Пресинаптическое торможение лишь представляется сниженным у некоторых пациентов со спастикой. Для нижних конечностей оно снижается при мышечной спастичности и параличе нижних конечностей, но не у пациентов с гемиплегией.
Современное понимание патофизиологии спинномозгового компонента спастичности определяет его как многофакторный синдром, вызываемый практически любой комбинацией недостаточной передачи в ряде спинномозговых механизмов контроля, включая взаимное Iа-торможение, пресинаптическое торможение, возвратное торможение, lb-торможение, подавление после активации, и, вероятно, некоторые другие механизмы.
Обобщение механизмов повышенного рефлекса растяжения у пациентов со спастичностью, очевидно, проблематично на этом сложном фоне. Таким образом, следует иметь в виду, что дальнейшие описания упрощены и совсем не обязательно применимы для всех случаев спастичности.
д) Порог и усиление патологического рефлекса растяжения. В принципе на патологический рефлекс растяжения могут влиять два различных параметра:
1. Прежде всего, порог рефлекса растяжения (эквивалентный порогу включения двигательного нейрона) может быть уменьшен, в результате чего для достижения порогового рефлекса достаточно меньшего или медленного движения.
2. Затем, может изменяться усиление рефлекса растяжения, что выражается аномальным увеличением амплитуды рефлекса растяжения с увеличением движения или скорости движения без существенного изменения в рефлекторном пороге.
Порог и усиление могут быть определены по соотношению «вход/выход» при построении кривой рефлекса растяжения (выход) на различных скоростях растяжения (вход). В расслабленных подошвенных сгибателях стопы порог рефлекса растяжения камбаловидной мышцы снижается, однако мнение оспаривается. Спастичность связана с увеличением возбудимости мотонейронов в покое — «прикроватная» ситуация. Порог рефлекса растяжения, видимо, отражает эту повышенную возбудимость мотонейронов в расслабленной или почти расслабленной мышце.
Объяснение изменения порога рефлекса растяжения может вестись разными путями, включая отсутствие взаимного торможения, измененное внутренние регулирование передачи импульса от Iа-афферентов при спастичности, изменения в деятельности гамма-мотонейрона, а также изменения в деятельности (в порядке убывания) двигательных путей ствола мозга, которые влияют на постсинаптическое торможение. Поскольку рефлекс растяжения гораздо менее чувствителен к пресинаптическому торможению, чем Н-рефлекс, то объяснить как снижение пресинаптического торможения может осуществить сдвиг порога активности, достаточно сложно.
е) Ригидность мышц во время ходьбы при спастичности. Состояние мышц и кожных рефлексов во время передвижения с адаптацией к каждой фазе шага значительно изменяется. Эта регулировка утрачивается или сильно снижается при спастичности. Увеличенный мышечный тонус относится к более функциональным двигательным задачам; в этой связи важным становится исследование «нерефлекторного/мышечного компонента» совместно со спинномозговой/центральной интеграцией афферентного входа при более функциональных задачах на выполнение таких движений, как ходьба.
1. Нерефлекторный/мышечный компонент. Повышение пассивной ригидности и внутренней скованности мышц, выявленные в положении сидя спастического субъекта, также присутствует во время ходьбы. На основании косвенных измерений силы ахиллова сухожилия у пациентов с гемипарезом, Berger et al. показали, что во время ходьбы жесткость мышц нерефлекторно увеличивается. Авторы предположили, что при спастичности у пациентов с гемипарезом может развиваться большее мышечное напряжение во время ходьбы при более низком уровне активности нейронов (ЭМГ активности), чем в контрольной группе здоровых людей. Это обстоятельство было расценено как преимущество, поскольку благодаря этому обеспечивается возможность поддержки веса тела в положении для ходьбы, несмотря на неспособность активации камбаловидной мышцы.
Возможно, это верно, но не стоит забывать, что основная часть увеличения нерефлекторной жесткости вызвана повышенной пассивной жесткостью, которая будет ухудшать тыльное сгибание. Это становится еще более заметным при спастичности, когда снижается произвольная подвижность стопы. Кроме того, у таких пациентов мышцы во время ходьбы часто дополнительно сокращаются, что еще больше увеличивает нерефлекторную жесткость.
2. Мышечные рефлексы во время спастической ходьбы. Помимо повышенной нерефлекторной жесткости, происходящая у здорового человека коррекция рефлексов, при спастичности нередко отсутствует. Нарушение модуляции рефлексов было интерпретировалось как увеличение мышечной скованности из-за нарушения супраспинального контроля рефлекса растяжения.
Nielsen et al. исследовали свойства рефлекса растяжения во время стояния и ходьбы, для более общего понимания, как именно нарушаются при спастичности «входные-выходные» свойства рефлекторной дуги, участвующей в контроле рефлекса растяжения у пациентов в положение сидя, перенесших инсульт. У здоровых людей в ЭМГ-активности передней большеберцовой мышцы большая разница была найдена в преддверии рефлекса растяжения в ранней стадии ходьбы (309 град/с) по сравнению с положением сидя (71 град/с). У пациентов, перенесших инсульт, эта разница в пороговых значениях была значительно сокращена до незначительных различий в порогах из 108 град/с на ранней стадии ходьбы по сравнению с 74 град/с в положении сидя.
Предположительно, это говорит о том, что изменения задачи на движение меняют порог, но не увеличивает входные и выходные свойства рефлекса растяжения. Кроме того, специфическое изменение порога при конкретной задаче при спастичности было невелико.
Разницу между порогом рефлекса растяжения во время сидения и ходьбы можно рассматривать как «безопасный диапазон», при котором скорость движения голеностопного сустава может меняться без рефлекса растяжения. Этот интервал в три и более раза выше, чем в контрольной группе. Следовательно, диапазон, в котором скорость сгибания может меняться в начальной фазе ходьбы, не вызывая рефлекса растяжения, при спастичности снижается. Тыльное сгибание связано с рефлексом растяжения подошвенных сгибателей, и, если скорость движения голеностопного сустава превысит порог рефлекса растяжения, будет наблюдаться быстрое сгибание ноги.
По этой причине человек начинает спотыкаться и даже падать. Таким образом, пациент должен адаптировать скорость ходьбы к своей способности подавлять рефлекс растяжения подошвенных сгибателей при переходе от положения стоя к начальной фазе ходьбы.
Периферические изменения, которые происходят во время ходьбы при спастичности, показаны на рисунке ниже.
На рисунке показана схема жесткости голеностопного сустава при полном цикле шага у здоровых лиц. Общая жесткость включает пассивный, внутренний и рефлекторно-опосредованный компоненты. У здоровых субъектов общая жесткость в положение стоя будет возрастать по мере увеличения внутренней жесткости всей позиции (в связи с увеличением центрального вклада в тонус мышц), также как увеличивается рефлекторная жесткость и пассивная жесткость, когда подошвенные сгибатели растянуты. Во время ходьбы, жесткость подошвенных сгибателей будет зависеть от пассивного компонента только тогда, когда центральный вход на эти мышцы равен нулю, а порог рефлекса перешел от «низкого» в положение «высокого» во время ходьбы.
У спастических пациентов внутренняя жесткость и рефлекторная жесткость, скорее всего, почти нормальная и пассивная жесткость увеличивается в положение стоя. В фазе переноса, пассивная жесткость увеличивается, и внутренняя жесткость равна нулю (за исключением совместного сокращения). В связи с пониженным порогом рефлекса растяжения, рефлекторная жесткость будет повышаться, если сгибание становится слишком быстрым.
ж) Клиническое значение. Врачи сталкиваются с рядом ситуаций, когда спастичность является основной причиной инвалидности пациента. До начала лечения должны быть четко определены цели терапии:
1. У спастических пациентов, которые не в состоянии ходить, но не страдают от контрактуры или болезненных спазмов, антиспастическое лечение предназначено для снижения мышечного тонуса, чтобы мышцы стали «вялыми». Это позволит повысить качество жизни, и такая, сильнодействующая терапия доступна.
2. У спастических пациентов, которые сохранили способность ходить, цели антиспастического лечения очень разные, по крайней мере, во время активной части дня. Здесь целью является подавление нежелательной активности мышц, и усиление желаемой активности в скоординированный «шаблон», который позволит улучшить ходьбу. Расширение знаний о регулировании и важности механизмов спинального и нисходящего контроля во время движения у здоровых лиц и при спастичности улучшит такое антиспастическое лечение. Например, клонидин, ципрогептадин, и баклофен способные влиять на рефлексы, оказывают разный эффект на движение.
Движения у спастического пациента могут улучшиться после лечения, предотвращающего повышение возбудимости мотонейронов, в силу снижения порога рефлекса растяжения. Nielsen и Sinkjaer показали, что баклофен увеличивает пороговую скорость камбаловидного рефлекса растяжения во время сидения у пациентов с мышечной спастичностью, но в то же время, он ослабляет силу мышечного сокращения. Альтернативным методом снижения рефлекса растяжения во время ходьбы является электрическая стимуляция периферических нервов, которые активируют пути торможения.
При применении стимуляции выше порога активности для глубокого малоберцового нерва у спастических пациентов, перенесших инсульт, в начале движения было показано, что порог камбаловидного рефлекса растяжения может увеличиваться в широких пределах и могут восстанавливаться почти нормальные фазовые модуляции рефлекса растяжения во время ходьбы. Интересно, что стимуляция выше порога активности приведет к прямой стимуляции от тыльных флексоров, тем самым способствуя улучшению сгибания. В дальнейшем это предотвратит падения.
Для определения оптимальных видов лечения необходимы дальнейшие исследования взаимосвязи модуляции рефлекса и локомоции.
После поражения центрального отдела (головного мозга или спинного мозга) возникает глубокое растормаживание коротко-латентных рефлексов растяжения и потеря прибретенных двигательных рефлексов. Эти изменения связаны с двумя формами адаптации: развитие спастического тонуса мышц и пластичности спинальных и сенсорно-моторных центров ЦНС. В литературе появляется все больше доказательств, что в нейрореабилигации после инсульта основное внимание должно уделяться восстановлению функций и силы. Смысл этого подхода в том, что при восстановлении функции (т.е. повторном научении) вероятно, вследствие пластических изменений остальных сенсорно-моторных центров, спастичность будет уменьшаться. Контролируемые клинические исследования новых нейростимуляторов и данные реабилитации подтверждают улучшение функций и качества жизни.
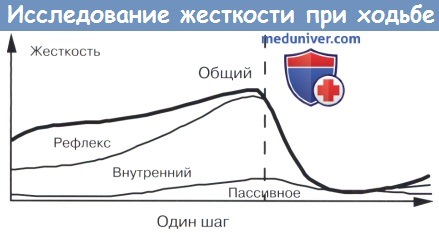
Внутренняя жесткость связана с центральной иннервацией мышц. При спастичности пассивная жесткость увеличена на всем протяжении цикла шага (не показано).
Рефлекторная жесткость при статической нагрузке будет нормальной.
Во время ходьбы рефлекс растяжения у здоровых пациентов значительно подавлен, но при спастичности это происходит за счет уменьшения порога рефлекса растяжения.
При сгибании во время ходьбы активируется рефлекс растяжения и напряжение голеностопного сустава. 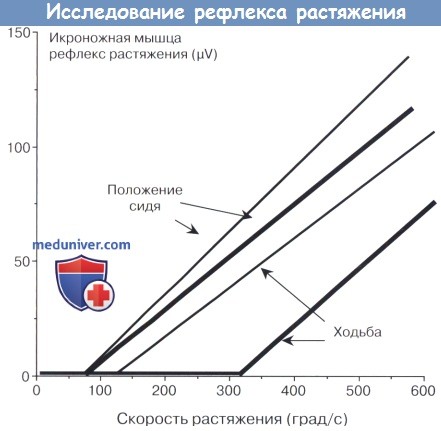
На ранней стадии ходьбы и в положении сидя, при ЭМГ передней порции большеберцовой мышцы у пациентов со спастичностью
и у здоровых испытуемых показана приблизительно одинаковая скорость растяжения лодыжки по сравнению с амплитудой камбаловидного рефлекса растяжения.
Никаких изменений в кривой не было найдено между пациентами и контрольной группой, в то время как порог рефлекса в контрольной группе во время ходьбы был значительно увеличен.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021