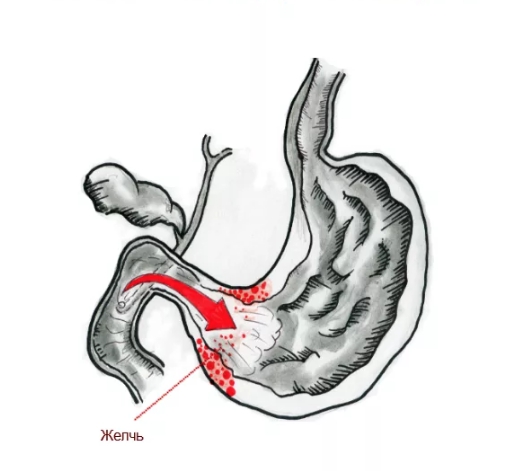
Актуальность проблемы
Дуодено-гастральный рефлюкс (ДГР) — одна из самых распространенных патологий верхних отделов желудочно-кишечного тракта, по данным разных источников, данное нарушение занимает 50-90% от всех заболеваний ЖКТ. Более того, за последние годы прослеживается рост количества заболевших. У пациентов с дуоденогастральным рефлюксом нередко также диагностируется хронический гастрит, в том числе рефлюкс-гастрит типа С, щелочной гастрит, язвенная болезнь желудка, функциональная диспепсия, грыжа пищеводного отверстия диафрагмы и ГЭРБ, пищевод Барретта, дуоденостаз, дисфункция сфинктера Одди, постхолецистэктомический синдром, рак желудка и целый ряд других заболеваний.
Следует знать, что ДГР способен привести к тяжелому гастриту и эзофагиту, стать причиной метаплазии желудка и пищевода, а также плоскоклеточного рака пищевода, который развивается на фоне метаплазии; это подтверждено клиническими исследованиями.
Таким образом, в результате патологического рефлюкса дуоденального содержимого в желудок течение многих органических и функциональных патологий ЖКТ может осложняться. Поэтому огромное значение должно уделяться своевременной диагностике, правильной клинической интерпретации и адекватной медикаментозной терапии.
При неэффективности консервативной коррекции показано хирургическое вмешательство, целью которого является укрепление пилорического жома, а также снижение количества забрасываемой желчи в желудок.
Есть данные о том, что на фоне ДГР желудка часто развиваются симптомы поражения системы дыхания, появляется синдром боли в грудной клетке, который не связан с коронарной патологией. Кроме того, у некоторых пациентов дуоденогастральный рефлюкс может вызвать рецидивирующий катаральный фарингит и пароксизмальный ларингоспазм. Однако у трети больных диагностируется «чистый» дуодено-гастральный рефлюкс, в этом случае можно говорить об изолированном диагнозе.
Причины дуодено-гастрального рефлюкса
Патогенетический механизм развития осложнений при ДГР
Желчь в составе рефлюксата при патологическом дуодено-гастральном рефлюксе ретроградно поступает из ДПК в органы, расположенные выше — желудок с пищеводом. Желчные кислоты, трипсин, лизолецитин — составляющие дуоденального содержимого — повреждают слизистую оболочку. Наиболее агрессивным действием при забросе дуоденального содержимого обладают желчные кислоты. Сегодня уже доказано, что при кислом рН среды лизолецитин и конъюгированные желчные кислоты (прежде всего тауриновые конъюгаты) сильнее повреждают слизистую желудка и пищевода, что определяет синергизм этих компонентов с соляной кислотой в развитии эзофагита и гастрита.
Неконъюгированные желчные кислоты и трипсин обладают более токсичным действием при слабощелочном и нейтральном рН, повреждающий эффект при дуодено-гастральном рефлюксе увеличивается при медикаментозном подавлении кислого рефлюкса. Их токсичность большей частью вызвана ионизированной формой, благодаря чему кислоты легко проникают через слизистую пищевода и желудка. Исходя из этого вполне объяснимо отсутствие адекватного ответа у 15-20% пациентов при монотерапии антисекреторными препаратами, если не будет учтен имеющийся дуодено-гастральный рефлюкс.
В результате действия на слизистую желудка желчных кислот, содержащихся в желчи, в течение длительного времени возникают изменения поверхностного эпителия желудка дистрофического и некробиотического характера, что ведет к развитию рефлюксгастрита — гастрита С. При имеющейся инфекции Нelicobacter pylori повреждающее действие рефлюксата на слизистую желудка возрастает. При наличии ДГР происходит заброс агрессивного содержимого в вышележащие отделы, что становится причиной нарушений в работе пищеварительной системы, воздействию подвергается мембранное и полостное пищеварение, возможность всасывания пищевых ингредиентов с микроэлементами и витаминами, изменяется водный баланс.
Признаком негативного воздействия ДГР являются признаки атрофии, метаплазии и дисплазии, это представляет опасность из-за риска развития рака желудка или пищевода. Кроме того, желчь в сочетании с панкреатическим соком из-за своей агрессивности разрушающе действует на слизистый барьер в желудке, при этом обратная диффузия водородных ионов усиливается. В результате этих процессов возникают эрозивные и язвенные поражения слизистой оболочки желудка.
Клинические проявления и диагностика дуодено-гастрального рефлюкса
Для ДГР характерно преобладание диспептических проявлений, пациента беспокоит отрыжка кислым содержимым или воздухом, изжога, тошнота, возможна рвота желчью, также появляется горечь во рту, которая не исчезает и даже усиливается при приеме ингибиторов протонной помпы.
Периодические боли в животе чаще схваткообразного характера, они могут возникать вследствие стресса или физической нагрузки.
Чаще дуоденогастральный рефлюкс сочетается с другими заболеваниями ЖКТ, в первую очередь с язвой желудка и ДПК, ГПОД, хроническим холециститом, панкреатитом и др. Соответственно, это отражается на симптоматике рефлюкса, существенно ее маскируя. В «чистом» виде ДГР появляется не так часто.
Дуодено-гастральный рефлюкс, в отличие от «классического» — желудочно-пищеводного рефлюкса кислой природы с изжогой, дисфагией и регургитацией — сопровождается не столь яркими клиническими проявлениями, но чаще проявляются признаки диспепсии. Кроме того, больных беспокоит боль в эпигастральной области, которая становится сильнее после приема пищи.
Диагностика основывается на результатах инструментальных методов обследования.
Лечение дуодено-гастрального рефлюкса
Консервативное лечение ДГР желудка отличается сложностью, целью терапии является нейтрализация агрессивного воздействия дуоденального содержимого на слизистую желудка и пищевода. Также в задачи лечения входит нормализация пропульсивной способности пищеварительного тракта. Назначения включают прокинетики, антациды, сорбенты, препараты урсодезоксихолевой кислоты (УДХК). При желчном рефлюксе терапия сочетается с базисным лечением основного заболевания. При этом огромное значение уделяется соблюдению диеты.
Медикаменты, используемые для устранения ДГР и восстановления моторики ЖКТ:
Следует учесть, что эритромицин в качестве прокинетика не рекомендован из-за побочных эффектов, цизаприд — не показан в клинической практике из-за вероятности нарушения сердечной проводимости, тегасерод — увеличивает вероятность инфаркта миокарда.
Фармакологическое действие домперидона (D2 антагонист) и метоклопрамида (5 НТ4 агонист и D2 антагонист) связано с блокадой рецепторов дофамина, антагонисты которых вызывают повышение тонуса нижнего сфинктера пищевода, увеличивают сократительную функцию желудка, а также препятствуют релаксации. Кроме того, благодаря антагонистам дофаминовых рецепторов улучшаются эвакуаторная способность желудка и антродуоденальная координация, что способствует устранению дуодено-гастрального рефлюкса.
Важно учесть, что клинические проявления рефлюкса с использованием медикаментозных препаратов уменьшаются, однако носят симптоматический характер. Добиться хороших результатов можно только при функциональных нарушениях, которые привели к ДГР. В остальных случаях консервативная терапия должна сочетаться с хирургическим лечением, способным устранить причину рефлюкса и укрепить пилорический клапан.
Хирургическое лечение дуодено-гастрального рефлюкса
При неэффективности консервативной терапии рекомендовано оперативное лечение, операция при этом проводится в нескольких направлениях:
При всех вышеперечисленных методиках используется лапароскопический доступ — через несколько (3-4) проколов на брюшной стенке.
Техника лапароскопической пилоропликации для уменьшения дуодено-гастрального рефлюкса
Прежде всего проводится ревизия пилородуодальной зоны, и оценивается выраженность спаечного процесса в зоне луковицы ДПК и привратника. Затем необходимо осмотреть связку Трейца, в случае необходимости она пересекается, тем самым улучшается прохождение пищи по двенадцатиперстной кишке. После ее мобилизации по Кохеру, что сделает ее более подвижной и снизит напряжение, накладываются швы в области привратника, что служит для профилактики несостоятельности.
Для пилоропликации поочередно накладываются серозно-мышечные швы симметрично к осе привратника, благодаря подобной методике передняя стенка луковицы ДПК сдвигается в проксимальном направлении, передняя полуокружность привратника погружается в просвет луковицы ДПК. Обычно четырех швов достаточно. Созданный антирефлюксный механизм способен препятствовать ДГР, не нарушая при этом эвакуации из желудка.
При необходимости проводится коррекция ГПОД или выполняется вмешательство на билиарном тракте. Следует помнить, что при лапароскопии возможно выполнение нескольких симультанных операций при наличии патологий в брюшной полости, малого таза или в забрюшинном пространстве, требующих оперативного лечения (киста почки, яичника, нефроптоз, миома и др.).
К настоящему времени нашими специалистами проведено более чем 600 оперативных вмешательств по поводу ГПОД и рефлюкс-эзофагита, а также связанных с хроническим нарушением дуоденальной проходимости. Накопленный опыт обобщен в 4-х монографиях: «Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии», «Грыжи пищеводного отверстия диафрагмы», «Ручной шов в эндоскопической хирургии» и «Технология дозированного лигирующего– электротермического воздействия на этапах лапароскопий». Кроме того, информация опубликована в многочисленных научных публикациях в разных профессиональных рецензируемых научных изданиях — российских и зарубежных.
После вмешательства на коже живота останется лишь несколько разрезов, длина которых не превышает 10 мм. Уже в день операции пациенты могут вставать, разрешается пить, на следующий день можно принимать теплую пищу в жидком виде. Клинику можно покинуть на 1-3 день — возможность выписки зависит от тяжести состояния. Но уже спустя 2-3 недели человек может вернуться к привычному образу жизни. Соблюдение строгой диеты необходимо в ближайшие два месяца, более мягкая разрешена через полгода после вмешательства. В дальнейшем человек, перенесший операцию, может обходится без медикаментов и не нуждается в строгом соблюдении диеты.
По желанию наши пациенты могут перед оперативным лечением пройти полное обследование, по результатам которого будет подобрана оптимальная тактика лечения и метод хирургического вмешательства.
На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное — свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие. Каждый день я по нескольку часов отвечаю на ваши письма. Направляя мне письмо с вопросом, вы можете быть уверены, что я внимательно изучу вашу ситуацию, при необходимости запрошу дополнительные медицинские документы. Огромный клинический опыт и десятки тысяч успешных операций помогут мне разобраться в вашей проблеме даже на расстоянии.
Многим пациентам требуется не хирургическая помощь, а правильно подобранное консервативное лечение, в то время как другие нуждаются в срочной операции. И в том, и в другом случае я намечаю тактику действий и при необходимости порекомендую прохождение дополнительных обследований или неотложную госпитализацию. Важно помнить, что некоторым больным для успешной операции требуется предварительное лечение сопутствующих заболеваний и правильная предоперационная подготовка.
В письме обязательно (!) укажите возраст, основные жалобы, место проживания, контактный телефон и адрес электронной почты для прямой связи. Чтобы я мог детально ответить на все ваши вопросы, прошу высылать вместе с вашим запросом сканированные заключения УЗИ, КТ, МРТ и консультаций других специалистов. После изучения вашего случая, я направлю вам либо подробный ответ, либо письмо с дополнительными вопросами.
В любом случае я постараюсь вам помочь и оправдать ваше доверие, которое является для меня наивысшей ценностью.
Дисфункция сфинктера Одди. Клинический случай
Резюме. В статье представлено определение и частота выявления дисфункций сфинктера Одди у пациентов с разной патологией желчевыводящей системы. Рассматриваются особенности дисфункции сфинктера Одди с учетом его анатомического строения. На основании материалов Римских критериев IV (2016) приведены современные подходы к диагностике и лечению дисфункции сфинктера Одди. Привлечено внимание к диагностическим критериям дисфункции сфинктера Одди по билиарному и панкреатическому типам. Даны схемы обследования и лечения пациентов с дисфункциями сфинктера Одди в зависимости от тяжести заболевания и объективных данных лабораторных и инструментальных исследований. Разобран клинический случай пациента с дисфункцией сфинктера Одди. В зависимости от особенностей клинического течения дисфункции была предложена тактика ведения пациента с применением препарата селективного спазмолитического действия и препарата с желчегонным действием.
Ключевые слова: желчевыводящая система, функциональные заболевания, сфинктер Одди, Римские критерии, дисфункция сфинктера Одди, сфинктеротомия, селективные спазмолитики.
Sphincter of Oddi dysfunction. Case history
Tatyana E. Polunina. Dr. of Sci. (Med.), Professor of Chair for Propaedeutics of Internal Diseases and Gastroenterology, Federal State Budgetary Educational Institution of Higher Education «Evdokimov Moscow State University of Medicine and Dentistry» of the Ministry of Healthcare of the Russian Federation.
Summary. The article presents the definition and prevalence of sphincter of Oddi dysfunction in patients with various disorders of the biliary system. It describes the characteristics of sphincter of Oddi dysfunction with due account of its anatomical structure. Based on Rome IV Criteria (2016), the authors provide modern approaches to the diagnosis and treatment of sphincter of Oddi dysfunction. Special attention is paid to the diagnostic criteria for sphincter of Oddi dysfunction depending on its type. There are two basic types of sphincter of Oddi dysfunction: biliary dysfunction and pancreatitis. The paper presents the algorithms for the examination and treatment of patients with sphincter of Oddi dysfunction depending on the severity level of the disease and objective findings of laboratory and instrumental tests. The article presents a clinical history of a patient with sphincter of Oddi dysfunction. Depending on the characteristics of a clinical course of dysfunction, it was proposed that the patient was treated with a selective antispasmodic drug and a choleretic drug.
Keywords: biliary system, functional diseases, sphincter of Oddi, Roman criteria, sphincter of Oddi dysfunction, sphincterotomy, selective antispasmodics.
Заболевания желчевыводящей системы (дисфункция желчного пузыря, дисфункция сфинктера Одди (СО), хронический акалькулезный холецистит, хронический калькулезный холецистит, желчнокаменная болезнь (ЖКБ), синдром постхолецистэктомии) являются распространенными заболеваниями органов пищеварения. На фоне участившихся случаев обращаемости пациентов с патологией желчевыводящей системы отмечается увеличение доли функциональной патологии желчного пузыря (ЖП) и (СО) до 15% от всех заболеваний желчевыводящей системы [1]. Дисфункция сфинктера Одди (ДСО) определяется как доброкачественное, некалькулезное обструктивное расстройство [2, 3]. Распространенность ДСО составляет 1,5% в общей популяции и может достигать 72% у пациентов с идиопатическим рецидивирующим панкреатитом. ДСО встречается у взрослых и детей любого возраста, но чаще всего — у женщин в возрасте 20–50 лет [4]. Однако его истинную распространенность трудно определить из-за отсутствия точных биомаркеров и стандартных диагностических критериев, а также множества вторичных причин ДСО, таких как фиброз сфинктерного канала (папиллярный стеноз и склерозирующий папиллит) или обструктивная карцинома. Ранняя диагностика и лечение ДСО имеют большое клиническое значение из-за возможности трансформации функциональных нарушений в органическую патологию желчевыводящей системы — в хронический холецистит и ЖКБ.
Анатомия СО
СО — это мышечная структура, окружающая слияние дистального общего желчного протока и протока поджелудочной железы (ПЖ) в ампулу Ватера (рис. 1). Структура сфинктера с выступающей в 12-перстную кишку слизистой оболочкой называется сосочком Ватера. Функции СО: регулирование потока желчи в 12-перстную кишку; предотвращение дуоденального рефлюкса; регуляция наполнения ЖП путем отведения желчи в ЖП с закрытием СО. Мышечные волокна СО окружают интрадуоденальный сегмент общего желчного протока и ампулу Ватера. Кольцевидное расположение мышечных волокон, известное как сфинктер холедоха (или сфинктер Бойдена), регулирует ток желчи в 12-перстную кишку таким образом, что позволяет заполнить ЖП во время голодания и предотвращает ретроградный рефлюкс содержимого 12-перстной кишки в желчный проток. Отдельная структура, называемая сфинктером панкреатического протока, охватывает дистальный проток ПЖ. Мышечные волокна сфинктера ПЖ переплетены с мышечными волокнами сфинктера холедоха в виде восьмерки [4].
ДСО характеризуется частичным нарушением проходимости протоков на уровне сфинктера и может иметь как органическую (стеноз), так и функциональную природу (нарушение двигательной активности, тонуса сфинктеров билиарного протока и/или панкреатического протока) (рис. 2). Клинически ДСО проявляется нарушением оттока желчи и панкреатического сока в просвет 12-перстной кишки.
Стеноз СО является аномалией с частичным или полным сужением сфинктера вследствие хронического воспаления и фиброза. Основными условиями развития стеноза являются: холедохолитиаз, панкреатит, травматические или хирургические вмешательства в брюшную полость, неспецифические воспалительные заболевания кишечника и, редко, юкстапапиллярный дивертикул 12-перстной кишки. Дисфункция СО может привести к желчным коликам. До одной трети больных с необъяснимой желчной коликой, особенно после холецистэктомии, с неизмененными внепеченочными билиарными протоками и протоками ПЖ, имеют манометрические доказанные ДСО. Этот тип дисфункции вызван реакцией холецистокинина (ХЦК), приводящей к повышению базального давления или увеличению амплитуды и частоты сокращений. В основе гипертонуса СО чаще всего лежат психогенные воздействия (стрессы, эмоциональные перенапряжения), реализуемые через повышение тонуса блуждающего нерва.
Рисунок 1. Анатомия сфинктера Одди
Рисунок 2. Нарушение двигательной активности СО: А – гипотонус (расслабление), В – гипертонус (спазм). Адаптировано из [5]
Клинические проявления ДСО:
Болевой синдром часто сопровождается проявлениями билиарной диспепсии (горечь во рту, отрыжка, чувство быстрого насыщения, тяжесть и боль в эпигастрии, тошнота и эпизодическая рвота, приносящая облегчение), а также кишечной дисфункции в виде неустойчивого стула. Нередко встречается астеновегетативный синдром (раздражительность, повышенная утомляемость, головная боль, повышенная потливость).
В Римских критериях IV 2016 г. (в дальнейшем Консенсус IV) предлагается разделять ДСО на дисфункцию билиарного и панкреатического сфинктеров (ДБСО и ДПСО) соответственно [6].
Дисфункция билиарного СО
ДБСО обычно рассматривается у пациентов с болями билиарного типа, в т. ч. с болями после холецистэктомии, когда камни и другая патология исключены.
Классическое представление о патогенезе ДБСО заключается в том, что патологические изменения в сфинктере приводят к уменьшению оттока желчи и последующему повышению давления в билиарном отделе СО, которое вызывает билиарную боль в эпигастральной области и правом подреберье с иррадиацией в правую лопатку. Однако теоретические и экспериментальные данные указывают на более сложную патофизиологию, которая подлежит дальнейшему изучению [6].
Основные диагностические критерии для ДБСО:
Дисфункция панкреатического СО
ДПСО может вызвать панкреатические боли и панкреатит. Панкреатическая боль обычно проявляется в левом подреберье с иррадиацией в спину. Конкременты в сфинктере вызывают панкреатит в таких клинических ситуациях, как опухоли сосочка, камни в протоке и муцинозно-кистозные новообразования. Кроме того, опиаты также усиливают давление сфинктера и вызывают приступы панкреатита. Наконец, у пациентов с необъяснимыми приступами панкреатита часто оказывается повышенным давление сфинктера ПЖ [6]. Доказательством того, что повышенное давление сфинктера вызывает панкреатит, может быть аномальная активность сфинктера и разрешение приступов болей после сфинктеротомии. Однако в ряде случаев отсутствовала положительная динамика клинических признаков при проведении панкреатической и билиарной сфинктеротомии [6]. Эти результаты говорят о том, что целесообразность проведения сфинктеротомии требует оценки результатов мониторирования клинических проявлений в динамике. Остается возможным то, что обнаружение аномалии сфинктера у этих пациентов является побочным эффектом, результатом предыдущих неуточненных воздействий. Тот факт, что у многих пациентов в конечном итоге развиваются признаки хронического панкреатита, указывает на то, что основной патогенез заболевания не изменился.
ДПСО может подозреваться у пациентов с документированным острым рецидивирующим панкреатитом после всесторонней оценки реальных причин и поиска аномалий развития при повышенном панкреатическом давлении, подтвержденном манометрией.
Основные диагностические критерии для ДПСО:
С учетом различий в клинической картине пациентов с ДСО классифицируют на три категории:
На рисунке 3 предлагается алгоритм обследования пациентов с постхолецистэктомической билиарной болью.
Рисунок 3. Алгоритм обследования пациентов с постхолецистэктомической билиарной болью. Адаптировано из [6]
Первоначальный диагностический подход должен включать тщательный анамнез и физикальное обследование, за которым следуют стандартные биохимические анализы печеночных и панкреатических ферментов, ЭГДС и ЭУЗИ внутренних органов.
Пациентам с доказанной билиарной непроходимостью должна быть назначена билиарная сфинктеротомия. Если уровень доказательств недостаточен, то проводятся дальнейшие исследования с манометрией и сцинтиграфией.
В настоящее время наиболее достоверным методом изучения функции СО является эндоскопическая манометрия СО. При этом возможно раздельное канюлирование билиарного сфинктера и панкреатического сфинктера с проведением манометрии, что позволяет выделить преимущественно билиарный или панкреатический тип расстройств, а также установить этиологию рецидивирующих панкреатитов у больных, перенесших холецистэктомию и папиллотомию. Признаками ДСО являются: повышение базального давления в просвете сфинктеров (выше 30–40 мм рт. ст.), повышение амплитуды и частоты фазовых сокращений (тахиоддия); увеличение частоты ретроградных сокращений. Следует учитывать, что длительно существующие функциональные расстройства в желчевыводящей системе могут приводить в дальнейшем к гипокинезии ЖП с застоем желчи, нарушению ее коллоидной стабильности и камнеобразованию, т. е. к формированию ЖКБ. Кроме того, застой желчи в ЖП на фоне ДСО может способствовать присоединению инфекции, т. е. приводить к возникновению холецистита. Следующим важным моментом является предрасположенность к синдрому холестаза. Так, длительно существующий спазм СО может приводить к проявлениям холестаза, вторичному поражению печени (холестатический гепатит, вторичный билиарный цирроз).
Подход к лечению пациентов с ДСО должен основываться на анализе истории заболевания и объективных данных лабораторных и инструментальных исследований (рис. 4) [7].
Медикаментозное лечение заболеваний желчевыводящей системы назначается, как правило, в фазе обострения процесса, связанного с присоединением инфекции. Из антибиотиков рекомендуется назначать препараты широкого спектра действия, которые поступают в желчь в достаточно высокой концентрации. При недостатке желчи или изменениях ее выделения снижается секреция ферментов самой желчи и ферментов ПЖ, что приводит к нарушению процесса пищеварения в 12-перстной кишке. Для коррекции ДСО применяются лекарственные препараты, нормализующие моторику СО и ЖП. С этой целью могут использоваться холеретики, к числу которых относятся препараты, содержащие желчь или желчные кислоты; синтетические препараты, некоторые фитопрепараты, а также холекинетики. Выбор препарата является очень важным, если не главным вопросом. Он, в частности, зависит от требуемой скорости получения эффекта. Если эффект должен быть быстрым, то лучше использовать холекинетики (значение имеет и доза препарата), а если необходимо длительное курсовое лечение, то предпочтение следует отдавать желчесодержащим препаратам. В случаях, когда одновременно требуется обеспечить противовоспалительный эффект, выбор должен быть сделан в пользу синтетических препаратов, но курсовое лечение ими не должно быть продолжительным.
Рисунок 4. Алгоритм лечения ДСО
Рисунок 5. Механизм действия селективного спазмолитика Гимекромон
В терапии ДСО могут использоваться препараты с прокинетическим действием, селективные блокаторы кальциевых каналов и миотропные спазмолитики. При выборе спазмолитика преимущество стоит отдавать препаратам с селективным действием в отношении билиарного тракта. Важное место в лечении ДСО занимают препараты, способствующие растворению билиарного сладжа и холестериновых желчных камней. К таким препаратам относится урсодезоксихолевая кислота, которая оказывает воздействие как минимум на 3 звена формирования дисфункций СО и ЖП: уменьшает синтез холестерина в гепатоцитах, повышает экскрецию холестерина с желчью, восстанавливает сократительную функцию ЖП [8].
Перспективным средством, применяемым в терапии ДСО, является Гимекромон (Одестон) — селективный холеспазмолитик с комбинированным эффектом действия, восстанавливающим большую часть расстроенных патогенетических механизмов (рис. 5). Он оказывает избирательное спазмолитическое действие на СО и сфинктер ЖП, а также обладает холеретическим эффектом. Сочетая спазмолитические и желчегонные свойства, Гимекромон обеспечивает гармоничное опорожнение внутри- и внепеченочных желчных путей, своевременное и беспрепятственное поступление желчи в 12-перстную кишку. Гимекромон, облегчая приток желчи в пищеварительный тракт, усиливает энтерогепатическую рециркуляцию желчных кислот, которые участвуют в первой фазе образования желчи. Преимущество Гимекромона перед другими спазмолитиками заключается в том, что он практически не оказывает влияния на гладкие мышцы сердечнососудистой системы и кишечника [9–11].
Гимекромон расслабляет СО, поэтому, в отличие от многих желчегонных средств, не повышает давление в желчных путях и в результате, что очень важно, не провоцирует желчную колику. Увеличивая поступление желчи в просвет кишечника, Одестон способствует улучшению пищеварения (ликвидации легкой и средней степени хронической билиарной недостаточности) и активирует перистальтику кишечника, что приводит к нормализации стула.
Гимекромон эффективен у больных с дисфункцией билиарного тракта, обладает желчегонным эффектом, устраняет билиарную недостаточность, ДСО, в т. ч. после холецистэктомии.
По рекомендациям Консенсуса IV у пациентов с доказанной обструкцией СО следует проводить эндоскопическую сфинктеротомию без проведения манометрии. Исследование EPISOD показало, что нет достаточных причин для выполнения манометрии или сфинктеротомии у пациентов с нормальными результатами лабораторноинструментальных исследований [6, 12]. Необхо димы достаточно весомые предикторы для сфинктеротомии у пациентов с предполагаемым функциональным расстройством СО билиарного типа. Freeman et al. [13] показали, что при нормальных результатах манометрии СО проведение эндоскопической сфинктеротомии неэффективно.
В настоящее время практикующие врачи и пациенты должны относиться к инвазивным методам лечения с большой осторожностью, признавая краткосрочные и долгосрочные риски и очень веские доказательства в их пользу.
Клинический случай
Пациентка Е., 50 лет. Жалобы: чувство тяжести в правом подреберье, боль спастического характера в правом подреберье и эпигастрии, горечь во рту, тошнота, тенденция к запорам.
В 2017 г. проведена холецистэктомия по поводу ЖКБ. Настоящее ухудшение самочувствия в течение 6 мес., участились эпизоды тошноты и рвоты желчью. Пациентка на протяжении 15 лет принимает гормональные контрацептивы.
Данные осмотра: правильное телосложение, признаки повышенного питания, кожные покровы — розовые, чистые, рост — 153 см, вес — 79 кг. ИМТ — 33,75.
Со стороны органов дыхания, кровообращения — без отклонений от нормы, АД — 130/80 мм рт. ст., ЧСС — 68 в 1 мин.
Язык обложен желтым налетом, живот мягкий, слегка болезненный при пальпации в подложечной области и правом подреберье, симптом Кера и симптом Василенко положительные.
Печень — 12—10—9 см по Курлову, селезенка перкуторно — 8×6 см.
Стул нерегулярный, тенденция к запорам. БК тип 5.
План обследования для исключения органической патологии:
В клиническом анализе крови: гемоглобин — 148,8 г/л, эритроциты — 4,86×1012/л, гематокрит — 43,9%, ЦП — 0,91, лейкоциты — 6,58×109/л, нейтрофилы — 47%, тромбоциты — 172×109/л, эозинофилы — 4,48%, лимфоциты — 36%, моноциты — 10,6%, СОЭ — 7 мм/ч.
В биохимическом анализе крови: общий белок — 8,4 г/дл, альбумин — 4,5 г/дл, глюкоза — 97 мг/дл, креатинин — 1,0 мг/дл, общий холестерин — 7,5 Ммоль/л; АЛТ — 20 ед/л (42 ед/л ), АСТ — 23 ед/л (до 38 ед/л); ГГТП — 67 ед/л (5–50 ед/л); щелочная фосфатаза — 172 ед/л (32–92 ед/л), уровни панкреатической амилазы и липазы — в пределах нормы, С-реактивный белок — норма.
Анализ мочи: диастаза в пределах нормы.
Анализ кала: умеренная стеато-, креаторея.
УЗИ брюшной полости: жировая инфильтрация печени и липоматоз ПЖ. Желчный пузырь удален. Растянутый общий билиарный проток.
ЭГДС с досмотром постбульбарного отдела: в просвете желудка и 12-перстной кишки желчь (рис. 6а). Просвет постбульбарных отделов широкий, складки циркулярные, слизистая без явлений атрофии и инфильтрации. Сфинктер Одди плоско-холмовидной формы, размерами до 0,4 см (рис. 6б), расположен по нижнему краю крупного дивертикула диаметром до 2,0–2,5 см (рис. 6в).
Диагноз: ЖКБ. Постхолецистэктомный синдром. Холецистэктомия в 2017 г
Спазм сфинктера Одди. Дуоденогастральный рефлюкс. Катаральный бульбит. Перипапиллярный дивертикул 12-перстной кишки. Жировая инфильтрация печени.
Диета. Стол № 5. Разгрузочная диета – 1200 ккал/д, физические нагрузки.
Гимекромон (Одестон) 400 мг 3 р/сут за 30 мин до еды 1 мес.; УДХК 1000 мг/сут после еды 1 мес.
Мониторирование печеночного профиля на 2-й и 4-й нед. терапии и в дальнейшем 1 раз в 3 мес.
ЭГДС с досмотром постбульбарного отдела через 1 мес.
В результате 1 мес. лечения: купированы болевой синдром, диспепсические явления и запоры. Отмечена стабильная положительная динамика печеночного, липидного спектра и показателей копрологии.
По результатам ЭГДС: в просвете желудка и 12-перстной кишки желчь не наблюдается, СО желудка и 12-перстной кишки розовая, перипапиллярный дивертикул 12-перстной кишки.
Таким образом, при ДСО применяют спазмолитические препараты, различающиеся по механизму действия. К основным проблемам такого подхода к лечению следует отнести возможность влияния спазмолитиков на гладкомышечные клетки не только билиарного тракта, но и других систем и органов, что в ряде случаев становится причиной развития нежелательных явлений и существенно лимитирует применение таких препаратов у отдельных категорий больных. Одним из актуальных вопросов терапии ДСО становится поиск лекарственных средств, обладающих наиболее физиологичным механизмом коррекции существующих нарушений и имеющих минимальное количество нежелательных явлений.
Рисунок 6. ЭГДС с досмотром постбульбарного отдела