Что такое токсокароз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
Токсокароз — зоонозный гельминтоз с фекально-оральным механизмом передачи, протекающий у человека исключительно в форме тканевого паразитирования личиночной стадии паразита (биологический тупик), проявляющийся в форме токсико-аллергических реакций различной степени выраженности и полиорганных поражений в зависимости от численности и локализации паразитов. Имеет склонность к длительному рецидивирующему течению.
Этиология
Тип — Nemathelmintes (круглые черви)
Класс — Nematoda (собственно круглые черви/нематоды)
Род — Toxocara (от греч. toxon — стрела, cara — голова)
Виды — Toxocara canis (поражает человека и животных семейства псовых), Toxocara mistax (поражает животных семейства кошачьих), Toxocara vitulorum (поражает крупный рогатый скот), Toxocara leonina (возникает у львов).
В патологии человека основная роль принадлежит Toxocara canis, роль остальных видов дискутабельна — они способны поражать людей с дефектами иммунной системы, в остальных случаях чаще всего наблюдается спонтанное выздоровление без каких-либо значимых клинических проявлений.
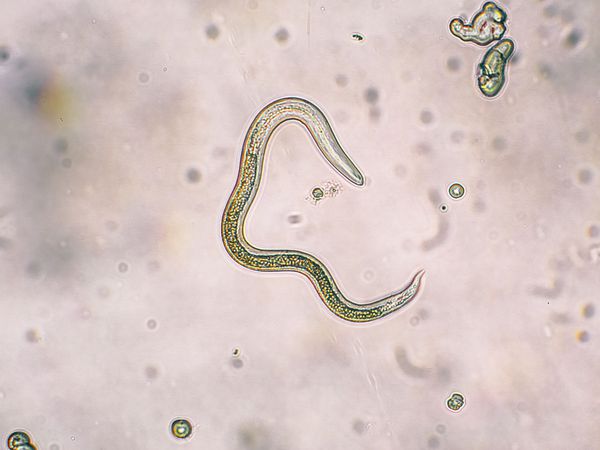
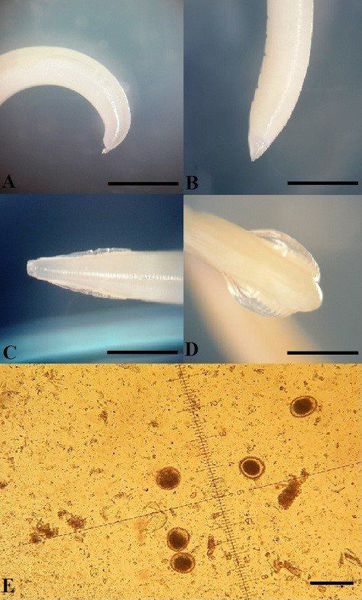
Взрослые половозрелые токсокары — это раздельнополые достаточно крупные черви с заострёнными концами (имеют некоторое сходство с аскаридами человека). Кутикула светло-жёлтого цвета. Длина самки достигает 18 см (с прямым хвостом), в передней половине тела есть отверстие вульвы. Самцы вырастают до 10 см (с загнутым хвостовым концом и консусовидным придатком). Головной конец имеет вид широких крыльев (вздутия кутикулы размерами до 2,3×5×0,3 мм), что является внешним отличительным признаком. Есть расширенный пищевод (желудочек). Продолжительность жизни взрослых особей — до шести месяцев.
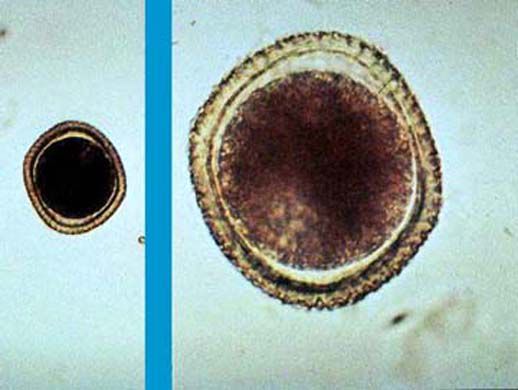
За сутки самка может откладывать свыше 200 тысяч яиц в кишечнике животного (собаки). Яйца имеют округлую форму, размерами 65-45 мкм, покрыты плотной бугристой оболочкой, коричневого цвета различных оттенков, прекрасно защищающей их от неблагоприятного воздействия внешней среды. Внутри яиц находятся тёмные бластомеры (зародыши). С калом незрелые яйца паразита (неинвазионные) попадают в окружающую среду (почву), где при благоприятных условиях (достаточная влажность — не ниже 70%, температура — не ниже 14°C и насыщение кислородом) происходит созревание яиц (в среднем около 2-3 недель) и образование в них инвазионной личинки, длительно сохраняющей свою жизнеспособность (до 3-5 лет). Яйца обладают высокой устойчивостью к действию агрессивных условий внешней среды, длительно выживают даже под воздействием ядов (таких, как медный купорос, сулема и другие).
У животных токсокары паразитируют в тонком кишечнике до 6 месяцев, питаясь содержимым кишечника (инвазированность может достигать несколько сотен гельминтов).
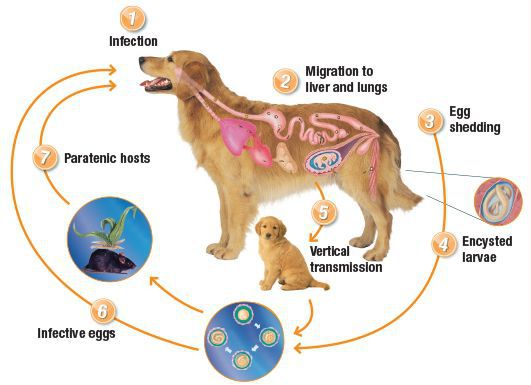
В жизни паразита у животного выделяют несколько различных путей развития. Основной происходит по аналогии с циклом развития аскарид при аскаридозе. Он протекает у молодых животных — щенков до двух месяцев. После заглатывания инвазионных яиц в тонкий кишечник собаки выходят личинки, которые, пробуравливая его стенку, попадают в систему воротной вены и, мигрируя по кровеносным сосудам, попадают в лёгочную капиллярную сеть. Большая часть личинок поднимаются по воздухоносным путям, они вновь заглатываются, попадая снова в тонкий кишечник. Там личинки растут и через пять недель от момента заражения начинают выделять яйца. Другая часть личинок у молодняка и в основном у взрослых животных проникает через стенку лёгочной вены в большой круг кровообращения, после чего разносится и оседает в самых разнообразных органах и тканях, где личинки образуют гранулематозные инфильтраты и пребывают в «спящем» состоянии в течении многих лет (соматические личинки).
У самок в период беременности на фоне гормональной и иммунологической перестройки организма дремлющие личинки возобновляют активность и, совершая миграцию, трансплацентарно инвазируют плод, т.е. новорождённый щенок уже оказывается инвазирован паразитом. Также возможна передача личинок с молоком при кормлении.
Имеет место заражение животного и при поедании факультативных хозяев (резервуарных, паратенических), инвазированных личинками — грызунов, скота, червей и других. По этой причине реализуются дополнительные варианты заражения.
Таким образом, источником распространения яиц паразита в окружающую среду в основном являются щенки, у которых наблюдается преимущественно гепатопульмональный вариант циркуляции возбудителя, а взрослые животные, как правило, являются лишь носителями личинок паразита в тканях даже при многократных заражениях за время жизни. [1] [4] [6] [8] [10]
Эпидемиология
Источником инвазии являются преимущественно собаки (щенки), с калом которых яйца паразита попадают в почву. Менее значимыми источниками являются другие представители псовых (лисы и волки).
Учитывая, что 1 гр фекалий собаки содержит до 15-30 тысяч яиц паразита, а распространённость собак и особенно их бездомных собратьев в последнее время крайне велика, степень загрязнённости яйцами токсокар окружающей нас среды огромна. Например, по самым скромным подсчётам, контаминация детских песочниц и газонов в Санкт-Петербурге — не менее 85%, что создаёт реальную угрозу инфицирования людей.
Механизм заражения — фекально-оральный.
Внутриутробная передача личинок от матери-плоду или через молоко у человека не доказана. Люди не являются источником распространения токсокар, так как в их организме черви существуют лишь в виде тканевых личинок и никогда не достигают половой зрелости (не паразитируют в кишечнике и не откладывают яиц), т.е. люди являются эволюционным тупиком в круговороте жизни данного вида паразита.
Определённую роль в распространении яиц паразита играют тараканы (могут поедать и выделять в жизнеспособном виде часть яиц) и мухи (как механические переносчики).
Восприимчивость — всеобщая. В реализации клинически выраженной формы заболевания играет роль количество попавших в организм яиц паразита и свойства иммунной системы. Наиболее часто заболевают дети (больше мальчики). [1] [5] [6] [8] [10]
Симптомы токсокароза
Клиническая симптоматика токсокароза не имеет специфичных симптомов. Она достаточно сходна с симптоматикой других тканевых гельминтозов в соответствующие фазы развития и выражается в виде синдромальных проявлений различной интенсивности и в разнообразных сочетаниях.
Широко распространено т.н. токсокароносительство — когда явные клинические признаки заболевания отсутствуют, и диагноз можно поставить лишь на основании обнаружения титра антител (обычно в низкой концентрации). Также распространена субклиническая инвазированность («скрытый токсокароз») — когда на фоне выявления антител к токсокарам в периферической крови появляется незначительная эозинофилия, клинические проявления не выявляются или не могут быть прямо связаны с токсокарами — температура 37,1-38,0°C, увеличение лимфоузлов, частые простудные заболевания, аллергизация и другое.
Следует выделять проявления висцерального (тканевого) и глазного токсокароза.
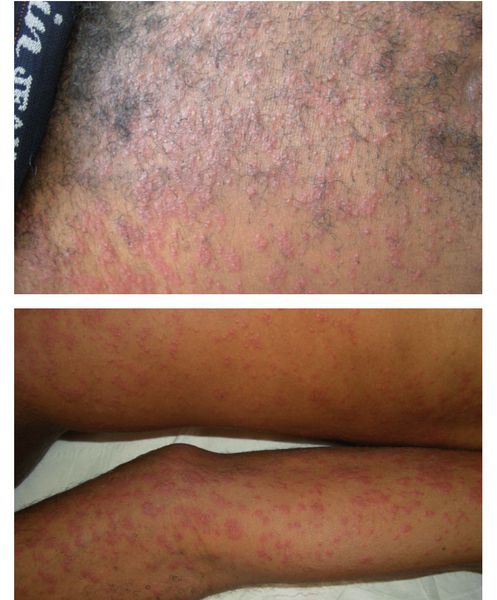
При висцеральной форме заболевания через 2-3 недели от момента заражения в острую фазу возникает повышение температуры до фебрильных цифр (38,0-39,0°C), слабость, головные боли, повышенная утомляемость, бессонница, полиморфные высыпания различных участков тела (в основном по типу крапивницы), иногда отёк Квинке, боли в мышцах, увеличение периферических лимфоузлов (умеренная болезненность), сухой кашель, нередко с обструктивным компонентом.
Детям при такой форме заболевания характерен синдром Леффлера (выраженный непроходящий кашель, гиперлейкоцитоз за счёт эозинофилии, летучие эозинофильные инфильтраты в лёгких), а также диффузные боли в животе и неустойчивый стул. Увеличиваются размеры печени и селезёнки, нарастает эозинофилия крови и гипергаммаглобулинемия (повышенная концентрация иммуноглобулинов в крови).
Как правило, проявления острой фазы продолжаются не более одного месяца и по мере улучшения общего самочувствия и стихания гиперэозинофилии купируются. Однако в некоторых случаях, особенно у детей, острая фаза приобретает затяжное течение с ярко выраженным лёгочным синдромом, проявляющимся в виде длительного мучительного кашля, обструкциями (непроходимость дыхательных путей) и ателектазами (спадение доли лёгкого), приступами удушья, нередко в дальнейшем с формированием гиперреактивности трахеобронхиального дерева (отличительная особенность — повышенная чувствительность к физиологическому раствору) и развитием бронхиальной астмы.
Чем раньше распознано заболевание и начата специфическая противопаразитарная терапия, тем больше шансов на быстрое купирование болезни, регресс бронхолёгочной симптоматики и снижение риска развития бронхиальной астмы. При длительно персистирующей инфекции и развитии астмы даже полное излечение от токсокароза не даёт существенного клинического эффекта, так как уже формируется патологический аутоиммунно-аллергический комплекс.
Возможно токсико-аллергическое поражение сердца, проявляющиеся учащённым сердцебиением, болями в области сердца, нарушением ритма, глухостью тонов при аускультации, колебаниями артериального давления и кардиомиопатией. Описан синдром Леффлера II — эозинофильный васкулит (воспаление стенок сосудов), пристеночный фибропластический эндокардит (воспаление внутренней оболочки сердца).
Возможно развитие поражения нервной системы в виде судорожного синдрома, нарушения психики, развития изолированного и/или сочетанного поражения отдельных нервов, менингитов и менингоэнцефалитов (повреждающее действие как личинок, так и токсико-аллергической интоксикации).
В хроническую фазу болезни при слабой выраженности общеинфекционной симптоматики проявления острого периода претерпевают значительную регрессию и приобретают характер преимущественно изолированных органных поражений — бронхиальная астма, миокардит, дерматит, гепатит, астеноневротический синдром нетипичного течения.
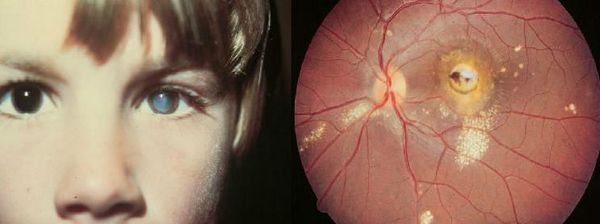
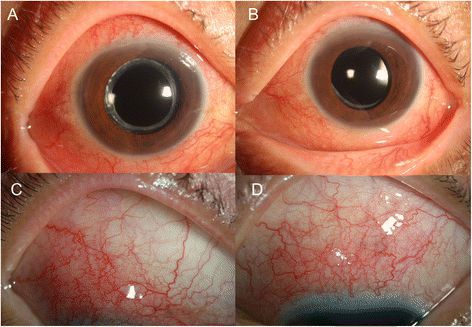
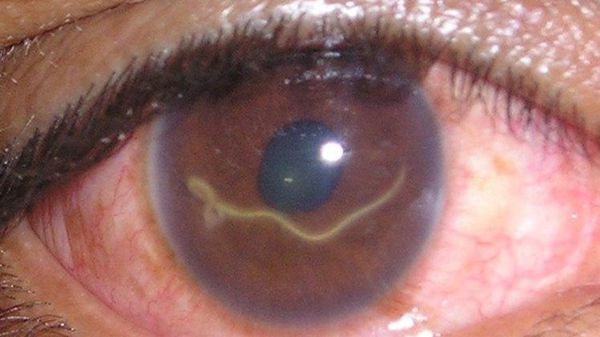
Глазной токсокароз проявляется обычно изолированным поражением одного глаза (без проявлений висцерального процесса). Он характеризуется в зависимости от локализации (задний гранулематозный хориоретинит, кератит, эндофтальмит, увеит, иридоциклит и другое) и может проявляться снижением остроты зрения, потерей части зрительной картинки, нарушением цвето- и световосприятия. Иногда возникает отёк параорбитальной области, гиперемия тканей и экзофтальм (выпучивание глаза). [1] [2] [6] [7] [9]
Патогенез токсокароза
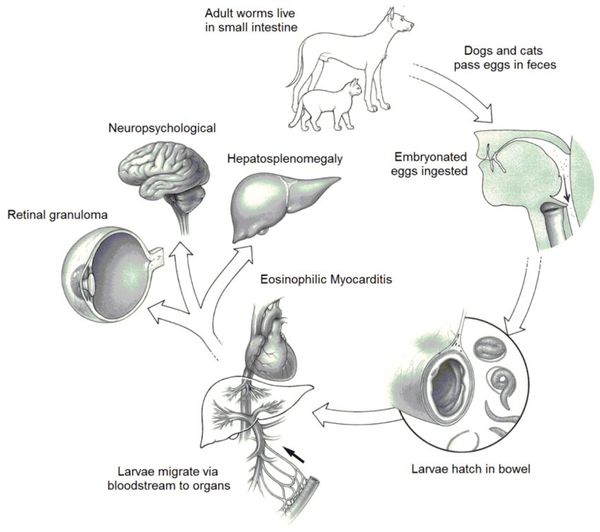
Входные ворота — ротовая полость. При проглатывании яиц токсокар они попадают в тонкий кишечник, где разрушается оболочка яйца, и живые личинки выходят в просвет кишки, пенетрируют (пробуравливают) стенку кишечника и с током крови через систему воротной вены попадают в печень. Там одна их часть задерживается (частично гибнет), окружается воспалительными инфильтратами с образованием паразитарных гранулём, а другая часть через печёночные вены попадает в правые отделы сердца, откуда проникает в лёгочную капиллярную сеть и разносится по большому кругу кровообращения, заселяя все возможные органы (кожу, мышцы, глаза, головной мозг, щитовидную железу и другие) и ткани (также оседая в них и формируя воспалительно-аллергические инфильтративные образования).
В этих органах, в зависимости от индивидуальных свойств иммунной системы и массивности заражения, личинки могут сохраняться десятилетиями, обуславливая весь комплекс патологических изменений. При значимом снижении иммунитета или влиянии неблагоприятных факторов не исключается повторная миграция.
В процессе миграции личинки паразита механически травмируют ткань человеческого организма, вызывая воспалительные реакции, геморрагии, некрозы.
Главное же воздействие на организм оказывают иммунопатологические реакции, связанные с выраженным аллергическим действием антигенов токсокар (аллергические реакции немедленного и замедленного типов). Происходит сенсибилизация иммуноаллергических клеток и последующее резкое повышение выброса медиаторов аллергии и выработки IgE, что обуславливает выраженный каскад реакций острой аллергии (крапивница и сокращение бронхов). Это в какой-то мере может стать позитивным звеном и привести к гибели части личинок, однако часто характер процесса несёт чрезмерный ответ и становится патологическим для организма.
В отсроченный период в результате реакций гиперчувствительности замедленного типа происходит контакт предварительно сенсибилизированных лимфоцитов с антигенами токсокар, что проявляется в образовании специфических иммунных комплексов и последующим привлечением в околопаразитарные ткани макрофагов, эозинофилов и иммунных кластеров с формированием паразитарных гранулём в любых человеческих органах (преимущественно в печени, лёгких, сердце, лимфатических узлах, коже и другое) с длительно протекающими токсико-аллергическими поражениями органа и организма целом.
С течением времени гранулёмы могут обрастать капсулой фиброзного характера, что несколько отграничивает патологический паразитарно-аллергический процесс и может являться препятствием при диагностике и лечении.
Преимущественная локализация гранулём определяет главенствующие клинические и патоморфологические изменения, например, обнаружено сходство изменений в лёгких при токсокарозе и бронхиальной астме: по статистике около 50% случаев бронхиальной астмы ассоциировано с токсокарозом и выявлением специфических антител при ИФА.
Длительное паразитирование у человека может приводить к функциональному истощению и извращению иммунологических реакций, что проявляется общим снижением и неадекватными реакциями иммунитета на какие-либо стандартные раздражители.
При малоинтенсивном заражении вследствие слабого иммунного ответа возможно изолированное единичное проникновение личинок в глаза (преимущественно в области сетчатки вблизи зрительного нерва или желтого пятна), что выражается развитием кровоизлияний, образованием эозинофильно-лимфоцитарных гранулём, длительно протекающими воспалительными процессами (воспалительно-аллергическими) различных сред глаза (в зависимости от локализации гельминта) и иногда приводит к потере органа зрения. [1] [6] [10]
Классификация и стадии развития токсокароза
Наименование заболевания по МКБ-10: В83.0 Висцерaльнaя формa зaболевaний, вызывaемых мигрaцией личинок гельминтов [висцерaльнaя Larva migrans]. Токсокaроз.
По течению заболевание бывает:
По клинической форме выделяют:
Степени тяжести заболевания:
Характер течения токсокароза:
Осложнения токсокароза
Диагностика токсокароза
Лабораторная диагностика:
Дифференциальная диагностика:
Лечение токсокароза
Необходимость лечения определяется совокупностью клинических и лабораторных проявлений заболевания.
Лёгкие и абортивные формы как правило не нуждаются в специфической терапии, так как организм самостоятельно производит деструкцию и удаление паразитов (если их небольшое количество) и требуют лишь симптоматического лечения — назначения противоаллергических и дезинтоксицирующих средств.
При более серьёзных поражениях проводиться комплексное противопаразитарное лечение с применением специфических противопаразитарных препаратов (действующих на тканевые формы червей) под контролем общелабораторных показателей в сочетании с дезинтоксикацией, поддержкой функции печени, снижением аллергической составляющей и иногда гормонотерапией.
При острых формах (особенно у детей) лечение проходит в стационаре под постоянным контролем медперсонала, при хронических формах — обычно в амбулаторном порядке.
Контроль излеченности путём определения титра антител в ИФА и общих анализов осуществляется не ранее, чем через 5-6 месяцев после окончания лечения, так как в первые месяцы из-за распада личинок и капсул количество антител резко повышается и может быть неверно истолковано.
Также показано диспансерное наблюдение в течения 6-12 месяцев в зависимости от конкретных проявлений с периодическим лабораторным обследованием. [1] [2] [6]
Прогноз. Профилактика
Как правило, при малоинтенсивных заражениях и своевременно начатом лечении прогноз благоприятный. При тяжёлых и запущенных формах (несвоевременное распознавание и лечение) возможно развитие осложнений (бронхиальная астма), редко — летальный исход (при ВИЧ в стадии СПИДа, других СПИД-ассоциированных состояниях, а также гипермассивной инвазии).
Профилактика и противоэпидемические мероприятия:
ТОКСОКАРОЗ: современный подход
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
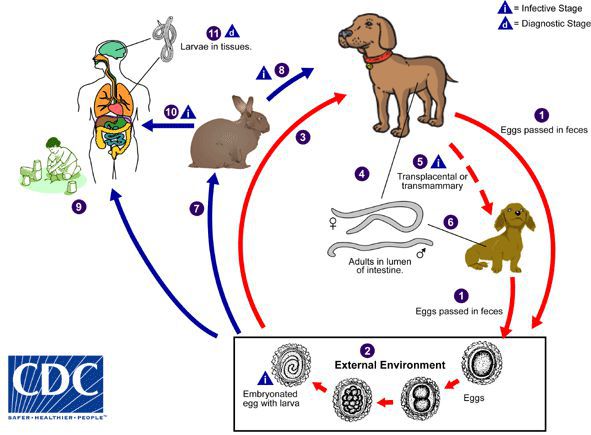
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека. Симптоматика токсокароза малоспецифична и имеет сходство с клиническими симптомами острой фазы других гельминтозов. Заболевание обычно развивается внезапно и остро или после короткой продромы проявляется в виде легкого недомогания. Появляется температура — субфебрильная в легких случаях и высокая до 39°С и выше, иногда с ознобом, — в тяжелых случаях инвазии. Могут наблюдаться кожные высыпания в виде крапивницы или полиморфной сыпи, иногда отеки типа Квинке. В остром периоде наблюдается легочный синдром различной степени тяжести: от легких катаральных явлений до острого бронхита, пневмонии, тяжелых приступов удушья. Особенно тяжело легочный синдром протекает у детей раннего возраста. Рентгенологически выявляется усиление легочного рисунка, «летучие» инфильтраты, картина пневмонии. Наряду с этим у части больных отмечается увеличение печени, иногда и селезенки. Лимфаденопатия более выражена у детей. Иногда имеет место абдоминальный синдром в виде приступов болей в животе, симптомов диспепсии. Возможно развитие миокардита, панкреатита. Известны случаи поражения щитовидной железы, проявляющиеся симптомами опухоли. Возможно поражение мышечной ткани с развитием болезненных инфильтратов по ходу мышц. При миграции личинок в головной мозг развиваются симптомы поражения ЦНС: упорные головные боли, эпилептиформные приступы, парезы, параличи. У детей заболевание сопровождается слабостью, легкой возбудимостью, нарушением сна.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).