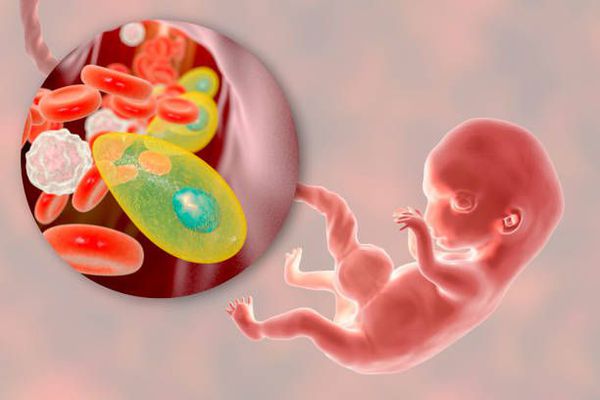
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
Этиология
Таксономия:
Вид — Toxoplasma gondii
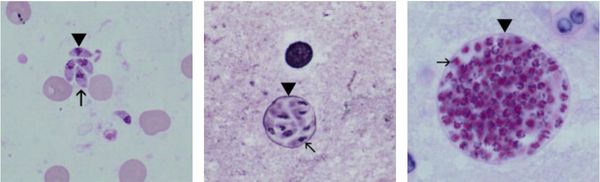
Токсоплазмы обитают в мире в трёх формах:
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
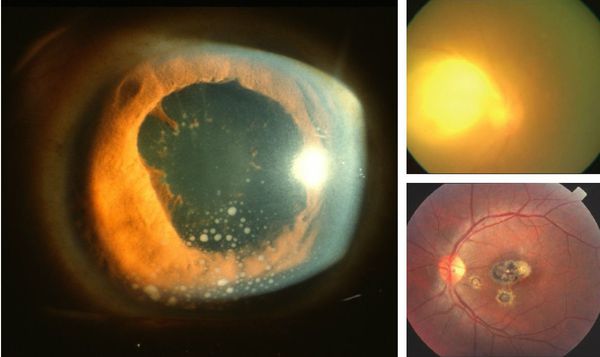
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
Патогенез токсоплазмоза
Входные ворота токсоплазмоза — ротовая полость, оттуда ооцисты попадают в кишечник человека. Далее при развитии паразита (делении его клеток) образуются трофозоиты, которые мигрируют в различные органы и ткани (преимущественно в ЦНС и мышечную). В клетках они формируют псевдоцисты — большое количество размножающихся паразитов.
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
По клиническим признакам выделяют пять форм заболевания:
По степени тяжести заболевание бывает:
По наличию осложнений выделяют:
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]
Токсоплазмоз
Автор: врач, научный директор АО «Видаль Рус», Жучкова Т. В., t.zhutchkova@vidal.ru
Что такое токсоплазмоз?
Причины возникновения токсоплазмоза
Заражение токсоплазмой человека происходит от домашних животных, чаще всего от кошек. Особенно опасно такое заражение для беременных женщин, поэтому им лучше с кошками не контактировать.
Заражение может произойти и при употреблении в пищу мясных продуктов, яиц от зараженных животных, не прошедших достаточную термическую обработку. Токсоплазма может попасть непосредственно в кровь человека через поврежденную кожу или передаваться кровососущими насекомыми. Наконец, бывают случаи и внутриутробного заражения.
Факторы, которые могут способствовать появлению в организме паразита и повышают риск возникновения токсоплазмоза:
Дотрагиваться грязными руками до рта после контакта с землей, после уборки кошачьего туалета, или любого другого контакта с кошачьими экскрементами.
Принимать в пищу сырое или не до конца приготовленное мясо, особенно свинину, мясо ягненка или оленину.
Прикасаться ко рту после контакта с сырым или непрожаренным/непроваренным мясом.
Пересадка органов или переливание крови (очень редко).
Если женщина беременна, и она заразилась токсоплазмозом, инфекция может от нее передаться ребенку, что может привести к серьезным последствиям.
Проявления токсоплазмоза
Различают врождённый и приобретённый токсоплазмоз.
Особую опасность представляет вероятность внутриутробного заражения плода. Токсоплазма способна проникать через плаценту и вызывать болезнь у еще не родившегося ребенка. Но это возможно только в том случае, когда мать заражается токсоплазмозом во время беременности. В случае, если она заразилась еще до беременности, будущему ребенку ничего не угрожает.
Но токсоплазмоз может поражать плод только один раз, все последующие беременности будут надежно защищены образовавшимися у матери антителами.
Приобретённый токсоплазмоз нередко протекает в латентной (скрытой) форме; острая форма может напоминать тиф или энцефалит, нередки поражения глаз. Длится острая стадия примерно 7 дней. Острый токсоплазмоз начинается с высокой температуры, головной боли, судорог, рвоты. Увеличивается печень и селезенка, могут присоединиться воспаление легких и параличи.
Наиболее частой является хроническая форма заболевания, с длительным повышением температуры до 37,2-37,8 градусов, головными болями, увеличением печени, селезёнки, лимфатических узлов; мышечными и суставными болями. Возможно и носительство инфекции.
Хроническая форма и носительство нередко переходят в острую форму на фоне стресса, беременности, снижения иммунитета различной природы. На выраженность проявлений токсоплазмоза существенно влияет общее состояние здоровья, иммунный статус. У лиц с иммунодефицитом (включая СПИД) заболевание протекает крайне тяжело, часто со смертельным исходом.
Профилактика токсоплазмоза
Учитывая возможность полового пути заражения целесообразно использование барьерных методов контрацепции, антисептических спреев. Особое внимание к профилактике токсоплазмоза должно уделяться в семьях, где есть домашние животные (в частности кошки). Не позволяйте кошкам бегать по столам, ограничьте своё общение с кошкой, тщательно мойте руки после контакта с животными. Не подносите животное к лицу, а тем более не целуйте его. Поручите смену кошачьего туалета другим членам семьи.
Соблюдение мер профилактики позволяет существенно сократить риск заражения.
Что может сделать ваш врач?
Необходимость лечения и выбор препаратов для лечения может подобрать только специалист.
Лечение токсоплазмоза проводится не всем. Это необходимо только при выраженных признаках заболевания у детей и ослабленных взрослых. Лечат обычно несколькими антибактериальными препаратами в различных сочетаниях.
Хронический токсоплазмоз поддается лечению с большим трудом, в данном случае кроме антибактериальных препаратов применяются средства, укрепляющие иммунитет.
Носителям токсоплазмы лечения не требуется.
При выявлении первичного токсоплазмоза на ранних сроках беременности женщине предлагается сделать аборт.
Что можете сделать Вы?
Как уже сказано выше, самую большую опасность токсоплазмоз представляет для плода.
При планировании беременности лучше обезопасить себя и будущего ребенка и прекратить любые контакты с животными и грызунами.
В случае появления вышеописанных признаков у взрослого человека, необходимо немедленно обратиться к врачу.
Токсоплазмоз, симптомы и лечение
Заболеванию в большей степени подвержены, как домашние, так и дикие животные и птицы, являясь основным источником заражения для человека. Человек может заразиться токсоплазмозом несколькими путями:
Токсоплазмоз чаще отмечается у рабочих мясокомбинатов, животноводов, ветеринаров, зоологов, паразитологов, медицинского персонала роддомов и больниц.
В Мордовии ежегодно регистрируется 1-2 случая заболевания токсоплазмозом.
Виды токсоплазмоза.
Токсоплазмоз подразделятся на врожденный и приобретенный. При приобретенном заболевании, заражая человека токсоплазмы паразитируют внутриклеточно в различных тканях и могут выделяться из кишечника, почек и слизистых оболочек рта, легких, глаз, носа. Инкубационный период после заражения токсоплазмозом бывает от нескольких дней до нескольких недель, когда появятся первые симптомы заболевания. Больных с острой формой заболевания необходимо изолировать.
При врожденном токсоплазмозе заражение плода происходит от матери при беременности, что вызывает различные поражения мозга плода, параличи, умственную отсталость, пороки развития, увеличение печени, селезенки, желтухи и др. Иногда на ранних сроках беременности это заболевание может вызвать гибель плода и выкидыш. При тяжелых врожденных последствиях ребенок погибает после родов в первые месяцы жизни. Для определения ранних симптомов токсоплазмоза при беременности проводят серологические реакции, для определения антител и наличия иммуноглобулина «М».
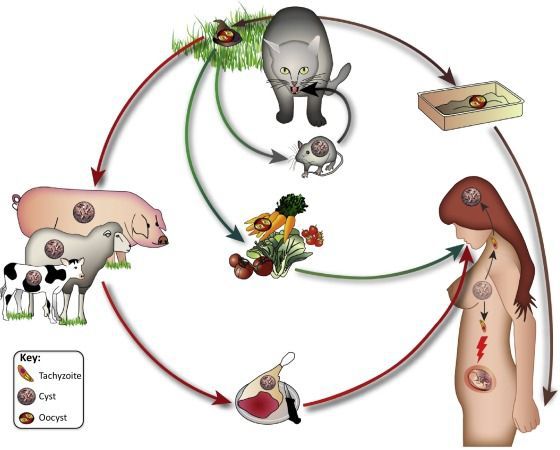
Источники инфекции и пути передачи.
1. Основными источниками заражения считаются домашние и беспризорные кошки, так как в организме этих животных происходит полный путь развития паразита (тканевой и кишечный). Кошачьи испражнения могут очень долго сохраняться во внешней среде, представляя потенциальную опасность для других животных и человека, но чаще инфицирование может произойти при уборке кошачьего туалета.
2. Песок или земля. Очень часто токсоплазма проникает в человеческий организм через загрязненный песок или землю (на огороде, в саду, в парке или на детской площадке, оборудованной песочницей).
3. Мясо и яйца. Некоторые сельскохозяйственные животные и птицы считаются промежуточными хозяевами паразита. Следует отметить, что они не являются непосредственным источником заражения, так как в их организме токсоплазма не образует цист, но, вместе с тем, возбудитель может находиться в мясе (чаще всего в баранине и в свинине), а также в птичьих яйцах. В этом случае заражение происходит из-за недостаточной термической обработки вышеперечисленных продуктов питания.
4. Немытые овощи и фрукты. Если продукты питания загрязнены инфицированной землей, риск заражения просто огромен (из литературных источников известно, что кошка за 2-3 недели может выделить во внешнюю среду порядка 2 млрд. цист, которые до двух лет остаются заразными).
5. Передача инфекции от матери к плоду. Данный путь передачи токсоплазмоза является самым опасным. Как правило, это заражение происходит в том случае, когда паразит проникает в организм ранее не инфицированной женщины, а затем, через плаценту – в организм плода. В этом случае последствия для еще не родившегося ребенка могут быть самыми катастрофическими, в связи с чем, токсоплазмоз во время беременности зачастую является показанием к её искусственному прерыванию.
Зараженный токсоплазмозом человек не опасен для окружающих, то есть, прямого заражения от человека к человеку не происходит ни при каких контактах. Однако переливание крови от инфицированного донора реципиенту или пересадка органов представляет определенную опасность, но и в этом случае, по мнению специалистов, риск заражения ничтожно мал.
Симптомы токсоплазмоза
Симптомы приобретенного токсоплазмоза похожи на симптомы других заболеваний: слабость, головная боль, мышечная боль, увеличение лимфатических узлов (чаще на шее), одышка, частый пульс, повышение температуры, иногда понос, нарушение зрения, розово-пузырная сыпь, боли в области сердца и в правом подреберье.
Выделяют 5 форм токсоплазмоза со своими симптомами:
Для подтверждения диагноза при данных симптомах токсоплазмоза нужно обязательно сделать анализ, для выявления антител в сыворотке больных
Лечение токсоплазмоза
Токсоплазмоз – это паразитарная инфекция, которая не всегда нуждается в лечении. К сожалению, полностью уничтожить возбудителя не представляется возможным, поэтому незначительное количество паразита и антитела к нему остаются в организме человека до конца его жизни.
Вместе с тем в клинической практике встречались единичные случаи, когда пациенты полностью излечивались от заболевания. Однако это происходило только тогда, когда им назначалась адекватная терапия в самые первые дни после заражения.
По истечении совсем незначительного промежутка времени после проникновения возбудителя в организм его хозяина, токсоплазма формирует цисты, обладающие высокой устойчивостью, в том числе и к лекарственным препаратам. Именно поэтому при обнаружении в организме человека антител к паразиту в отсутствие клинических признаков заболевания лечение токсоплазмоза, как правило, не проводится. Исключение составляют беременные женщины, новорожденные и лица с иммунодефицитом.
Следует подчеркнуть, что лечение токсоплазмоза – это сложный и длительный процесс, проводящийся в несколько курсов с использованием этиотропных средств и антибиотиков.
Для каждого пациента курс лечения токсоплазмоза назначается сугубо индивидуально и длится до тех пор, пока не ликвидируются все клинические проявления болезни, ухудшающие качество жизни человека.
Самолечение приводит к хронической форме болезни.
Профилактика заболевания заключается в неукоснительном соблюдении правил личной и общественной гигиены. Беременным женщинам не рекомендуется контактировать с кошками, а еще, по возможности не следует допускать животных в песочницы и другие места, где играют дети. Категорически недопустимо дегустировать сырой фарш и употреблять термически необработанное мясо, а также пить сырые яйца и молоко.
Лечение токсоплазмоза
Варианты химиотерапии токсоплазмоза
Резистентность и побочные эффекты
Устойчивость T. gondii к лекарственным препаратам считается незначительной проблемой по сравнению с плохой комплаентностью и спектром побочных эффектов. Однако, сообщалось о неэффективности длительного лечения врожденного токсоплазмоза на основе PYR, возможно, из-за развития лекарственно-устойчивого штамма T. gondii. PYR и SDZ являются ингибиторами синтеза ДНК у тахизоитов T. gondii, но также могут подавлять синтез ДНК в тканях с высокой метаболической активностью, таких как костный мозг и эпителий. Этого можно избежать, добавив фолиновую кислоту (FA), и эти побочные эффекты будут обращены вспять после прекращения лечения.
Лечение врожденного токсоплазмоза
Существует два показания для введения специфического лечения против T. gondii : 1) пренатальное лечение, направленное на предотвращение передачи паразитов от матери к плоду (MFTP) и / или уменьшение повреждений плода, и 2) послеродовое лечение с целью облегчения клинических проявлений и / или предотвращения отдаленных последствий у инфицированного новорожденного.
Однако преимущества дородового лечения по-разному оцениваются в литературе из-за смешивающих факторов ( Robert-Gangneux, 2014 ), поскольку это может зависеть, среди прочего, от типа лечения, времени введения препаратов после заражения матери, дозы, режимы и продолжительность.терапии. Таким образом, необходимо знать точное время материнского заражения, что возможно только в странах с программами серологического скрининга беременных, то есть в ограниченном числе европейских стран. Соотношение польза / риск послеродового лечения также подвергалось сомнению, особенно у бессимптомных или субклинических инфицированных пациентов, для которых продолжительность лечения и долгосрочные преимущества все еще обсуждаются в литературе.
ПЦР-анализ образцов AF, начиная с 16-й недели гестации (gw) и далее, позволяет переключить лечение на комбинации на основе PYR, в первую очередь на комбинацию PYR-сульфадиазин (PYR-SDZ), при получении положительного результата ПЦР. Однако комбинация PYR-SDZ является тератогенной, и поэтому ее следует избегать в течение первых 14 gw, хотя это пороговое значение варьируется в зависимости от страны к стране. В любом случае, пренатальная диагностика никогда не проводится раньше 14 gw, поэтому лечение SPI является правилом в течение первого триместра беременности.
Защитный эффект SPI известен давно. В классическом исследовании Desmonts и Couvreur ( Desmonts and Couvreur, 1974 ) сообщалось о снижении MFTP более чем на 50% (45% в группе без лечения по сравнению с 22% в группе лечения), но результаты были смещены из-за того, что не учитывался срок беременности. при сероконверсии. Однако несколько обсервационных исследований, опубликованных с 1999 г., ставят под сомнение способность пренатального лечения снижать тяжесть инфекции, признавая при этом его роль в снижении материнско-фетальной передачи.
Исследование EMSCOT 2005 года показало на 72% меньшую вероятность внутричерепных поражений у младенцев, рожденных от матерей, пролеченных в течение 4 недель после сероконверсии. Мета-анализ SYROCOT 2007 среди 1438 матерей, получавших лечение, показал, что начало пренатального лечения в течение трех недель после сероконверсии привело к снижению MFTP на 52% по сравнению с лечением, введенным через 8 или более недель, но не сообщил о явном влиянии пренатального лечения на частоту. клинических проявлений у инфицированных новорожденных.
Послеродовое лечение начинается после подтверждения диагноза врожденной инфекции и направлено на предотвращение или уменьшение клинических проявлений при рождении и облегчение возможных отдаленных последствий или клинических рецидивов, в основном, глазных.
Гематологические побочные эффекты
Фолиновая кислота
Новые варианты лечения токсоплазмоза
Системное лечение ( Butler et al., 2013 ; Ozgonul and Besirli, 2017 ), сочетающее противопаразитарные препараты и кортикостероиды ( Holland and Lewis, 2002 ), рекомендуется при токсоплазмозе глаз у пациентов с ослабленным иммунитетом. Однако сравнительные исследования этой популяции пациентов немногочисленны.
Большинство соединений, ингибирующих рост паразитов, обладают противовоспалительными и противораковыми свойствами. Это неудивительно, поскольку уже было продемонстрировано, что некоторые лекарственные препараты, используемые при лечении рака и воспалительных процессов, проявляют сильное действие на рост T. gondii in vitro. Из них милтефозин показал многообещающие результаты в лечении многочисленных протозойных инфекций и в настоящее время широко используется для лечения висцерального лейшманиоза. Его способность успешно лечить энцефалит, вызванный свободноживущими амебами, подчеркивает его способность преодолевать гематоэнцефалический барьер. Он не показал эффективности в борьбе с острым токсоплазмозом, но, наоборот, введение этого препарата через 60 дней после заражения мышей штаммом ME49 привело к уменьшению количества и размера кист головного мозга. Другая противораковая молекула (тетраоксан) была протестирована на мышиной модели острого токсоплазмоза и значительно увеличила выживаемость инфицированных мышей по сравнению с контрольными мышами.
Иммунотерапевтические стратегии
Острая инфекция токсоплазмой остается в основном бессимптомной у иммунокомпетентных хозяев благодаря соответствующему иммунному контролю, приводящему к инцистации паразитов. Однако частичное нарушение реакции хозяина паразитом позволяет цистам сохраняться на протяжении всей жизни. Это сожительство паразита и хозяина опирается на строго регулируемый баланс для контроля репликации паразита. Возникновение любого иммунного дефекта, особенно влияющего на ответ Т-клеток, в основном вторичного по отношению к ВИЧ-инфекции или иммуносупрессивной терапии, приводит к реактивации паразитов, что приводит к тяжелому энцефалиту или диссеминированной инфекции. В настоящее время ни один из описанных выше методов лечения не может уничтожить паразита у инфицированных хозяев, что делает их уязвимыми для дальнейших рецидивов. В этом контексте в течение многих лет иммунотерапия рассматривалась как многообещающий и полезный подход к лечению токсоплазмоза, позволяющий хозяевам с ослабленным иммунитетом восстановить адекватный иммунный ответ.
Провоспалительный ответ Th1 с участием цитокинов, таких как IL-12, IFNγ, TNFα, а также IL-7 и IL-15, является основой адекватного антипаразитарного ответа, сначала во время острой инфекции для уменьшения количества паразитов, а затем во время хроническая инфекция для оказания иммунного давления, достаточного для поддержания инцистации паразитов. И наоборот, иммунодепрессивные цитокины, такие как IL-10, способствуют внутримозговому сохранению паразитов, а нарушение местного иммунного ответа приводит к реактивации латентных цист T. gondii в головном мозге. Во-первых, для усиления врожденного иммунитета было показано, что введение IL-18 усиливает IL-12-опосредованную устойчивость к токсоплазме у мышей SCID с сильной иммуносупрессией, что приводит к уменьшению количества паразитов и увеличению времени до смерти. Несмотря на то, что эндогенный IL-18, по-видимому, принимает ограниченное участие в врожденной резистентности, защитная роль, обеспечиваемая добавлением экзогенного IL-18, коррелировала с увеличением количества NK-клеток и цитотоксической активностью, а также с повышенными уровнями INOS в ткани селезенки.
Слабый терапевтический ответ на обычное лечение можно было бы компенсировать добавлением альтернативной терапии, включая добавление или ингибирование определенных интерлейкинов (анти-IL-10), непрямых иммуностимулирующих препаратов, клеточного переноса или переноса антител. Таким образом, усиление иммунного ответа хозяина может быть соблазнительным терапевтическим подходом 1) для предотвращения реактивации токсоплазмоза у пациентов с ослабленным иммунитетом, если он имеет меньше побочных эффектов, чем широко используемый лекарственный препарат котримоксазол, или 2) для помощи в лечении эпизодов тяжелой реактивации в сочетании с обычные препараты, но все еще необходимы активные исследования в этой области.
Пациенты с ослабленным иммунитетом
PYR / SDZ, казалось, был наиболее эффективным лечением, но мощность исследования не может показать превосходного лечения ( Katlama et al., 1996 ) с меньшим количеством рецидивов во время поддерживающей терапии, чем PYR / CLD, но вызвала больше побочных эффектов, чем PYR / CLD или TMP / SMX. Предпочтительным режимом является PYR (ударная доза 200 мг в день 1, затем 75 мг / день, если пациент весит ≥60 кг, или 50 мг / день, если пациент весит