Вся правда о гормонозаместительной терапии
Беру на себя смелость описать преимущества и страхи перед назначением гормонозаместительной терапии (ГЗТ). Уверяю вас – будет интересно!
ГЗТ у женщин сложнее и многограннее, чем у мужчин. Если мужчине нужен для замещения только тестостерон, то женщине и эстрогены, и прогестерон, и тестостерон, а иногда и тироксин.
При ГЗТ используются меньшие дозы гормонов, чем в препаратах гормональной контрацепции. Препараты ГЗТ не обладают контрацептивными свойствами.
Все приведённые ниже материалы основаны на результатах крупномасштабного клинического исследования ГЗТ у женщин: Womens Health Initiative (WHI) и опубликованы в 2012 году в консенсусе по гормонозаместительноной терапии НИИ Акушерства и гинекологии им. В.И. Кулакова (Москва).
Итак, основные постулаты ГЗТ.
Противопоказания к ГЗТ:
Обследования перед назначением ЗГТ:
О препаратах, используемых в ГЗТ.
Этрогены накожные (гели):
Дивигель 0.5 и 1 гр 0.1%, Эстрожель
Комбинированные препараты Э/Г для циклической терапии: Фемостон 2/10, 1/10, Климинорм, Дивина, Трисеквенс
Комбинированные препараты Э/Г для непрерывного приёма: Фемостон 1/2.5 конти, Фемостон 1/5, Анжелик, Клмодиен, Индивина, Паузогест, Климара, Прогинова, Паузогест, Овестин
Тиболон
Гестагены: Дюфастон, Утрожестан
Андрогены: Андрогель, Омнадрен-250
К альтернативным методам лечения относятся
растительные препараты: фитоэстрогены и фитогормоны. Данные о долговременной безопасности и эффективности этой терапии не достаточны.
В некоторых случаях возможно единовременное сочетание гормональной ГЗТ и фитоэстрогенов. (например, при недостаточном купировании приливов одним видом ГЗТ).
Женщины, получающие ЗГT, должны не реже одного раза в год посещать врача. Первое посещение намечается через 3 месяца от начала ГЗТ. Необходимые обследования для мониторирования ГЗТ врач вам назначит, учитывая особенности вашего здоровья!
Важно! Обращение администрации сайта о вопросах в блоге:
Уважаемые читатели! Создавая этот блог, мы ставили себе цель дать людям информацию по эндокринным проблемам, методам диагностики и лечения. А также по сопутствующим вопросам: питанию, физической активности, образу жизни. Его основная функция – просветительская.
В рамках блога в ответах на вопросы мы не можем оказывать полноценные врачебные консультации, это связано и недостатком информации о пациенте и с затратами времени врача, для того чтобы изучить каждый случай. В блоге возможны только ответы общего плана. Но мы понимаем, что не везде есть возможность проконсультироваться с эндокринологом по месту жительства, иногда важно получить еще одно врачебное мнение. Для таких ситуаций, когда нужно более глубокое погружение, изучение медицинских документов, у нас в центре есть формат платных заочных консультаций по медицинской документации.
Как это сделать? В прейскуранте нашего центра есть заочная консультация по медицинской документации, стоимостью 1200 руб. Если эта сумма вас устраивает, вы можете прислать на адрес patient@mc21.ru сканы медицинских документов, видеозапись, подробное описание, все то, что сочтете нужным по своей проблеме и вопросы, на которые хотите получить ответы. Врач посмотрит, можно ли по представленной информации дать полноценное заключение и рекомендации. Если да, вышлем реквизиты, вы оплатите, врач пришлет заключение. Если по предоставленным документам нельзя дать ответ, который можно было бы рассматривать как консультацию врача, мы пришлем письмо о том, что в данном случае заочные рекомендации или выводы невозможны, и оплату брать, естественно, не будем.
С уважением, администрация Медицинского центра «XXI век»
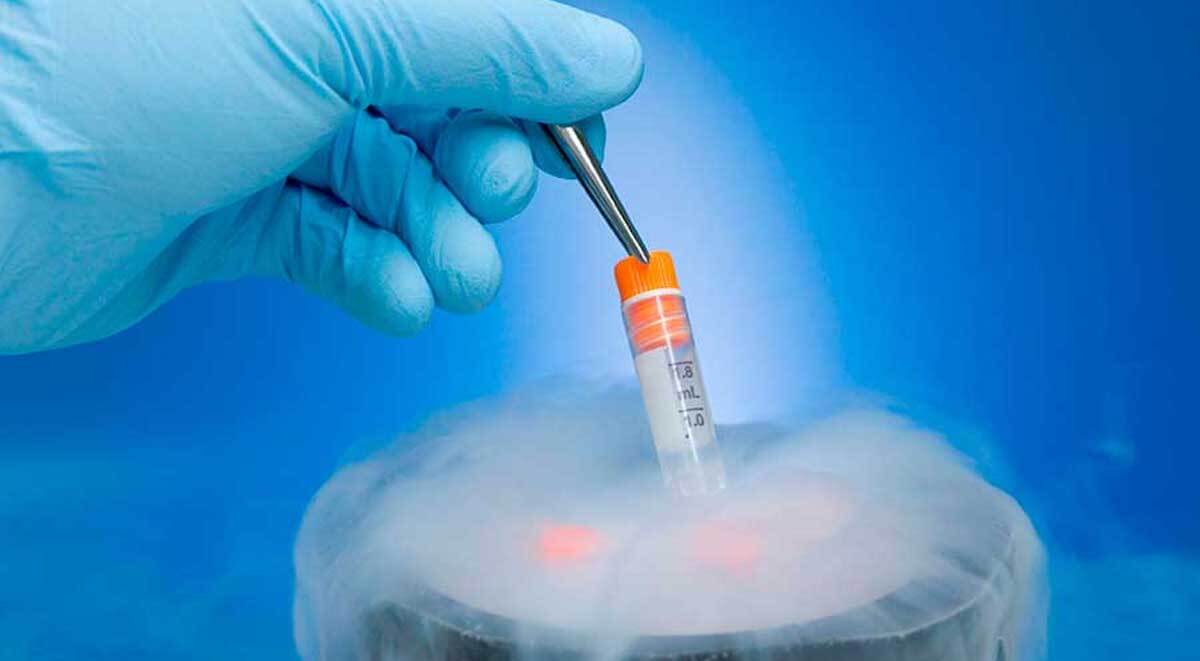
Криоперенос эмбриона – особенности
Одна из ступеней цикла ЭКО – криоперенос эмбриона. Эта процедура проводится в случае, если созрели и были оплодотворены порядка 4-6 здоровых яйцеклетки. Как правило, женщине переносят от двух до четырех яйцеклеток. Другие жизнеспособные эмбрионы врачи советуют замораживать. Бывает так, что приживаются все 4 эмбриона, а бывают случаи, когда все эмбрионы погибают. В таком случае пересаживают оставшиеся криогенные эмбрионы. Один из самых больших плюсов криопереноса – это то, что женщине не нужно делать повторную стимуляцию гормонами, а мужчине сдавать свой генетический материал.
Плюсы и минусы
Нацеливание себя на успех – один из основных советов будущим родителям. Криоперенос является дополнительным фактором успешности зачатия ребенка, и этот фактор сказывается на настроении будущих родителей. У криопереноса зародыша есть существенные плюсы. Самые важные из них это снижение риска того, что возникнет синдром гиперстимуляции яичников и их преждевременное старение. Другие плюсы криопереноса эмбриона:
Процесс криопереноса эмбриона
Что нужно делать после криопереноса
Для начала необходимо обеспечить женщине полный покой. Она ни в коем случае не должна волноваться и переживать. Необходимо соблюдать режим дня, хорошо спать и много времени проводить с друзьями и близкими, чтобы не дать себе зациклиться на своем положении.
В первые сутки после криопереноса не нужно принимать горячую ванну и душ. Нельзя поднимать тяжелые вещи и наклоняться, водить автомобиль. На период до контрольного теста на беременность лучше не заниматься сексом и избегать физических нагрузок. Лучше носить свободную одежду, питаться как можно более сбалансировано – пить овощные и фруктовые соки, есть нежирное мясо, включить в рацион крупы и злаки. Словом, лучше вести как можно более размеренный образ жизни. И, конечно же, необходимо быть под постоянным наблюдением специалиста. Врачи клиники Вспомогательных Репродуктивных Технологий помогут в этот волнительный период жизни справится с эмоциями и дадут четкие индивидуальные рекомендации. Специалисты ВРТ имеют многолетний опыт, который помог многим парам стать родителями. На любые вопросы по планированию семьи ответят внимательные сотрудники центра, а также проведут полное обследование организма будущих мамы и папы.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Гипоэстрогенные состояния у женщин репродуктивного, пре- и менопаузального возрастов
Патогенетической терапией лечения ранневременных симптомов гипоэстрогении является заместительная гормональная терапия (ЗГТ). В случае противопоказаний к ЗГТ или отказа от нее, достаточно эффективны альтернативные фитопрепараты, которые в меньшей степени,
К гипоэстрогенным состояниям относятся изменения в организме женщин на фоне снижения или прекращения выработки эстрогенов яичниками.
В первую очередь возникает комплекс вегетативно-сосудистых, нейроэндокринных и нейропсихических симптомов (ранневременные расстройства). Затем появляются урогенитальные и сексуальные нарушения, изменения внешности (средневременные расстройства). В последнюю очередь наступают поздневременные обменные нарушения: остеопороз, ишемическая болезнь сердца, болезнь Альцгеймера [1].
Эти многочисленные симптомы гипоэстрогении связаны с наличием огромного количества рецепторов к эстрогенам в различных органах и системах женщины: половых органах, гипоталамусе и гипофизе, сердечно-сосудистой системе, уретре и мочевом пузыре, коже и волосах, толстом кишечнике, печени [2].
Вышеназванные изменения могут возникать не только естественно в климактерическом периоде, но и при воздействии на организм женщины других факторов: после хирургических операций (удаление или резекция яичников по поводу кист и апоплексии, ампутации матки); при истощении фолликулярного аппарата (синдром истощения яичников) [3, 4]; при извращенной реакции эстрогеновых рецепторов (синдром резистентных яичников); на фоне применения некоторых лекарственных препаратов, в частности агонистов рилизинг-гормонов (АГ-РГ); при лечении эстроген-зависимых заболеваний женской половой системы, а также в длинных протоколах стимуляции суперовуляции программы экстракорпорального оплодотворения (ЭКО) при лечении бесплодия (требует add-back терапии для снятия нейровегетативных симптомов) [5, 6].
Гипоэстрогенные состояния, связанные с незначительным снижением продукции эстрогенов (при щадящей резекции яичников, каутеризации не поликистозных, а мультифолликулярных яичников и др.), имеют свои особые клинические проявления, чаще всего приводящие к нарушению репродуктивной функции (ановуляция, недостаточность лютеиновой фазы; сниженный овариальный резерв, приводящий к бедному ответу яичников в программах ЭКО) [7]. По нашим данным в программах ЭКО такие пациентки встречаются в 22,3% случаев.
Гипоэстрогения в климактерическом периоде может служить моделью для изучения классических клинических проявлений этого состояния, т. к. климактерий это естественный достаточно длительный биологический процесс перехода от периода репродукции к старости, в основе которого лежит постепенное угасание функции яичников и снижение продукции эстрогенов. Наиболее ярко проявляют себя ранневременные расстройства [1]. Комплекс симптомов ранневременных расстройств при определенной степени выраженности принято называть климактерическим синдромом (КС). По нашим данным, полученным совместно с И. В. Бесман [8], КС в перименопаузе встречается в 57,6% случаев, при этом в 65% — в осложненной форме (т. е. на фоне экстрагенитальной патологии). Осложненная форма КС обуславливает максимальную выраженность симптомов КС. В настоящее время ранневременные симптомы гипоэстрогении связывают с дезорганизацией функции лимбико- ретикулярного комплекса. С нарушением функции гипоталамуса связывают такие проявления ранневременных расстройств, как приливы, гипергидроз, сердцебиение, гипертензия. С нарушением функции лимбической системы связывают депрессию, нарушение сна, головные боли, снижение памяти. Все ранневременные нарушения снижают качество жизни женщины, но особенно это касается приливов и расстройств сна. Приливы могут беспокоить женщину 5–10–20 и более раз в сутки. Расстройства сна: удлинение периода засыпания, частое пробуждение ночью, поверхностный сон — не дают ощущения полноценного отдыха. Несомненно, все эти нарушения требуют дифференцированного подхода к лечению в зависимости от причины гипоэстрогении и возраста, в котором они наступают.
Безальтернативной патогенетической терапией ранневременных симптомов гипоэстрогении считается сегодня заместительная гормональная терапия (ЗГТ) [1, 6]. У женщин репродуктивного возраста после оперативного удаления или резекции яичников, с синдромами резистентных и истощенных яичников лечение можно начинать с комбинированных эстроген-гестагенных препаратов [1]. Это могут быть современные трехфазные препараты, например Клайра. У женщин после гистерэктомии терапия проводится с использованием натуральных эстрогенов с последующим добавлением гестагенов [6]. При плохой переносимости пероральных препаратов можно рекомендовать их в виде геля или пластыря для чрезкожного введения (Эстрожель, Дивигель, Климара) с периодическим назначением гестагенов вагинально (например, Утрожестан). Длительность ЗГТ определяется состоянием и самочувствием пациентки.
В климактерическом периоде при лечении ранневременных расстройств важно придерживаться позиции Международного общества по менопаузе (2007 г.):
Кроме того, должны учитываться современные принципы назначения ЗГТ:
Противопоказания к ЗГТ:
Интересен по своему составу препарат Менопейс Плюс, в который входят капсулы с витаминами и минералами (21 компонент), а также растительные таблетки, содержащие изофлавоны сои, лигнаны семян льна, шалфей и зеленый чай. Составляющие растительной таблетки превращаются в фитоэстрогены в кишечнике, благоприятно действуют на нервную систему, уменьшают приливы, являются источниками антиоксидантов. Цикл приема этого препарата по одной капсуле и одной растительной таблетке в день составляет 28 дней.
Мы, совместно с И. В. Бесман [9], имеем опыт применения альтернативных ЗГТ растительных средств, при лечении осложненной формы КС в случаях, когда ЗГТ было противопоказано. Наши исследования показали, что качество жизни этих пациенток, определяемое по специальной шкале, несколько хуже, чем у тех, кто принимал ЗГТ; но значительно лучше, чем у тех, кто не принимал вообще никаких препаратов. Кроме того, эти средства дают хороший эффект при купировании вазомоторных симптомов в длинных протоколах с АГ-РГ программ ЭКО.
Все вышесказанное еще раз подтверждает мнение специалистов о том, что дифференцированный подход к лечению ранневременных нарушений при гипоэстрогенных состояниях с применением ЗГТ различных режимов или альтернативных растительных средств дает хороший эффект и значительно улучшает качество жизни женщин.
Литература
ГБУЗ МО МОПЦ, Балашиха
Abstract. Pathogenetic therapy treatment of early symptoms of hypoestrogenism consists of hormone replacement therapy (HRT). In the case of contraindications to the HRT medication or refusal of a woman, alternative herbal medication is effective less than HRT, but however improves the quality of life.
Что лучше эстрожель или дивигель при эко
Клиника ГЕНЕЗИС, Санкт-Петербург
ООО «Генезис», 191015, Санкт-Петербург, Россия
Опыт применения препарата Эстрожель в программах ВРТ
Журнал: Проблемы репродукции. 2018;24(5): 58-62
Волкова Ю. В., Боярский К. Ю., Семененко А. Е. Опыт применения препарата Эстрожель в программах ВРТ. Проблемы репродукции. 2018;24(5):58-62.
Volkova Iu V, Boiarskiĭ K Iu, Semenenko A E. Estrogel supplemontation in ART program. Russian Journal of Human Reproduction. 2018;24(5):58-62.
https://doi.org/10.17116/repro20182405158
Препараты эстрадиола широко применяют в программах вспомогательных репродуктивных технологий. Поддержку лютеиновой фазы, назначение заместительной гормональной терапии в циклах c переносом криоконсервированных/размороженных эмбрионов, программы с использованием донорского материала и программы суррогатного материнства невозможно представить без назначения препаратов эстрадиола. Несомненно, что контролируемая овариальная стимуляция может оказывать повреждающее действие на активность желтого тела, поэтому необходимо дополнительно назначать препараты прогестерона и эстрадиола, которые восполняют его функцию. Нами проанализированы систематические обзоры, опубликованные в течение последних 5 лет и посвященные применению эстрадиола в программах вспомогательных репродуктивных технологий. Рассмотрены биологические эффекты и особенности метаболизма препаратов эстрадиола в зависимости от способа введения. Имеющиеся в литературе данные указывают на преимущество трансдермального пути введения препаратов эстрадиола. На клиническом примере продемонстрирована эффективность трансдермальной формы препарата эстрадиола Эстрожель у пациентки с «тонким» эндометрием в протоколе контролируемой овариальной стимуляции с применением антагонистов гонадотропин-рилизинг-гормона.
Клиника ГЕНЕЗИС, Санкт-Петербург
ООО «Генезис», 191015, Санкт-Петербург, Россия
Современные методы вспомогательной репродукции — экстракорпоральное оплодотворение (ЭКО) и перенос эмбрионов — широко вошли в медицинскую практику. Они зарекомендовали себя как эффективные методы лечения бесплодия, связанного с трубно-перитонеальным и мужским факторами, с эндометриозом, синдромом поликистозных яичников, а также бесплодия неясного генеза. Широко применяются программы с использованием донорского материала (ооциты, эмбрионы) и программы суррогатного материнства. В основе данных методов — получение достаточного количества ооцитов и эмбрионов, определяющих результативность программ вспомогательных репродуктивных технологий (ВРТ), подготовка эндометрия к прегравидарной трансформации и имплантации эмбриона, последующее лечение для поддерживания беременности раннего срока. Последние этапы невозможно представить себе без применения препаратов эстрадиола [1].
Показания к назначению эстрогенов в циклах ВРТ можно определить как абсолютные, индивидуальные и подлежащие дальнейшим исследованиям. К абсолютным показаниям относятся программы с использованием ооцитов/эмбрионов донора, программы суррогатного материнства, перенос криоконсервированных/размороженных эмбрионов.
К индивидуальным показаниям можно отнести недостаточный рост и трансформацию эндометрия в процессе стимуляции яичников в программах ВРТ, недостаточную толщину эндометрия в посттрансферном периоде, старший репродуктивный возраст [2, 3]. Дальнейшие исследования необходимы в отношении показаний к назначению «эстрогенового прайминга» с целью повысить ответ яичников на последующую стимуляцию.
Эстрогены — общее собирательное название подкласса стероидных гормонов, производимых в основном фолликулярным аппаратом яичников у женщин. В небольших количествах эстрогены производятся также яичками у мужчин и корой надпочечников у представителей обоих полов. Из различных биологических жидкостей человека выделено более 30 видов эстрогенов. Основными из них считаются следующие: эстрон (Е1), 17-β-эстрадиол (Е2) и эстриол (Е3). Эстрадиол и некоторое количество эстрона синтезируются в яичниках непосредственно из андрогенов при участии ферментов ароматаз. Эстрон и эстриол образуются преимущественно в печени из эстрадиола, а также в других тканях из андрогенов, главным образом из андростендиона.
С помощью транспортной системы крови — альбумина и глобулина, связывающего половые гормоны (ГСПГ), эстрогены доставляются к органам-мишеням, проникают через клеточные мембраны в цитоплазму, где связываются с рецепторами эстрогенов. Образующийся рецепторный комплекс переходит в ядро клетки и активирует геном, что приводит к синтезу специфичных белков, в том числе рецепторов. Эстрогены циркулируют в крови и выводятся из организма главным образом в виде аддуктов с глюкуроновой и серной кислотами [4, 5].
Эстрогены и их синтетические аналоги можно классифицировать следующим образом:
1) природные стероиды (эстрадиол, эстрон, эстриол);
2) эфиры и конъюгаты природных эстрогенов (17β-эстрадиол, эстрадиола гемигидрат, эстрадиола валерат, эстропипат, полиэстрадиола фосфат, конъюгированный эстроген, эстрадиола бензоат, эстрадиола дипропионат);
3) синтетические стероиды (этинилэстрадиол, местранол, квинэстрол);
4) синтетические вещества нестероидной структуры (диэтилстилбестрол, диенэстрол, бензэстрол, гексэстрол, метэстрол, металенестрил, хлоротрианизен) [1].
Официально зарегистрированы для применения в клинической практике на территории РФ следующие виды эстрогенов:
1) этинилэстрадиол представлен в качестве эстрогенового компонента многих комбинированных оральных контрацептивов (КОК);
2) эстриол (применяется у женщин в постменопаузе для локального лечения вульво-вагинальной атрофии);
3) эстрадиол, 17β-эстрадиол, эстрадиола гемигидрат и эстрадиола валерат — наиболее приближены к натуральным эстрогенам, применяются для гормонотерапии в период менопаузы в качестве монотерапии или в сочетании с гестагенами, для подготовки к беременности, в том числе в программах ВРТ, а также в составе некоторых КОК.
Наиболее привычным и часто используемым методом является прием препарата перорально. Эффект в таком случае развивается через 20—40 мин в зависимости от содержимого желудка, липофильности лекарства, характера растворителя, но такой способ применения эстрогенов связан с рядом проблем. Как показывают исследования [6], многие нежелательные реакции обусловлены эффектом первичного прохождения эстрадиола через печень (первичный печеночный метаболизм), поскольку концентрация эстрадиола в портальной вене в 3—4 раза выше, чем в циркулирующей крови после приема эстрогена внутрь. Биодоступность форм эстрадиола для перорального приема в среднем составляет 3%. Для того, чтобы получить желаемый эффект, приходится идти по пути увеличения дозы лекарственного препарата, что и делается на практике [7]. Однако это повышает вероятность риска развития нежелательных побочных эффектов. В частности, при пероральном приеме препаратов эстрадиола в ответ на его метаболизм в печени могут усиливаться белковые и липидные обменные процессы, может возрастать синтез биологически активных веществ (факторы свертывания, ангиотензиногены, ГСПГ, а также глобулина, связывающего тироксин). В данном случае плазменные концентрации эстрадиола (пиковые и субтерапевтические) имеют значительную вариабельность, что осложняет предсказуемость клинического ответа [6]. Более физиологичным способом введения эстрогенов является трансдермальный путь, при котором активное вещество попадает непосредственно в большой круг кровообращения в течение суток постепенно, без выраженных пиков (см. рисунок). 
Программы донации ооцитов сопряжены с процессом синхронизации циклов донора и реципиента при условии «свежих» ооцитов/эмбрионов и последующего назначения гормональной поддержки на этапе подготовки эндометрия к переносу эмбриона в полость матки и далее для поддержания ранних сроков беременности до полноценного включения плаценты как гормонпродуцирующего органа. Следует отметить, что альтернативы назначению препаратов эстрадиола и прогестерона нет, так как указанные программы проводят женщинам с удаленными или нефункционирующими яичниками [2].
Применение эстрадиола является обязательным при подготовке эндометрия и активации его рецептивности в циклах переноса размороженных эмбрионов. Назначение эстрадиола 4—8 мг/сут перорально воспроизводит его сывороточный уровень и оказывает периферический эффект аналогично тому, как это происходит в естественном менструальном цикле. Однако печень при этом подвергается воздействию значительно большего количества эстрадиола, что у некоторых пациентов может привести к нежелательным последствиям. Особенно это касается женщин с высоким риском развития тромбозов вен. В таких случаях для достижения необходимой эстрогенной насыщенности назначение эстрадиола лучше проводить путем комбинирования форм для трансдермального введения (с использованием максимально возможной дозы) и для перорального введения; в итоге доза перорального эстрадиола может быть значительно снижена [7, 8].
Интенсивность печеночного метаболизма при пероральном применении эстрадиола зависит также от приема дополнительных препаратов. У женщин, получающих психотропные препараты, наблюдается резистентность к препаратам эстрадиола, принимаемым перорально; в таких случаях следует прибегнуть к формам для трансдермального применения. Чаще всего при трансдермальном применении препарата достаточно выбрать дозу эстрадиола, которая обычно продуцируется яичниками для достижения периферического эффекта (0,2 мг/сут). При трансдермальном введении эстрадиола (Е2) уровень эстрона (Е1) остается в физиологическом соотношении Е2/Е1 >1; при приеме внутрь уровень эстрона в 10 раз выше. Эстрон является слабым эстрогеном с низким сродством для рецепторов эндометрия. Пока еще нет достаточных данных о влиянии повышенного уровня эстрона на организм [8, 9].
В 2017 г. T. Ghobara и соавт. [10] проанализировали результаты 18 рандомизированных контролируемых исследований, включивших 3815 женщин, которым производили перенос размороженных эмбрионов в разных режимах: в естественном цикле с применением триггера хорионического гонадотропина человека (ХГЧ) и без него, на фоне заместительной гормональной терапии с десенситизацией гипофиза препаратами агонистов гонадотропин-рилизинг-гормона (ГнРГ) и без них. Авторы установили, что статистически достоверных различий в эффективности между различными протоколами подготовки к переносу размороженных эмбрионов нет. Подготовка эндометрия в циклах с гормональной поддержкой зачастую является протоколом выбора не только у пациенток с ановуляторным менструальным циклом. Сегодня большинство центров применяют препараты эстрадиола и прогестерона в циклах криопереносов, так как это минимизирует посещения клиники пациентами и позволяет планировать дату переноса эмбриона.
Поддержка лютеиновой фазы в программах ВРТ
Контролируемая овариальная стимуляция в программах ВРТ позволяет получить достаточное количество ооцитов и эмбрионов, что обеспечивает высокую частоту наступления беременности, но также оказывает повреждающее действие на аденогипофиз, влияя на механизм высвобождения лютеинизирующего гормона (ЛГ). Как известно, после овуляции, индуцированной спонтанным пиком ЛГ или введением триггера (ХГЧ, 5000—10 000 МЕ), лютеинизированные клетки гранулезы начинают продуцировать как эстрадиол, так и прогестерон. Активность желтого тела поддерживается пульсирующей выработкой ЛГ. К факторам, повреждающим этот механизм в программах ВРТ, относятся аналоги ГнРГ (антагонисты, агонисты); супрафизиологический уровень эстрадиола при контролируемой овариальной стимуляции (КОС); замещение эндогенного пика ЛГ введением триггера (ХГЧ, агонистов ГнРГ) [8, 11, 12].
В проспективном рандомизированном исследовании, выполненном корейскими учеными [13], сравнивали исходы циклов с применением антагонистов ГнРГ при поддержке лютеиновой фазы только вагинальным прогестероном и при комбинации вагинального прогестерона и перорального эстрадиола в дозе 4 мг. Установлено, что у пациенток, получавших комбинацию прогестерона и эстрадиола, частота имплантации была выше, а частота кровотечения во II фазу — достоверно ниже.
В рандомизированном исследовании E. Yanushpolsky и соавт. [14] продемонстрировано снижение частоты кровотечений в лютеиновой фазе циклов ВРТ при дополнительном назначении препаратов эстрадиола.
В 2015 г. M. van der Linden и соавт. [15] проанализировали результаты 94 рандомизированных контролируемых исследований (с участием 26 198 женщин), в которых использованы различные режимы поддержки лютеиновой фазы. Авторы отмечают повышение частоты наступления беременности и родов у пациенток, принимающих микронизированный прогестерон в сочетании с комбинацией трансдермального и перорального введения эстрадиола, либо только в сочетании с трансдермальным. При комбинировании только перорального приема эстрадиола с гестагенами не отмечено увеличение частоты наступления беременности и родов. Таким образом, назначение трансдермальных форм введения эстрадиола в поддержке посттрансферного периода у пациентов в программах ВРТ повышает вероятность наступления беременности и родов живым плодом.
«Тонкий» эндометрий — одна из нерешенных проблем в программах ЭКО
Результаты большинства исследований [7] указывают на то, что частота наступления беременности существенно снижается при толщине эндометрия менее 7 мм в день переноса эмбрионов. Возможно, при такой толщине эндометрия бластоциста в процессе имплантации близко соприкасается со спиральными артериями и находится в области высокой концентрации кислорода. В литературе [14] описаны исследования влияния дополнительного назначения эстрадиола с 7-го дня менструального цикла на исход программ ЭКО, в ходе которых обнаружили повышение частоты беременности и частоты имплантации у женщин, получавших эстрадиол по сравнению с женщинами, которым подобное лечение не проводили.
Также одной из областей применения препаратов эстрадиола является назначение эстрогенового «прайминга» с целью снижения уровня фолликулостимулирующего гормона (ФСГ). Исследования показали, что назначение препаратов эстрадиола в лютеиновую фазу цикла, предшествующего циклу КОС, приводит к гомогенности антральных фолликулов и к тому, что на 3-й день они имеют меньшие размеры.
На сегодняшний день опубликован метаанализ 8 исследований, из которых лишь одно является рандомизированным, что означает необходимость дальнейшего анализа и накопления данных [16, 17].
Клинический пример
Пациентка П., 33 лет обратилась по поводу бесплодия в браке. Из анамнеза: возраст начала первой менструации — 13 лет, цикл регулярный. Половая жизнь с 18 лет. Барьерный метод контрацепции. Соматически здорова. В браке состоит 6 лет, из которых в течение последних 2 лет методы контрацепции не использовала. Беременности не было.
Объективно: индекс массы тела — 18,13 кг/м 2 ; оволосение по женскому типу; молочные железы развиты правильно, отделяемого из сосков нет. Данные обследования: ЛГ — 3,4 МЕ/л, ФСГ — 5 МЕ/л, антимюллеров гормон — 2,3 нг/мл. На первичном приеме при ультразвуковом исследовании (УЗИ) обнаружен гидросальпинкс с двух сторон. Рекомендована лапароскопия. При обследовании супруга выявлена тератозооспермия (3% нормальных форм сперматозоидов в спермограмме по Крюгеру).
После проведенной лапароскопии, удаления гидросальпинкса с двух сторон пациентке проведен цикл КОС в протоколе с антагонистами ГнРГ. Протокол и стартовая доза выбраны с учетом данных гормонального обследования, количества антральных фолликулов, возраста и статуса пациентки. С 7-го дня стимуляции, учитывая данные УЗИ, идентифицирован дефицит эстрогенов (толщина эндометрия 5 мм, средний диаметр фолликулов составил 14—15 мм), назначен трансдермальный гель Эстрожель в дозе 3 мг/сут. В день введения триггера (рекомбинантный ХГЧ) толщина эндометрия составила 8 мм. Ответ на стимуляцию был адекватным, получено 10 ооцитов, из которых 8 было М2. При оплодотворении методом интрацитоплазматической инъекции сперматозоида получено 8 эмбрионов. На 5-е сутки пациентке перенесена 1 бластоциста отличного качества. Толщина эндометрия в день переноса составила 10 мм. Криоконсервированы 3 бластоцисты. Поддержка посттрансферного периода — микронизированный прогестерон вагинально 400 мг, эстрадиол 3 мг в трансдермальной форме введения (Эстрожель), фолиевая кислота 2 мг, агонисты ГнРГ 0,1 мг двукратно после эмбриотрансфера. Беременность наступила. Данный клинический пример демонстрирует эффективность назначения препарата Эстрожель в комбинации с микронизированным прогестероном в циклах КОС с применением антагонистов ГнРГ.
Заключение
Препараты эстрадиола широко применяют в программах вспомогательных репродуктивных технологий для поддержки лютеиновой фазы, на фоне заместительной гормональной терапии в циклах c переносом криоконсервированных/размороженных эмбрионов, а также в программах суррогатного материнства и других. Анализ данных литературы о биологических эффектах и особенностях метаболизма препаратов эстрадиола в зависимости от способа введения показал преимущество трансдермального пути. На клиническом примере продемонстрирована эффективность трансдермальной формы препарата эстрадиола Эстрожель у пациентки с «тонким» эндометрием в протоколе контролируемой овариальной стимуляции с применением антагонистов ГнРГ.
Авторы заявляют об отсутствии конфликта интересов.