Что лучше ксефокам или ибупрофен
Самые популярные НПВП
Многие люди даже не представляют, насколько часто нам приходится использовать нестероидные противовоспалительные препараты для излечения от различных хворей, сопровождающих человеческий род со времен изгнания Адама и Евы из райских кущ.
Почитайте список таких средств, наверняка некоторые из них лежат в вашей домашней аптечке. Итак, к НПВП относятся такие лекарства, как: «Аспирин», «Амидопирин», «Анальгин», «Пироксикам», «Быструмгель», «Диклофенак», «Кетопрофен», «Индометацин», «Кеторол», «Напроксен», «Кеторолак», «Флурбипрофен», «Вольтаренгель», «Нимесил», «Диклофенак», «Ибупрофен», «Индопан», «Ипрен», «Упсарин УПСА», «Кетанов», «Месулид», «Мовалис», «Найз», «Нурофен», «Ортофен», «Тромбо АСС», «Ультрафен», «Фастум», «Финалгель».
Да, все это НПВП-препараты. Список получился хоть и большой, но, конечно же, далеко не полный. И все-таки он вполне дает представление о многообразии современных нестероидных противовоспалительных лекарственных средств.
Немного исторических фактов
Но пройдут еще долгие годы научных исследований, прежде чем это лекарство появится на свет. Грандиозное событие свершилось в 1899 году. Врачи и их пациенты быстро оценили преимущества нового лекарственного средства. В 1925 году, когда на Европу обрушилась страшнейшая эпидемия гриппа, «Аспирин» стал спасителем для огромного множества людей.
А в 1950-м данный нестероидный противовоспалительный препарат попал в книгу рекордов Гиннесса как обезболивающее средство с самым большим объемом продаж. Ну а впоследствии фармацевтами были созданы и другие нестероидные противовоспалительные препараты (НПВП).
При каких болезнях применяются противовоспалительные нестероидные лекарства?
Спектр применения НПВП очень широк. Они являются весьма действенными при врачевании как острых, так и хронических болезней, сопровождающихся болями и воспалением.
В наши дни полным ходом идут исследования на предмет изучения эффективности данных препаратов при лечении заболеваний сердца и сосудов. А о том, что их можно использовать при болях в позвоночнике, знают сегодня практически все (НПВП при остеохондрозе являются настоящим спасением).
Вот перечень болезненных состояний, при возникновении которых показано применение различных нестероидных противовоспалительных средств: Лихорадка. Головные боли, мигрени. Почечные колики. Ревматоидный артрит. Подагра. Артрозы. Остеоартрит. Дисменорея. Воспалительные артропатии (псориатический артрит, анкилозирующий спондилоартрит, синдром Рейтера). Болевой синдром послеоперационный. Болевой синдром от слабой до средней степени тяжести при травмах и различных воспалительных изменениях.
Классификация НПВП по их химической структуре
Читая эту статью, вы уже имели возможность убедиться в том, что нестероидных противовоспалительных лекарств очень много. Чтобы ориентироваться среди них хотя бы чуточку получше, давайте займемся классификацией этих средств.
Классификация нестероидных противовоспалительных лекарств по их эффективности
Применение НПВП при остеохондрозе и при лечении других суставных болезней способно в буквальном смысле творить чудеса. Но, к сожалению, не все препараты одинаковы по своей эффективности. Безусловными лидерами среди них можно считать: «Диклофенак», «Кетопрофен», «Индометацин», «Флурбипрофен», «Ибупрофен» и некоторые другие препараты.
Перечисленные лекарственные средства можно назвать базовыми; т. е. на их основе могут разрабатываться и поступать в аптечную сеть новые НПВП, но уже под другим измененным названием и часто по более высокой цене. Чтобы не тратить свои деньги понапрасну, изучите как следует следующую главу.
То же самое можно сказать, например, о «Метиндоле» и «Индометацине» или «Ибупрофене» и «Бруфене» и т. д. Чтобы разобраться в путанице, всегда внимательно смотрите на упаковку, ведь там обязательно должно быть указано основное действующее вещество лекарственного средства. Только написано оно будет, скорее всего, маленькими буковками.
Но это еще не все. Вернее, не все так просто! Применение НПВП-аналога какого-нибудь хорошо знакомого вам лекарства неожиданно может вызвать аллергическую реакцию или побочные действия, которые никогда ранее вами не наблюдались. В чем тут дело? Причина может крыться в дополнительных добавках, о которых, конечно же, на упаковке ничего не было написано. Значит, надо изучать еще и инструкцию.
Список аналогов известных препаратов
Мы публикуем эту небольшую шпаргалку в надежде, что она вам поможет лучше ориентироваться в многочисленных красивых аптечных упаковках. Допустим, вам немедленно требуются эффективные НПВП при артрозе, чтобы снять мучительную боль. Достаете шпаргалку и читаете следующий список:
Правила приема НПВП
Прием НПВП может сопровождаться целым рядом побочных эффектов, поэтому рекомендуется при их приеме соблюдать следующие правила:
Побочные эффекты и нестероидная гастропатия
Теперь вам предстоит узнать, что такое НПВП-гастропатия. К великому сожалению, все НПВП обладают немалыми побочными эффектами. Особенно негативно они влияют на желудочно-кишечный тракт. Больных могут беспокоить такие проявления, как Тошнота (иногда очень сильная). Изжога. Рвота. Диспепсия. Кровотечения желудочно-кишечные. Диарея. Язва двенадцатиперстной кишки и желудка.
Все вышеперечисленные неприятности и есть НПВП-гастропатия. Поэтому врачи так часто стараются назначать своим пациентам минимально возможные дозы классических нестероидных противовоспалительных лекарств. Чтобы свести к минимуму вредное воздействие на желудок и кишечник, рекомендуется никогда не принимать такие препараты на голодный желудок, а делать это только после обильного приема пищи.
Нестероидные противовоспалительные препараты нового поколения
В последние два десятилетия одновременно несколько фармкомпаний усиленно вели разработку новых современных НПВП, которые, наряду с эффективным устранением боли и воспаления, имели бы побочных эффектов как можно меньше.
О некоторых их преимуществах мы расскажем на примере «Мовалиса». Он выпускается как в традиционных таблетках (по 7,5 и 15 мг), так и в суппозиториях по 15 мг, и в стеклянных ампулах для введения внутримышечно (также по 15 мг). Действует данное лекарство очень мягко, но в то же время чрезвычайно эффективно: на весь день достаточно всего одной таблетки. Когда пациенту показано длительное лечение при тяжелых артрозах тазобедренных или коленных суставов, «Мовалис» просто незаменим.
Разные формы, в которых выпускаются НПВП
Большинство популярных нестероидных противовоспалительных средств можно приобрести и использовать не только в виде таблеток и капсул для приема внутрь, но так же и в мазях, гелях, свечах и в растворах для инъекций. И это, безусловно, очень хорошо, так как подобное разнообразие дает возможность в некоторых случаях избежать вреда при лечении с одновременным получением более быстрого лечебного эффекта.
В основном, уколы назначаются при обострении воспалительных и дегенеративно-дистрофических заболеваниях суставов и позвоночника, сопровождающихся сильной нестерпимой болью. После того как состояние пациента улучшается, становится возможным переход на таблетки и наружные средства в виде мазей.
Обычно врачи комбинируют разные лекарственные формы, решая, что и когда может принести больному наибольшую пользу. Вывод напрашивается сам: если не хотите нанести себе вред самостоятельным лечением таких распространенных недугов, как остеохондроз или артроз, обращайтесь за помощью в медицинское учреждение, именно там вам смогут помочь.
Можно ли применять НПВП при беременности
Врачи категорически не советуют принимать НПВП беременным женщинам (особенно этот запрет касается третьего триместра), а также мамочкам, которые кормят грудью. Считается, что лекарства данной группы способны отрицательно сказываться на вынашивание плода и вызывать у него различные пороки развития.
По некоторым данным, такое безобидное лекарство, по мнению многих, как «Аспирин», способно увеличивать риск выкидыша на ранних сроках. Но иногда врачи по показаниям назначают женщинам данный препарат (ограниченным курсом и в минимальных дозах). В каждом конкретном случае решение должно приниматься специалистом-медиком.
Разумный выбор НПВП при сочетанной патологии: заболеваниях суставов и гипертонической болезни
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением а
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением активности циклооксигеназы-2 (ЦОГ-2) в очаге воспаления — ключевого фермента синтеза простагландинов провоспалительной активности, а подавление изоформы ЦОГ-1 приводит к нарушению физиологических реакций: в частности, к нарушению синтеза простагландинов класса Е в слизистой оболочке желудка и развитию НПВП-гастропатии.
Большинство «стандартных» НПВП способно подавлять активность обеих изоформ ЦОГ, поэтому их применение часто ограничено из-за развития побочных эффектов, в первую очередь — со стороны желудочно-кишечного тракта (ЖКТ). Субъективные симптомы со стороны ЖКТ встречаются примерно у трети больных, а в 5% случаев представляют серьезную угрозу жизни пациентов. Именно поэтому в последние годы особо пристальное внимание привлекает проблема безопасного применения НПВП. Полагают, что препараты более селективные в отношении ЦОГ-2 реже вызывают развитие НПВП-гастропатии. Изучение механизмов действия НПВП послужило толчком к созданию новых препаратов, обладающих всеми положительными свойствами стандартных НПВП, но менее токсичных, — это специфические ингибиторы ЦОГ-2 [3, 4, 13].
В последние годы особую актуальность приобрела проблема взаимодействия НПВП и гипотензивных препаратов, а также связи между применением НПВП и развитием гипертонической болезни (ГБ). Неселективные НПВП могут привести к повышению АД (преимущественно диастолического) не только у больных артериальной гипертензией (АГ), но и у лиц с нормальным АД за счет ингибиции системного и локального, внутрипочечного синтеза простагландинов. Известно, что постоянный прием НПВП вызывает у пациентов увеличение АД в среднем на 5,0 мм рт. ст. Характерным свойством НПВП является также взаимодействие с гипотензивными препаратами, в основе гипотензивного действия которых лежат преимущественно простагландин-зависимые механизмы. Назначение НПВП пациентам, получающим по поводу АГ β-адреноблокаторы, ингибиторы АПФ и диуретики, приводит к снижению гипотензивного эффекта [8, 9].
Нимесулид был разработан еще в 1985 г. и является одним из первых НПВП, при изучении которого продемонстрирована более высокая селективность в отношении ЦОГ-2 и накоплен большой клинический опыт. В многочисленных исследованиях in vitro и in vivo было показано, что нимесулид примерно в 5–20 раз более селективно ингибирует ЦОГ-2, чем ЦОГ-1. Большой интерес представляет и тот факт, что нимесулид обладает широким спектром ЦОГ-независимых эффектов, которые могут определять его противовоспалительную, анальгетическую и хондропротективную активность [1, 2, 5, 7, 11, 12].
Нимесулид хорошо переносится больными и редко вызывает развитие серьезных побочных эффектов, требующих отмены препарата. По результатам ряда исследований, частота побочных эффектов, развивающихся на фоне приема нимесулида, достоверно не отличается от плацебо или ниже, чем при приеме других НПВП. Например, по данным мета-анализа, у больных, получавших нимесулид, общая частота побочных реакций со стороны ЖКТ была значительно ниже (8,7%), чем при назначении других НПВП (16,8%). Низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ-2-селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [6, 10, 13].
Таким образом, нимесулид относится к селективным ингибиторам ЦОГ-2, сравним по эффективности с «классическими» НПВП, но отличается более благоприятным профилем токсичности. Фармакоэкономический анализ свидетельствует о преимуществах нимесулида по сравнению с диклофенаком, в первую очередь в связи с более низкой частотой поражения ЖКТ.
Целью нашего исследования явилось изучение эффективности и переносимости найза (нимесулида) у больных РА в сравнении с ортофеном (диклофенаком).
Материалы и методы
Оба НПВП назначались случайным способом 40 больным с момента первого установления диагноза РА, согласно критериям Американской коллегии ревматологов. Найз применялся в виде таблеток по 100 мг дважды в день, ортофен — в виде таблеток по 25 мг в суточной дозе 150 мг. Одновременно всем больным проводилась базисная терапия, преимущественно метотрексатом или сульфасалазином. Эффективность и переносимость НПВП оценивались через 3 нед. от начала лечения, т. е. в те сроки, когда эффект базисных препаратов еще не имел клинической значимости.
В I группе из 20 пациентов, получавших найз, было 14 женщин и 6 мужчин, средний возраст пациентов составил 55,1 года, длительность суставного синдрома к моменту установления диагноза — от 3 до 14 мес., в среднем — 7,25 мес. Во II группе из 20 больных, получавших ортофен, было 18 женщин и 2 мужчин, средний возраст больных — 42,75 года, длительность суставного синдрома — от 2 до 14 мес., в среднем — 5,65 мес. Клиническая характеристика обеих групп представлена в таблице 1.
Результаты лечения оценивались по динамике показателей суставного синдрома (суставной индекс Ричи (СИ), счет болезненных суставов (СБС), счет припухших суставов (СПС), продолжительность утренней скованности (мин), выраженность боли по визуально-аналоговой шкале (ВАШ)) и на основании общей оценки эффективности лечения, по мнению врача и больного. Кроме того, у всех больных оценивалась динамика АД на фоне лечения НПВП.
Результаты
В I группе на фоне лечения найзом в суточной дозе 200 мг за 3 нед. лечения достигнута достоверная динамика показателей суставного синдрома. При этом эффективность терапии оценена 17 пациентами (85%) как хорошая и 3 (15%) — как удовлетворительная. По мнению врача, в 16 случаях (80%) наблюдалась хорошая эффективность препарата, в 4 случаях (20%) — удовлетворительная (рис. 1). Переносимость найза у 85% была хорошей, только у 2 больных (10%) отмечались изжога и гастралгии, у 1 больного (5%) — чувство тяжести в эпигастральной области. Однако при фиброгастроскопии у этих пациентов не выявлено эрозивного повреждения слизистой оболочки желудка. В группе больных, принимавших найз, не потребовалось отмены препарата ни у одного больного.
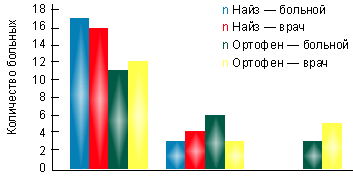 |
| Рисунок. Оценка эффективности препаратов на основании мнения больного и врача |
Во II группе на фоне терапии ортофеном в суточной дозе 150 мг через 3 нед. также отмечена существенная динамика показателей суставного синдрома. Однако оценка эффективности терапии показала, что только 11 пациентов (55%) оценили эффективность препарата как хорошую, 6 (30%) — как удовлетворительную и трое больных (15%) признали ее неудовлетворительной. По мнению лечащего врача, достаточная эффективность ортофена, соответствующая градации «хорошая», отмечалась в 12 случаях (60%), удовлетворительная — в 3 (15%) и неудовлетворительная — в 5 (25%) случаях (рис.).
Переносимость препарата ортофен была хуже, чем у найза: у 9 пациентов (45%) отмечались симптоматические побочные эффекты, причем у 3 больных (15%) потребовалась отмена препарата через 2 нед. от начала лечения в связи с выявленным при ФГДС эрозивным поражением слизистой оболочки антрального отдела желудка. В целом из побочных эффектов чаще отмечались изжога — у 7 (35%) пациентов, гастралгии — у 8 (40%), тошнота — у 4 (20%) и диарея — у 2 (10%) больных.
Особый интерес представляет влияние исследуемых НПВП на уровень АД, так как из 40 больных у 15 имелась сопутствующая ГБ, по поводу которой проводилась гипотензивная терапия. Динамика уровня АД в обеих группах на фоне лечения найзом и ортофеном представлена в таблице 2. Следует отметить, что терапия найзом не требовала усиления проводимой гипотензивной терапии (β-блокаторами, ингибиторами АПФ, диуретиками) и не вызывала повышения АД у ранее нормотензивных пациентов. В то же время лечение ортофеном потребовало коррекции доз гипотензивных препаратов у 4 (66,7%) из 6 больных ГБ и вызвало повышение АД у 5 (25%) женщин в постменопаузе с исходно высоконормальным АД. Данный эффект неселективного НПВП — ортофена — следует считать предсказуемым, особенно с учетом характера проводимой гипотензивной терапии. Все больные ГБ получали в разных комбинациях β-адреноблокаторы, ингибиторы АПФ и диуретики; при этом ни одному пациенту не был назначен дигидропиридиновый антагонист Са — амлодипин, который является препаратом выбора для лечения АГ в условиях терапии НПВП.
Таким образом, результаты открытого клинического исследования показали, что препарат найз у больных РА проявляет выраженную противовоспалительную активность, превосходящую диклофенак. При этом найз характеризуется хорошей переносимостью, малым числом симптоматических побочных эффектов и превосходит с этой точки зрения наиболее широко применяемый в клинической практике ортофен. Дополнительным преимуществом препарата найз можно считать менее выраженное влияние на уровень АД. При назначении найза не требовалось увеличения дозы гипотензивных препаратов. С учетом высокой распространенности эссенциальной гипертензии в популяции, взаимодействие НПВП с наиболее часто используемыми гипотензивными средствами представляется актуальной проблемой. Ревматические заболевания, требующие постоянной терапии НПВП, часто сочетаются с АГ. При этом у большинства больных ГБ коррекция АД может достигаться только благодаря комбинированной антигипертензивной терапии, а монотерапия дигидропиридиновыми антагонистами Са признается недостаточно эффективной. Следовательно, в большинстве случаев при лечении воспалительных ревматических заболеваний у лиц, страдающих ГБ, невозможно полностью нивелировать отрицательное взаимодействие «стандартных» НПВП с основными кардиологическими препаратами — β-адреноблокаторами, ингибиторами АПФ и диуретиками. В такой ситуации представляется рациональным выбор для проведения противовоспалительной терапии специфических ингибиторов ЦОГ-2, представителем которых является найз.
Литература
И. М. Марусенко, кандидат медицинских наук
Н. Н. Везикова, кандидат медицинских наук, доцент
В. К. Игнатьев, доктор медицинских наук, профессор
Петрозаводский университет, кафедра госпитальной терапии
Современные аспекты диагностики и лечения грыж межпозвонкового диска поясничного отдела позвоночника
Боль в области спины, обусловленная заболеваниями позвоночника, представляет собой одну из актуальных проблем современной неврологии. Связано это в первую очередь с высокой частотой встречаемости данной патологии. Согласно статистике
Боль в области спины, обусловленная заболеваниями позвоночника, представляет собой одну из актуальных проблем современной неврологии. Связано это в первую очередь с высокой частотой встречаемости данной патологии. Согласно статистике, от 60 до 80% работоспособного населения страдает от болей в пояснично-крестцовой области [3]. В 2003 г. в Москве данная группа заболеваний явилась причиной почти 380 тыс. дней временной нетрудоспособности и почти 1700 первичных случаев стойкой нетрудоспособности (инвалидности) [3]. За период с 1991 по 2003 г. заболеваемость болезнями костно-мышечной системы и соединительной ткани в Москве увеличилась на 23,4% и составила более 2000 случаев на 100 тыс. взрослого населения [3]. В связи с этим разработка новых методов диагностики и консервативного лечения боли в спине является очень актуальной.
Наиболее частой причиной боли в поясничном отделе является грыжа межпозвонкового диска, которую рассматривают как проявление остеохондроза позвоночника [15].
С возрастом пульпозное ядро — центральная часть диска — теряет эластичность и частично утрачивает амортизирующую функцию. Повторные травмы (подъем тяжести, избыточная статическая и динамическая нагрузка, падения и др.) на фоне возрастных дегенеративных изменений ведут к повышению внутридискового давления. Фиброзное кольцо, расположенное по периферии диска, истончается, в нем образуются трещины, к которым смещается студенистое ядро, образуя выпячивание (пролапс), а при разрыве фиброзного кольца — грыжу. Грыжа диска внутри позвоночного канала может вызывать компрессию нервных корешков и спинного мозга, обусловливая появление боли в спине и конечности (компрессионный механизм). Вещество пульпозного ядра, являясь химическим раздражителем для нервной ткани, способствует возникновению местной воспалительной реакции, отека, микроциркуляторных расстройств. Это вызывает локальное раздражение чувствительных рецепторов и мышечный спазм, приводящий к ограничению подвижности в пораженном отделе (рефлекторный механизм). Длительное существование спазма ведет к нарушению осанки, развитию патологического двигательного стереотипа и поддерживает болевой синдром. Таким образом, рефлекторное напряжение мышц вначале имеет защитный характер, поскольку приводит к иммобилизации пораженного сегмента, однако в дальнейшем становится фактором, дополнительно провоцирующим боль («порочный круг»: боль–спазм–боль).
На формирование болевого синдрома при грыже диска влияют:
Диагностика и дифференциальная диагностика
Основными диагностическими критериями грыжи межпозвонкового диска являются:
Боль в спине может быть обусловлена другими вертеброгенными и невертеброгенными причинами.
Артроз фасеточных суставов является одной из самых распространенных причин хронической боли в спине у пожилых людей. Боль двусторонняя, локализуется, в отличие от дискогенной, паравертебрально, а не по средней линии, усиливается при длительном стоянии и разгибании и уменьшается при ходьбе и сидении.
Стеноз позвоночного канала характеризуется болью в спине после длительной ходьбы — синдром спинальной (псевдоперемежающейся) хромоты. Боль и судороги в пояснице и в ягодицах развиваются при ходьбе, исчезают в положении сидя или лежа, однако вновь усиливаются при возобновлении физической нагрузки. В покое неврологическое обследование не выявляет отклонений от нормы, но сразу после физической нагрузки определяются слабость в нижних конечностях, снижение рефлексов и расстройство чувствительности.
Остеопороз в связи с увеличением в популяции доли лиц пожилого возраста, среди которых бoльшую часть составляют женщины в постменопаузальном периоде, приобретает все большее значение в возникновении боли в спине. В этом случае боль, как правило, умеренно выражена, постоянная, сопровождается локальным мышечно-тоническим синдромом. Диагноз подтверждается данными денситометрии.
Опухоли позвоночника (первичные и метастатические), опухолеподобные заболевания позвонков (кисты) могут проявляться единственным клиническим симптомом в виде боли в спине. Боль не проходит в покое, усиливается ночью и при перкуссии. Для опухолей позвоночного канала характерна острая боль радикулярного типа.
При деструктивном поражении позвоночника (туберкулезный спондилит, первичная опухоль или метастазирование в позвоночник, гиперпаратиреоз), переломе позвоночника, его врожденных или приобретенных деформациях, деформирующем спондилоартрите часто наблюдаются локальная болезненность и локальный мышечно-тонический синдром; диагноз устанавливают на основании результатов рентгенограммы и (или) КТ или МРТ позвоночника.
При первом обращении пациента с острой поясничной болью врачу нужно помнить об аневризме брюшного отдела аорты, поскольку смертность, связанная с ее разрывом, превышает 50%. Быстрое развитие интенсивных болей в пояснице, особенно у мужчин старше 50 лет, страдающих атеросклерозом и артериальной гипертонией, указывает на возможность разрыва или расслоения аневризмы брюшного отдела аорты. Кровотечение в ретроперитонеальную область может привести к иррадиации боли по задне-боковой поверхности бедер. В отличие от острых мышечно-скелетных болей, при которых пациент может найти положение, при котором болевой синдром снижается (анталгическая поза), кровоточащая или расслаивающая аневризма аорты вызывает постоянные боли, не зависящие от положения тела.
При соматических заболеваниях (язвенная болезнь желудка, панкреатит, пиелонефрит и т. д.) отраженная боль в спине обычно носит локальный характер, сочетается с другими проявлениями заболевания, сопровождается напряжением мышц спины, не связана с движениями в позвоночнике; выявляются типичные зоны ирритации и реперкуссии в виде зон гиперстезии (зоны Захарьина–Геда).
Гинекологические заболевания: опущение матки, миомы, эндометрит, аднексит, рак матки, эндометриоз, варикозное расширение вен таза, менструальные боли и даже беременность — являются наиболее частым источником люмбалгии хронического типа у женщин. При этих состояниях боль умеренной интенсивности чаще локализуется в крестце и усиливается при длительном стоянии.
У мужчин к появлению подобных поясничных болей могут приводить заболевания предстательной железы, в том числе хронический простатит.
Опухоли органов брюшной полости и малого таза также являются источником болей в поясничном отделе. Так, например, опухоль поджелудочной железы, особенно хвоста или тела, гипернефрома, рак простаты практически всегда проявляются болями в нижней части спины, сопровождаются локальным мышечно-тоническим синдромом.
Для патологии тазобедренного сустава характерны боли в области сустава с иррадиацией в поясницу и бедро. Боли провоцируются движениями в суставе и сопровождаются ограничением его подвижности. Определяется болезненный спазм всех мышц, принимающих участие в движении сустава.
Ревматическая полимиалгия — достаточно редкая, но требующая внимания у пожилых пациентов причина боли в поясничном отделе позвоночника. Синдром характеризуется постепенно усиливающимися болями и скованностью в проксимальных отделах верхних и нижних конечностей и пояснице, сопровождается значительным ускорением скорости оседания эритроцитов (СОЭ) (до 100 мм/ч) и изменением других лабораторных показателей.
Недостаточное содержание в организме магния может проявляться болевым синдромом в спине, повышением мышечного тонуса, судорогами в ногах и парестезиями. Магний является физиологическим регулятором клеточной и нейрогенной возбудимости, а также способствует активизации витамина В6 [7]. Дефицит магния приводит к внутриклеточному ацидозу, гемодинамическим нарушениям, повышению сосудистого тонуса, гиперкоагуляции, нарушению микроциркуляции. Появление таких нервно-мышечных признаков, как парестезии — чувство жжения и покалывания, «бегания мурашек», похолодания; синдром «беспокойных ног«, мышечные контрактуры, судороги, расстройства мочеиспускания (частые позывы, боли в области мочевого пузыря); простреливающие и ноющие боли в пояснице, другие неприятные ощущения, не имеющие четкого анатомического распределения и объективного подтверждения, также ассоциируются с дефицитом магния. В подобных ситуациях важно определить концентрацию магния в сыворотке крови, особенно в группах высокого риска по его дефициту (интенсивный ритм жизни, постоянные стрессовые ситуации, недостаточный сон, работа при высокой или низкой температуре; синдром мальабсорбции, дисбактериоз кишечника).
Боли в пояснице при отсутствии существенных отклонений в соматическом и нейроортопедическом статусе достаточно часто являются маской депрессии [8]. Болевой синдром в рамках депрессии характеризуется следующими особенностями.
Диагноз устанавливается лишь методом исключения при наличии специфичного болевого синдрома (психалгии), клинических признаков депрессии при отсутствии органического заболевания, которое может объяснять хронический болевой синдром.
Диагностический алгоритм действий врача при обращении пациентов с жалобой на боль в пояснице представлен на рисунке.
Первоначальная оценка пациента с жалобами на боли в пояснице должна включать полный сбор анамнеза и тщательное физикальное исследование, что позволяет выявить лиц, имеющих серьезное заболевание и требующих более широкого обследования.
При сборе жалоб и анамнеза необходимо выяснить:
Обязательным является полное исследование неврологического статуса. Если в процессе неврологического обследования выявлены двигательные или чувствительные расстройства, гипорефлексия, нарушения функции тазовых органов, показано инструментальное исследование — проведение КТ или МРТ.
В случае отсутствия неврологического дефицита, необходимо провести рентгеновское исследование поясничного и крестцового отделов позвоночника. При этом могут диагностироваться следующие патологические изменения: метаболические заболевания костей (остеопороз, остеомаляция, гиперпаратиреоз), остеоартроз, компрессионный перелом, анкилозирующий спондилит (болезнь Бехтерева), спондилолистез, опухоли (гемангиома, остеосаркома, остеома, миеломная болезнь, метастатическое поражение позвоночника), остеохондроз позвоночника, мочекаменная болезнь.
Если патологических изменений при рентгенологическом исследовании не выявлено, осуществляют мануальное исследование тазовых органов (ректальное, вагинальное). Могут быть диагностированы эндометриоз, опухоли органов малого таза, инфекции тазовых органов (абсцесс, цервицит).
При отсутствии патологических изменений в органах малого таза проводят компьютерное или магнитно-резонансное исследование. Исключают инфекционный процесс (остеомиелит, туберкулез, сифилис), ретроперитонеальные опухоли, грыжи межпозвонкового диска, стеноз позвоночного канала.
С целью диагностики остеопороза как причины боли в пояснице, особенно у лиц с высокими факторами риска по остеопорозу (низкий индекс массы тела, ранняя менопауза, пожилой возраст, наличие переломов в анамнезе и т. д.), проводится костная денситометрия. Значение минеральной плотности костной ткани (МПКТ) (Т-индекс) на 2,5 стандартных отклонения ниже средней МПКТ у взрослых (пиковая костная масса) свидетельствует о наличии остеопороза (высокий риск остеопоретических переломов), а на 1 стандартное отклонение — об остеопении.
Впервые возникшая боль в поясничном отделе позвоночника в пожилом возрасте, особенно у мужчин, требует исключения онкологических заболеваний и метастатических поражений скелета, у пожилых женщин — остеопороза и коксартроза.
Лечение боли в спине
Алгоритм лечения грыж межпозвонкового диска предполагает:
Максимально раннее и полное купирование болевого синдрома способно предотвратить закрепление патологического двигательного стереотипа, обеспечить своевременное подключение двигательной терапии и предупредить формирование эмоциональных расстройств.
Лечение рефлекторных и компрессионных синдромов вследствие грыж межпозвонковых дисков в остром периоде основывается на создании щадящего режима, избегании резких наклонов и болезненных поз. Лечение проводится на дому или в неврологическом стационаре. Рекомендованы постельный режим в течение нескольких дней — до уменьшения интенсивности боли, жесткая постель (щит под матрац), прием анальгетиков, нестероидных противовоспалительных препаратов (НПВП) и миорелаксантов.
При невозможности госпитализации следует обеспечить иммобилизацию соответствующего отдела позвоночника при помощи ортезов (фиксирующих поясов, корсетов, полукорсетов, снабженных вертикальными ребрами жесткости) и реклинаторов. Фиксацию поясничного отдела осуществляют до стихания резких болей; в дальнейшем поясничный корсет можно использовать «по требованию»: при длительных статических нагрузках, сидении (работа за столом), интенсивных физических нагрузках, езде на транспорте.
Ведущее место среди методов патогенетически обоснованного лечения боли в поясничном отделе на фоне грыж межпозвонковых дисков принадлежит фармакотерапии.
НПВП и анальгетики. НПВП являются «золотым стандартом» в лечении боли в спине, поскольку воздействуют на основные звенья патогенеза болевого синдрома. Механизм их действия связан с подавлением активности фермента циклооксигеназы (ЦОГ). Существует два вида этих ферментов: ЦОГ-1 и ЦОГ-2. ЦОГ-1 через промежуточные вещества регулирует восстановление слизистой желудка и кишечника, а ЦОГ-2 преимущественно связана с развитием воспалительной реакции и формированием болевого импульса. «Классические» НПВП (диклофенак, ибупрофен, пироксикам и др.) подавляют оба эти фермента, за счет чего понижают чувствительность нервных окончаний к болевым медиаторам, оказывают противовоспалительное и антиагрегантное действие. С подавлением активности ЦОГ-1 связаны побочные эффекты — боли в животе, тошнота, рвота, отрыжка, язвенно-эрозивное поражение желудка, желудочно-кишечные кровотечения, нарушения кишечной проходимости, повышение артериального давления. Побочное действие на желудочно-кишечный тракт проявляется как при назначении таблетированных форм, так и при использовании препаратов в инъекциях или в виде свечей (хотя и в меньшей степени), что существенно ограничивает применение их у пациентов с патологией желудочно-кишечного тракта.
Из всех «классических» НПВП наиболее широко в неврологической практике используются препараты из группы оксикамов, относящиеся к производным эноловых кислот. Наиболее безопасный и эффективный из них ксефокам рапид (лорноксикам). Выраженное анальгетическое действие ксефокама рапида обусловлено мощным ингибированием ЦОГ, простагландин-депрессивным эффектом, одновременной стимуляцией выработки физиологического эндорфина [18]. Кроме того, ксефокам рапид угнетает высвобождение кислорода из активированных лейкоцитов. Многочисленными клиническими исследованиями показано, что ксефокам рапид по силе противовоспалительного и обезболивающего действия превосходит индометацин, диклофенак, не оказывая гастротоксического действия, а также такие анальгетики, как кеторолак, кетопрофен и трамадол, приближаясь по выраженности обезболивающего эффекта к опиоидам [18]. Фармакокинетика соответствует внутримышечному способу введения препарата: анальгетический эффект препарата развивается уже через 20–30 мин после приема 1 таблетки (8 мг) и длится до 4 ч. Таким образом, ксефокам рапид используется в средней дозе 8–16 мг для быстрого купирования выраженного болевого синдрома. Неселективность действия в отношении ЦОГ-1 обусловливает развитие характерных для НПВП нежелательных реакций. Поэтому через 3–5 дней применения ксефокама рапида переходят на прием НПВП с преимущественным действием на ЦОГ-2 — селективных ингибиторов ЦОГ-2 [13, 19]. Механизм их действия обеспечивает высокую эффективность и значительно меньшее количество побочных реакций.
К данной группе относится препарат мовалис (мелоксикам). Проведенные исследования показали, что совокупный риск тяжелых осложнений со стороны желудочно-кишечного тракта (язва, кровотечение) при приеме мовалиса значительно ниже, чем при приеме диклофенака и пироксикама (в 7 и 10 раз соответственно) [13]. Эффект развивается в течение 45 мин — 1 ч после введения препарата и достигает максимума к 3–4-му дню. Препарат выпускается в таблетированной и в инъекционной формах (15 мг мелоксикама/1,5 мл раствора для глубоких внутримышечных инъекций), что позволяет проводить сочетанную терапию. Обычно курс состоит из трех инъекций по 15 мг (1 инъекция в день) и последующего приема препарата в таблетках по 7,5 или 15 мг (1 раз в день).
Нимесил (нимесулид) — избирательный ингибитор ЦОГ-2 — в дозе 100 мг 2 раза в день оказался более эффективен у пациентов с острой болью в спине и менее — с хронической [2]. Благодаря гранулированной форме, препарат обладает высокой биодоступностью; хорошо растворяется, быстро всасывается из желудочно-кишечного тракта и оказывает мощный анальгетический эффект. Прием нимесила снижает интенсивность боли у пациентов с мышечно-тоническим и миофасциальным синдромами уже с 5-го дня лечения; при радикулопатии — с 10-го дня. Существенных побочных эффектов при применении препарата выявлено не было.
Сроки применения НПВП и анальгетиков определяются интенсивностью болевого синдрома, длительность их приема зависит от достижения эффекта. Проводить курсы «профилактического» приема НПВП у больных с дорсопатиями при отсутствии болевого синдрома нецелесообразно, поскольку убедительного превентивного эффекта достичь не удается, тогда как риск осложнений возрастает значительно.
Рекомендуется дополнительное применение НПВП в виде мазей и гелей, способных в определенной степени уменьшать боль при всасывании их под кожу. При этом использование гелей и мази в качестве основного лечения в большинстве случаев не может заменить назначения инъекционных или таблетированных форм НПВП.
Миорелаксанты. Хорошим терапевтическим эффектом обладает комбинация НПВП с миорелаксантами, уменьшающими выраженность рефлекторного мышечно-тонического синдрома. Доказано, что добавление к стандартной терапии (НПВП, лечебная гимнастика) миорелаксантов приводит к более быстрому регрессу боли, мышечного напряжения и улучшению подвижности позвоночника [15, 22]. Курс лечения миорелаксантами составляет несколько недель. В качестве препаратов, снижающих повышенный мышечный тонус, используются производные бензодиазепинов — диазепам, тетразепам; мидокалм (толперизон), сирдалуд (тизанидин). Тизанидин, помимо расслабляющего действия на поперечно-полосатую мускулатуру, обладает умеренным гастропротекторным действием, что немаловажно при комбинации его с НПВП [23].
Коррекция нарушений микроциркуляции
С учетом микроциркуляторных расстройств, развивающихся при грыжах межпозвонковых дисков, особенно осложненных радикулопатией, обязательным является назначение препаратов, улучшающих микроциркуляцию, влияющих на сосудисто-тромбоцитарное звено патогенеза.
Назначают пентоксифиллин по 1 таблетке (0,4 г) 3 раза в день в течение 3–4 нед. Особая ретардированная форма пентоксифиллина — вазонит ретард 600 — предусматривает непрерывное высвобождение активного вещества и его равномерное всасывание из желудочно-кишечного тракта. Максимальная концентрация пентоксифиллина и его активных метаболитов в плазме достигается через 3–4 ч и сохраняется на терапевтическом уровне около 12 ч, что позволяет принимать препарат всего 2 раза в сутки. Включение вазонита в традиционную комплексную терапию дискогенных радикулопатий обеспечивает улучшение кровотока, микроциркуляции и трофики в зоне повреждения; уменьшается выраженность отека корешка, что приводит к постепенному регрессу неврологической симптоматики.
В качестве дополнения к патогенетическому лечению у больных с болью в спине и дискогенными радикулопатиями используются препараты α-липоевой кислоты, в частности берлитион. С одной стороны, α-липоевая кислота (берлитион) улучшает энергетический обмен, нормализует аксональный транспорт, с другой — снижает окислительный стресс, связывая свободные радикалы, подавляя их образование и инактивируя оксиданты, что приводит к восстановлению клеточных мембран. Методом лазерной допплеровской флуометрии доказано непосредственное влияние препарата на капиллярный кровоток (усиление кровотока, уменьшение зоны ишемии и отека), а также на восстановление активности симпатического звена вегетативной нервной системы. Таким образом, берлитион, обладая антиоксидантной, мембранопротекторной, антигипоксической, антиишемической активностью, улучшает микроциркуляцию в зоне поврежденного корешка; уменьшает симптомы радикулопатии, способствует увеличению скорости распространения возбуждения по нервному волокну. Стандартная схема лечения предполагает внутривенное капельное введение раствора берлитиона 300 ЕД на 250 мл физиологического раствора в течение 10 дней, затем — длительную (в течение 2–3 мес) поддерживающую терапию препаратом берлитионом 300 ораль в дозе 600 мг/сут (по 1 таблетке за 20 мин до приема пищи 2 раза в день).
В комплексную терапию грыж межпозвонковых дисков и дискогенных радикулопатий включают актовегин, обладающий антигипоксической, антиоксидантной активностью и улучшающий микроциркуляцию. Актовегин является депротеинизированным гемодиализатом, содержит 30% органических веществ (аминокислоты, нуклеозиды, промежуточные продукты углеводного и жирового обмена, липиды и олигосахариды), а также электролиты и микроэлементы, в том числе магний [22]. Под воздействием актовегина усиливается потребление кислорода и глюкозы, что ведет к повышению энергетического статуса клетки, функционального метаболизма нейронов. Под влиянием препарата значительно улучшается диффузия кислорода в нейрональных структурах, что позволяет уменьшить выраженность трофических расстройств [22]. Отмечаются также значительное улучшение периферической микроциркуляции, вазодилатация на фоне улучшения аэробного энергообмена сосудистых стенок и высвобождения простациклина и оксида азота (вторичный эффект). Таким образом, актовегин при грыжах межпозвонковых дисков уменьшает выраженность отека, гипоксии, микроциркуляторных расстройств в зоне поврежденного корешка; оказывает нейротрофическое действие и способствует скорейшему регрессу симптомов радикулопатии.
Показано капельное введение 200–400 мг препарата в течение 10 дней, с последующим переходом на пероральное применение (по 1 драже 3 раза в день внутрь в течение 1–2 мес).
В острый период дорсопатии используют местное воздействие: втирание мазей, компрессы с 30–50% раствором димексида и новокаином, новокаиновые и гидрокортизоновые блокады; электропроцедуры: чрескожную электроанальгезию, синусоидально-модулированные токи, диадинамические токи, электрофорез с новокаином и др.
С той же целью применяется рефлексотерапия (иглоукалывание, прижигание, электроакупунктура, лазеротерапия), гирудотерапия.
По мере стиханий острых явлений постепенно наращивают двигательную активность, назначают упражнения на укрепление мышц поясничного отдела, лечебную физкультуру, массаж, мануальную терапию, бальнеотерапию.
В случае хронизации болевого синдрома к терапии подключают препараты, оказывающие воздействие на структуру хрящевой и костной тканей, улучшающие микроциркуляцию, антидепрессанты.
Хондропротекторы. В базисную терапию остеохондроза включают так называемые хондропротекторы — препараты, положительно влияющие на структуру хрящевой ткани, активирующие анаболические процессы в матриксе хряща, снижающие активность лизосомальных ферментов, стимулирующие хондроциты. Эти лекарственные средства (дона, структум и др.) содержат естественные компоненты суставного хряща и повышают резистентность хондроцитов к воздействию провоспалительных цитокинов. Схема лечения препаратом дона подразумевает длительный, непрерывный курс в течение 3–6 мес с дозой 1 пакетик (1,5 г) порошка в сутки.
Препараты витамина D и кальция. Большое значение при лечении болевого синдрома приобретают препараты на основе витамина D, его активных метаболитов и производных, оказывающие положительное влияние на костную ткань. Наиболее изучен альфа Д3-тева (альфакальцидол), применяющийся у пациентов с дорсопатиями и хроническими болями в спине на фоне остеопении и остеопороза [3, 4, 11]. Являясь пролекарством, альфакальцидол превращается в организме в D-гормон (кальцитриол), оказывает положительное влияние на ремоделирование костной ткани, поддержание кальциевого гомеостаза, улучшение нервно-мышечной проводимости и сократимости двигательных мышц.
Прием альфа Д3-тева в дозе 0,5–1,0 мкг в сутки в течение 6 мес достоверно увеличивает массу костной ткани, улучшает показатели костного метаболизма, увеличивает объем движений и повышает качество жизни. Доказано анальгетическое действие данного препарата при лечении хронического болевого синдрома в пояснице [3, 9, 11].
Кальций-Д3 Никомед — комбинированный препарат, регулирующий обмен кальция или фосфора в организме. Одна жевательная таблетка содержит активные компоненты: кальция карбоната — 1250 мг (что соответствует 500 мг элементарного кальция), колекальциферола (витамина D3) — 200 МЕ. При длительном (до 3–6 мес) приеме препарат достоверно увеличивает плотность костной ткани, восполняя недостаток кальция и витамина Д в организме. Кальций-Д3 Никомед хорошо переносится, что позволяет использовать его у лиц пожилого возраста с различными сопутствующими заболеваниями внутренних органов [9].
Антидепрессанты. Затянувшийся болевой синдром, хронизация боли, изменение походки, невозможность заниматься привычной деятельностью, необходимость введения самоограничений, болезненная терапия (инъекции, мануальная терапия) могут приводить к развитию посттравматического стрессового расстройства, депрессивных расстройств невротического круга, ипохондрических расстройств, тревожно-депрессивным реакциям при расстройстве адаптации. В связи с этим увеличиваются сроки выздоровления, ограничиваются возможности двигательной реабилитации больных. Методики рациональной, когнитивной и когнитивно-поведенческой терапии, аутогенная тренировка с биологической обратной связью способствуют адаптации пациентов, выходу из депрессии [10]. Наряду с психотерапевтической реабилитацией назначают антидепрессанты, причем желательно использовать препараты, оказывающие седативный и миорелаксирующий эффекты. Этим требованиям отвечают классические трициклические антидепрессанты (например, амитриптилин), однако большое количество побочных эффектов ограничивают их длительное применение.
Селективные ингибиторы обратного захвата норадреналина и серотонина в синапсах лишены побочных эффектов трициклических антидепрессантов. Помимо антиноцицептивного действия, они хорошо корригируют депрессию, тревогу, расстройства сна у пациентов с болевым синдромом на фоне грыж межпозвонковых дисков. Появившийся в прошлом году на фармацевтическом рынке препарат симбалта (дулоксетин) показал в открытых и плацебо-контролируемых исследованиях быстрое купирование эмоциональных и соматических симптомов, нейропатической боли. Симбалта уже в начальных дозах (40 мг/сут) оказывает сбалансированное и мощное влияние на обратный захват серотонина и норадреналина, участвует в модуляции нисходящих болевых путей [27]. Это, в свою очередь, обеспечивает высокую эффективность в лечении хронической боли. Селективность действия ограничивает возможность развития нежелательных реакций. Рекомендуемая схема применения дулоксетина при хроническом болевом синдроме — 60–120 мг в сутки в течение 3–6 мес.
При хроническом течении рефлекторных синдромов и радикулопатий наиболее эффективны физиотерапевтическое лечение, НПВП, миорелаксанты, мануальная терапия, рефлексотерапия и санаторно-курортное лечение.
У многих больных с длительным течением болевого синдрома хорошие результаты дает применение антидепрессантов в комбинации с другими методами терапии.
Хирургическое лечение (удаление грыжи диска) показано при дискогенной радикулопатии, сопровождающейся выраженным парезом, присоединяющейся клинике радикуломиелоишемии, при отсутствии эффекта от консервативного лечения в течение 3 мес, а также при выраженном стенозе позвоночного канала.
В качестве профилактики обострений остеохондроза рекомендуется избегать провоцирующих факторов (подъем больших грузов, ношение тяжелой сумки в одной руке, переохлаждение и др.), регулярно заниматься лечебной гимнастикой.
Таким образом, боли в пояснично-крестцовом отделе позвоночника часто вызваны грыжей межпозвонкового диска, проявляющейся компрессионными и рефлекторными синдромами. Важное место в патогенезе занимают расстройства микроциркуляции. В случае нетипичного болевого синдрома в пояснице необходимо дополнительное обследование для исключения остеопороза, онкологического, воспалительного и соматического заболеваний, а также травмы спины. Выявление дегенеративно-дистрофических изменений позвоночника, по данным рентгенографии, не исключает других причин боли в спине. При лечении рефлекторных синдромов остеохондроза, миофасциальных болей в остром периоде эффективны покой, применение НПВП и миорелаксантов, следует избегать болезненных поз и физических нагрузок. При лечении хронических вертеброгенных болевых синдромов существенный эффект может быть получен от применения антидепрессантов.
Литература
Т. Т. Батышева, доктор медицинских наук
Л. В. Багирь
З. В. Кузьмина
А. Н. Бойко, доктор медицинских наук, профессор
Поликлиника восстановительного лечения № 7 УЗ ЦАО, РГМУ, Москва


