Что лучше кветиапин или азалептин
Основными показаниями для смены проводимой антипсихотической терапии и перевода больных на рисполепт являются:
— недостаточная эффективность и резистентность к проводимой нейролептической терапии;
— высокий риск рецидивов,
— плохая переносимость классических нейролептиков,
— риск развития поздней дискинезии;
— отказ больного от приема других нейролептиков;
— несоблюдение больным режима приема антипсихотической терапии классическими нейролептиками (отсутствие комплаентности);
— подростковый и юношеский возраст пациентов, имеющих относительно благоприятный прогноз;
— патологические изменения в крови у пациентов, принимающих клозапин
Рикошетные психозы проявляются внезапным появлением психомоторного возбуждения, которое носит характер кататоно-гебефренного или маниакально-гебефренного психоза. В основе патогенеза данных состояний, как принято считать, лежит гиперчувствительность мезолимбических дофаминовых рецепторов. Эти психозы возникают через более короткий промежуток времени, чем при обострении психотической симптоматики вследствие недостаточности антипсихотической терапии. При купировании данных состояний рекомендуется увеличение дозы рисполепта, с возможным дополнительным назначением нейролептиков с выраженным седативным действием (аминазина).
Появление рикошет-дискинезий обусловлено изменением соотношения концентрации нейролептиков и их активных метаболитов в плазме крови на фоне уменьшения или отмены предшествующей антипсихотической терапии. Для профилактики данных явлений рекомендуется уменьшение дозы антипаркинсонических препаратов только спустя 2 недели после уменьшения нейролептической терапии. В отдельных случаях при уменьшении дозы нейролептика требуется временное увеличение дозы корректоров и дополнительное назначение бензодиазепинов.
Холинергический рикошет-эффект отмечается при относительно быстрой отмене нейролептиков с выраженным антихолинергическим действием (клозапин, оланзапин, хлорпромазин, сонапакс, хлорпротиксен, неулептил) и проявляется нарушением сна, ажитацией, гриппоподобными симптомами, повышенным потоотделением, ощущением подъема или понижения температуры тела, спутанностью сознания, головной болью, расстройствами желудочно-кишечного тракта (тошнота, рвота, диарея, анорексия). Для предотвращения данного рикошет-эффекта рекомендуется постепенная отмена вышеуказанных нейролептиков с сохранением, а при необходимости дополнительном назначении холинолитических (антипаркинсонических) препаратов. При купировании подобных состояний акцент делается на холинолитических препаратах и дополнительном назначении бензодиазепинов.
Длительность периода перевода определяется индивидуально в зависимости как от психического и соматического статуса больного, так и от дозы и типа предшествующего антипсихотика, возможности регулярного наблюдения за больным. Возраст пациента также играет немаловажную роль, применяемые препараты нуждаются в медленной отмене у детей и пожилых пациентов. Период смены терапии может достигать 4-5 недель при переводе с классических нейролептиков, и 7-8 недель при переводе с клозапина и оланзапина.
Существует три основных способа перевода на терапию рисполептом.
Перевод с монотерапии пероральных форм классических нейролептиков:
Скорость и способ перевода с монотерапии пероральных форм нейролептиков зависит как от дозы препарата, так и выраженности его холинергических эффектов. При аналогичных дозах наиболее быстро производится отмена нейролептиков с низкой антихолинергической активностью (галоперидол, триседил, тизерцин, трифтазин, этаперазин, мажептил, модитен). Нейролептики, обладающие высокой антихолинергической активностью (аминазин, клопиксол, флюанксол, пипортил, сонапакс, неулептил, хлорпротиксен), отменяются постепенно, так как здесь велик риск возникновения холинергических рикошет-эффектов.
Перевод с депонированных форм нейролептиков:
При переводе больных с депонированной формы нейролептиков, рисполепт назначается за неделю до даты следующей инъекции депо, так чтобы к моменту предполагаемой инъекции препарат достиг терапевтических доз. Снижение дозы сопутствующей холинолитической (антипаркинсонческой) терапии должно занять более длительный период (до 4 недель), при отсутствии экстрапирамидных побочных эффектов, непосредственно связанных с терапией рисполептом.
Перевод с комбинированной терапии несколькими нейролептиками:
Проведение антипсихотической терапии одновременно несколькими нейролептиками достаточно распространено в отечественной практике. Если в ряде случаев это является «терапией отчаяния», то в других случаях этот метод представляется недостаточно обоснованным. Перевод с комбинированной терапии должен производиться постепенно, опираясь на некоторые принципиальные положения. Оптимальным методом для перевода на терапию рисполептом представляется метод «перекреста», когда до назначения рисполепта производится частичная отмена одного из нейролептиков. В первую очередь необходимо производить постепенную отмену нейролептиков с низкой антихолинергической активностью (галоперидол, триседил, тизерцин, трифтазин, этаперазин, мажептил, модитен). Нейролептики, обладающие высокой антихолинергической активностью (аминазин, сонапакс, неулептил, пипортил, хлорпротиксен, клопиксол, флюанксол), рекомендуется отменять после подбора терапевтической дозы рисполепта при стабильном состоянии больного. Холинолитические препараты (циклодол, акинетон и др.) необходимо начинать отменять через 2 недели после полной отмены традиционных нейролептиков при отсутствии клинических проявлений нейролепсии.
При переводе на терапию рисполептом с комбинированной терапии депонированных и пероральных форм нейролептиков, в первую очередь рекомендуется производить отмену пероральных форм. Скорость отмены зависит от дозы препарата и выраженности его антихолинергических свойств. Оптимальным здесь также будет метод «перекреста», когда уменьшение дозы таблетированных нейролептиков производиться до назначения рисполепта. Отмена депонированного нейролептика производится после достижения терапевтической дозы рисполепта. При этом в отдельных случаях предпочтительным может быть первоначальное уменьшение дозы депонированного нейролептика и увеличение интервала между инъекциями.
Перевод с терапии клозапином (азалептином):
Резкая отмена терапии клозапином методом «обрыва» возможна при появлении выраженных патологических изменений в картине крови и осложнений соматического характера. В этом случае врач должен быть готов к купированию выраженного психотического обострения, которое должно трактоваться в рамках синдрома отмены клозапина. Для предупреждения развития данного состояния необходимо быстрое увеличение дозы рисполепта. Однако в связи с отсутствием у рисполепта холинолитического и выраженного седативного эффекта необходимо временное назначение как холинолитических препаратов (антипаркинсонических), так и бензодиазепинов или седативных антипсихотиков (аминазина, хлорпротиксена). Прекращение контроля крови у больных, получающих клозапин, рекомендуется не менее чем через 3 недели после полной его отмены. Необходимо помнить, что у ряда больных, получающих длительное время высокие дозы клозапина, не удается произвести его полную отмену из-за ухудшения психического состояния. В этих случаях нередко оптимальной становится комбинированная терапия рисполептом и клозапином, который будет назначаться уже в более низких дозах.
Перевод с терапии оланзапином (зипрексой)
Общие принципы смены терапии здесь аналогичны переводу с терапии клозапином. Оланзапин, также как и клозапин, обладает выраженным антихолинергическим и седативным действием. Отмена оланзапина должна производиться постепенно, в течение нескольких недель в зависимости от дозы и длительности приема оланзапина. При резкой отмене оланзапина нередко имеет место возникновение как рикошетных психозов, так и рикошетных холинергических эффектов. На период отмены рекомендуется назначение холинолитических препаратов и бензодиазепинов.
Перевод с терапии кветиапином (сероквелем):
Кветиапин, так же как и оланзапин. относится к атипичным нейролептикам клозапиновой группы. Препарат обладает антихолинергическим эффектом, однако этот эффект у него менее выражен, чем у других препаратов данной группы. Риск появления рикошет-реакций может рассматриваться при переводе с высоких доз кветиапина. Холинолитическая терапия добавляется только при отмене высоких доз кветиапина. Предпочтительными способами перевода с кветиапина являются «наложение» и «перекрест».
Во всех случаях смены нейролептической терапии и переводе больных на терапию рисполептом необходимо помнить, что способ перевода и доза рисполепта определяются индивидуально, зависят от психического и соматического состояния пациента, основываются на безопасности клинической дозы препарата. Применение бензодиазепинов может быть показано на начальных стадиях смены терапии, но оно не должны длиться дольше, чем 2-3 недели терапии рисполептом.
Что лучше: Кветиапин или Азалептин
Кветиапин
Азалептин
Исходя из данных исследований, Азалептин лучше, чем Кветиапин. Поэтому мы советуем выбрать его.
Но не забывайте, что у данных препаратов в составе разные активные вещества. Поэтому обязательно проконсультируйтесь с врачом. Возможно, какой-то из них может не подойти для вашей терапии.
Сравнение эффективности Кветиапина и Азалептина
У Азалептина эффективность больше Кветиапина – это означает, что способность лекарственного вещества оказывать максимально возможное действие разное.
Например, если терапевтический эффект у Азалептина более выраженный, то у Кветиапина даже в больших дозах добиться данного эффекта невозможно.
Также скорость терапии – показатель быстроты терапевтического действия у Азалептина и Кветиапина тоже разное, как и биодоступность – количество лекарственного вещества, доходящее до места его действия в организме. Чем выше биодоступность, тем меньше его потерь будет при усвоении и использовании организмом.
Сравнение безопасности Кветиапина и Азалептина
Безопасность препарата включает множество факторов.
При этом у Кветиапина она достаточно схожа с Азалептином. Важно, где метаболизируется препарат: лекарственные вещества выделяются из организма либо в неизмененном виде, либо в виде продуктов их биохимических превращений. Метаболизм протекает спонтанно, но чаще всего задействует основные органы, такие как печень, почки, лёгкие, кожу, мозг и другие. При оценивании метаболизма у Кветиапина, также как и у Азалептина мы смотрим, какой орган является метаболизирующим и наколько критично действие на него.
Соотношение риска к пользе – это когда назначение лекарственного препарата нежелательно, но оправдано при определенных условиях и обстоятельствах, с обязательным соблюдением осторожности применения. При этом у Кветиапина нет никаих рисков при применении, также как и у Азалептина.
Также при рассчете безопасности учитывается проявляются ли только аллергические реакции или же возможная дисфункция основных органов. В прочем как и обратимость последствий от использования Кветиапина и Азалептина.
Сравнение противопоказаний Кветиапина и Азалептина
Исходя из инструкции. Количество противопоказаний у Азалептина в пределах нормы, но оно больше чем у Кветиапином. Это и перечень симптомов с синдромами, и заболевания, различные внешних и внутренние условия, при которых применение Азалептина или Кветиапина может быть нежелательным или недопустимым.
Сравнение привыкания у Кветиапина и Азалептина
Как и безопасность, привыкание тоже включает множество факторов, которые необходимо учитывать при оценивании препарат.
Так совокупность значения таких параметров, как «cиндром отмены» и «развитие резистентности», у Кветиапина достаточно схоже со аналогичными значения у Азалептина. Синдром отмены – это патологическое состояние, возникающее после прекращения поступления в организм веществ, вызывающих привыкание или зависимость. А под резистентностью понимают изначальную невосприимчивость к препарату, этим она отличается от привыкания, когда невосприимчивость к препарату развивается в течение определенного периода времени. Наличие резистентности можно констатировать лишь в том случае, если была сделана попытка увеличить дозу препарата до максимально возможной. При этом у Кветиапина значения «синдрома отмены» и «резистентности» достотачно малое, впрочем также как и у Азалептина.
Сравнение побочек Кветиапина и Азалептина
Побочки или нежелательные явления – это любое неблагоприятное с медицинской точки зрения событие, возникшее у субъекта, после введения препарата.
У Кветиапина состояния нежелательных явлений почти такое же, как и у Азалептина. У них у обоих количество побочных эффектов малое. Это подразумевает, что частота их проявления низкая, то есть показатель сколько случаев проявления нежелательного эффекта от лечения возможно и зарегистрировано – низкий. Нежелательное влияние на организм, сила влияния и токсическое действие у Кветиапина схоже с Азалептином: как быстро организм восстановиться после приема и восстановиться ли вообще.
Сравнение удобства применения Кветиапина и Азалептина
Это и подбор дозы с учетом различных условий, и кратность приемов. При этом важно не забывать и про форму выпуска препарата, ее тоже важно учитывать при составлении оценки.
Удобство применения у Азалептина лучше, чем у Кветиапина.
Рейтинг препаратов составлен опытными фармацевтами, изучающий международные исследования. Отчет сгенерирован автоматически.
Дата последнего обновления: 2020-12-04 13:42:56
Замена одного нейролептика на другой
Смена нейролептика из-за отсутствия эффективности
Смена нейролептика из-за побочных эффектов
Проблема переносимости одна из основных причин смены нейролептика : экстрапирамидные побочные эффекты, не поддающиеся противопаркинсонической терапии ( поздняя дискинезия, постоянные когнитивные нарушения, стойкая седация, нарушения обмена веществ, увеличение QT, другие раздражающие побочные эффекты, например, сексуальная дисфункция.
Следующие побочные эффекты являются наиболее раздражающими для пациентов (или наиболее клинически значимыми для психиатра) : экстрапирамидные симптомы, увеличение веса, когнитивные расстройства, седативный эффект, расстройства, связанные с гиперпролактинемией, сексуальная дисфункция, депрессия, агранулоцитоз и метаболические нарушения. Побочные эффекты являются важной причиной перехода при лечении детей и подростков, где такие эффекты более выражены, чем у взрослых. В этой популяции особенно значительны побочные эффекты, связанные с гиперпролактинемией и увеличением веса.
Другие причины смены нейролептика
Осложнения при смене нейролептика
Как часто меняют один нейролептик на другой
Противопоказания для смены нейролептика
Бег по кругу
Фармакокинетика и фармакодинамика при смене нейролептиков
Антипсихотические препараты метаболизируются в основном в печени системой цитохрома p450, поэтому они могут взаимодействовать с другими лекарственными средствами, которые действуют как ингибиторы их основного метаболического пути или сами являются его субстратами, поскольку может происходить взаимодействие из-за конкурентного ингибирования.
Единственным атипичным антипсихотиком, от которого не ожидается серьезных проблем взаимодействия на уровне цитохрома p450, является палиперидон. Этот препарат продемонстрировал in vitro, что он существенно не ингибирует изоферменты CYP1A2, CYP2A6, CYP2C8 / 9/10, CYP2D6, CYP2E1, CYP3A4 и CYP3A5. Палиперидон также не является субстратом CYP1A2, CYP2A6, CYP2C9 или CYP2C19, и, похоже, CYP2D6 и CYP3A4 лишь минимально участвуют в его метаболизме. например). Можно также также использовать этот путь (например, рисперидон, арипипразол и клозапин) или путь изофермента 1A2 (например, клозапин и оланзапин).
Почти незаменимый клозапин
Смена нейролептиков с аналогичной активностью по отношению к рецепторам
Стратегии преход с одного нейролептика на другой
Традиционно используют три схемы переключения с одного нейролептика на другой. Резкое переключение; немедленное прекращение приема предыдущего антипсихотического средства и начало приема нового нейролептика в обычных дозировках. Поперечное сужение; начало постепенного увеличения дозировки нового нейролептика с одновременным постепенным прекращением приема предыдущего антипсихотического средства. Перекрытие и прерывание; поддержание дозировки предыдущего антипсихотического средства и в то же время постепенное введение нового антипсихотического средства; как только будет достигнута эффективная дозировка нового нейролептика, предыдущий антипсихотик постепенно отменяется.
Какая стратегия перехода лучше
Как менять конкретные нейролептики?
Что делать с негативной симптоматикой?
Как бороться с экстрапирамидной симптоматикой?
По моему мнению, переход на кветиапин значительно улучшает симптомы паркинсонизма и акатизии, но не симптомы поздней дискинезии. И респиридон и оланзапин ослабляют паркинсонизм и позднюю дискинезию, но не акатизию, и не было обнаружено различий между двумя препаратами с точки зрения их воздействия на оцениваемые экстрапирамидные симптомы ( оба препарата вызывают дозозависимые экстрапирамидные побочные эффекты, но респиридон более ). Кроме того, результаты двух метаанализов показывают, что использование противопаркинсонических препаратов значительно меньше связано с кветиапином, чем с рисперидоном, оланзапином и зипразидоном. Другим вариантом переключения у пациентов с поздней дискинезией может быть клозапин, который доказал свою эффективность, несмотря на отсутствие рандомизированных клинических испытаний в этой области, и некоторые авторы считают его лечением выбора в этих случаях.
Сбросить лишний вес
Снизить пролактин
В рандомизированном клиническом исследовании пациентов с шизофренией и гиперпролактинемией, которые лечились рисперидоном или обычными нейролептиками, переход на оланзапин сопровождался возвращением к нормальному уровню пролактина через 4 месяца у 90% пациентов, по сравнению с ни одним из пациентов, которые продолжали принимать предыдущий антипсихотик. Считается, что оланзапин имеет очень небольшую тенденцию вызывать гиперпролактинемию, но краткосрочные клинические испытания на взрослых показали, что уровень пролактина повысился с нормального до повышенного у 30% пациентов, получавших оланзапин, по сравнению с 10% пациентов, получавших плацебо ; у подростков эти показатели были увеличены до 47% и 7% для оланзапина и плацебо соответственно. Согласно метаанализу, оланзапин повышал уровень пролактина несколько больше, чем арипипразол, клозапин и кветиапин. Эти данные позволяют предположить, что оланзапин следует рассматривать как вторичный вариант для замены антипсихотических препаратов у пациентов с гиперпролактинемией.
Зачем нужны сексуальные расстройства
В единственном рандомизированном клиническом исследовании, проведенном на сегодняшний день, пациенты с сексуальной дисфункцией, связанной с терапией рисперидоном, были переведены на кветиапин; Через 6 недель не было значительных различий между пациентами, которые перешли на другой прием, и теми, кто продолжал принимать рисперидон, с точки зрения сексуальной функции. Если оставить в стороне эти обескураживающие результаты, кветиапин и оланзапин являются антипсихотиками, которые оказались наиболее устойчивыми и последовательными, то есть в рандомизированных клинических испытаниях, в отношении более низкой частоты сексуальной дисфункции. Другие авторы обнаружили, что кветиапин, зипразидон и арипипразол были лекарствами, связанными с более низкой частотой сексуальной дисфункции как в целом, так и в большинстве измерений. Таким образом, кветиапин, оланзапин, зипразидон и арипипразол можно считать лучшими вариантами замены антипсихотических препаратов у пациентов с сексуальной дисфункцией.
Смена нейролептика в нашей клинике
Атипичные антипсихотики в терапии биполярного расстройства
Проблема терапии биполярного расстройства (БАР) является одной из самых обсуждаемых тем в психиатрической литературе в последнее время. Мнения меняются в отношении большинства аспектов этого заболевания – определения, механизмов развития и способов терапевтического вмешательства.
БАР, несмотря на приступообразное хроническое течение, стали признавать потенциально излечимым заболеванием.
Однако не существует единого и идеального препарата для его лечения. Терапевтическое средство должно обладать свойством купирования острых состояний (мании, депрессии или смешанного состояния), а также поддержания достигнутой ремиссии и предотвращения последующих эпизодов. Для многих больных БАР основные применяемые при этом заболевании препараты оказываются неэффективными. Так, в течение двухлетнего периода только у половины лиц с БАР формируется состояние ремиссии. Более того, у 50% больных в течение того же периода возникают обострение или новый эпизод.
Последние десять лет ознаменовались новыми достижениями как в медикаментозном, так и в психотерапевтическом аспектах терапии БАР. Важнейшим нововведением стало признание того, что антипсихотические препараты (АП) II поколения (атипичные антипсихотики) эффективны в отношении маниакальных состояний, а некоторые из них – и депрессивных, а также обладают свойством предотвращать последующие приступы.
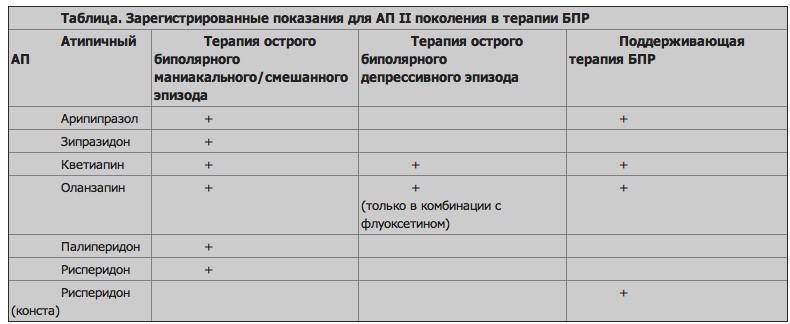
После успешного применения в 80х гг. клозапина у больных шизофренией, резистентных к лечению, были получены аналогичные результаты и для резистентных пациентов с БАР. С этого времени большинство возникавших атипичных АП испытывались в терапии мании с постоянной положительной результативностью, которая привела к регистрации рисперидона, палиперидона, оланзапина, кветиапина, зипразидона и арипипразола как антиманиакальных средств (таблица).
Для того чтобы признать атипичные АП стабилизаторами настроения, необходимо получить ответы на следующие вопросы:
Рисперидон
Относительно рисперидона, в области терапии БАР известно единственное двойное слепое контролируемое плацебо исследование эффективности и переносимости монотерапии препаратом острого маниакального состояния продолжительностью 3 недели. Существенное улучшение состояния по шкале мании Янга (YMRS) отмечено в группе рисперидона по сравнению с таковой плацебо, частота экстрапирамидных побочных явлений была выше в группе рисперидона. Прибавка в весе в группе рисперидона в среднем составила 1,6 кг, а в группе плацебо изменение было отрицательным – 0,25 кг.
Оланзапин
Что касается оланзапина, известно несколько контролируемых двойных слепых исследований терапии препаратом острого маниакального состояния в сравнении как с плацебо, так и со стандартными активными препаратами – литием, антиконвульсантами и антипсихотиками. Улучшение по шкале YMRS в группе оланзапина отмечалось с первых недель исследований, к концу испытаний было выше, чем в группе плацебо, и не уступало активным препаратам сравнения. Необходимо отметить, что частота экстрапирамидных побочных явлений в группе оланзапина была не выше, чем в группе плацебо.
При сравнении со стандартными стабилизаторами в терапии маниакальных состояний оланзапин не уступал вальпроатам в эффективности, по достигнутым параметрам качества жизни, а также частоте сообщенных побочных явлений. При сопоставлении с терапией литием скорость формирования терапевтического ответа, а также динамика по шкале общего клинического впечатления свидетельствовали в пользу оланзапина.
При прямом сравнении с рисперидоном показатели эффективности и удовлетворения проводимым лечением были сопоставимы. Однако количество больных, преждевременно прекративших прием препарата, было выше в группе рисперидона.
При проведении поддерживающей терапии оланзапин оценивали в рамках 48недельного исследования в сравнении с плацебо. Частота обострений и время появления первого обострения свидетельствовали в пользу оланзапина (174 дня в сравнении с 22 в группе плацебо).
Даже у больных с проявившимся обострением в группе оланзапина выраженность аффективного приступа была существенно ниже. При лечении депрессивной фазы БАР оланзапин сравнивали с плацебо как в монотерапии, так и в комбинации с флуоксетином. Эффективными оказались как монотерапия, так и сочетание с антидепрессантом с более выраженным улучшением в последнем случае.
За 8-недельный период состояния ремиссии достигли 24,5% больных в группе плацебо, 32,8% – в группе получавших монотерапию оланзапином и 48,8% – комбинацию оланзапина и флуоксетина.
Таким образом, опубликованные данные подтверждают эффективность оланзапина в купировании мании, а также его эквивалентность или превосходство при сопоставлении со стандартными стабилизаторами. Более того, стабилизирующие свойства оланзапина подтверждены позитивными результатами терапии биполярной депрессии, особенно в комбинации с антидепрессантом. В плане переносимости и безопасности, во всех исследованиях отмечались повышение веса и некоторые лабораторные показатели метаболического синдрома.
Кветиапин
Интересно, что в рамках изучения атипичных антипсихотиков как потенциальных стабилизаторов в терапии БАР история применения кветиапина занимает особое место. Дизайны исследований с применением этого препарата планировались таким образом, чтобы ответить на вопросы, связанные с проблемами безопасности и переносимости в данной популяции больных. И клинический опыт, и результаты научных исследований указывают на корреляцию между аффективной симптоматикой и вероятностью формирования экстрапирамидных побочных явлений при применении антипсихотиков.
Готовность лиц с БАР соблюдать рекомендованный режим лечения с применением антипсихотиков как в активной, так и в поддерживающей терапии в значительной степени определяется отсутствием побочных двигательных нарушений (возможно, в большей степени, чем у больных шизофренией). Атипичные антипсихотики как фармакологический класс по своим фармакодинамическим и фармакокинетическим свойствам, вероятно, являются наиболее неоднородными среди всех психотропных препаратов.
Основное антипсихотическое действие кветиапина по блокированию D2-рецепторов отличается гибкостью и чувствительностью к колебаниям концентрации свободного дофамина, в частности, в нигростриарной системе. Именно поэтому кветиапин, в отличие от многих других антипсихотиков, не просто не вызывает экстрапирамидных нарушений, а даже обладает способностью снижать уровень уже присутствующих подобных симптомов.
Vieta et al показали, что в контролируемых плацебо исследованиях монотерапии кветиапином острой мании проявлялось существенное улучшение (по шкале YMRS) уже на 4-й день после начала лечения, и этот эффект поддерживался и нарастал в течение всех 12 недель исследования. Однако не менее важным было то, что подавляющее большинство больных в группе кветиапина не прекращали терапию, поскольку сообщаемые побочные явления были непродолжительными и невыраженными.
Особенно важными стали результаты контролируемых проспективных исследований кветиапина в лечении биполярной депрессии. По переносимости монотерапия кветиапином была не хуже, чем терапия плацебо, но во многом превосходила ее по эффективности. Результаты исследования Calabrese et al. монотерапии кветиапином депрессивного состояния при БАР I и II типа оказались настолько сенсационными, что с целью перепроверки оно было проведено повторно другой группой. Терапия в обоих рукавах активного препарата кветиапина с фиксированными дозировками 300 и 600 мг/сут оказалась существенно эффективнее по сравнению с плацебо, но не различалась ни по эффективности, ни по переносимости.
Улучшение отмечалось в обеих группах, начиная с первой недели. Эти исследования лечения биполярной депрессии с применением кветиапина поставили под сомнение абсолютность утверждения, что кветиапин в активной фазе и в противорецидивной терапии эффективен в дозе 400 мг/сут.
Данное утверждение основывалось на результатах проспективных и ретроспективных исследований применения кветиапина при шизофрении. Результативность терапии биполярных больных при дозировке кветиапина 300 мг/сут скорее отражает благоприятный профиль переносимости препарата, чем его эффект непосредственно на симптомы мании.
В процессе исследований частота инверсии фазы была незначительной. Последнее особенно важно, поскольку при применении некоторых антидепрессантов при подобных состояниях переключение настроения возникает у 310% пациентов.
В одной из последних публикаций сообщается о результатах сравнения эффективности лития и кветиапина в лечении биполярной депрессии. В этом контролируемом плацебо исследовании кветиапин существенно превосходил плацебо, а терапия литием не отличалась по эффективности от плацебо.
В масштабном проспективном открытом 4-летнем исследовании профилактической эффективности кветиапина указывалось на впервые описанную возможность предотвращать не только развернутые эпизоды депрессии, но и подпороговые, субклинические колебания депрессивного спектра, что не отмечалось при терапии литием – классическим средством для профилактики БАР. А применение кветиапина в комбинации с литием или вальпроатами позволило 80% больных оставаться в состоянии ремиссии на протяжении всего периода исследования. Такой уровень выживаемости пациентов при БАР ранее никогда не описывался.
Механизм стабилизирующего и антидепрессивного действия кветиапина остается неясным. Тем не менее, для активного метаболита кветиапина – норкветиапина – описано высокое сродство к рецепторам 5HT2A (постсинаптическим серотонинергическим). Похожее действие в виде перенастройки (снижения чувствительности) этих рецепторов описано для современных антидепрессантов (селективных ингибиторов обратного захвата серотонина [СИОЗС] и селективных ингибиторов обратного захвата серотонина и норадреналина) и электросудорожной терапии.
Подобное влияние на эти рецепторы связывают с анксиолитическим и антидепресивным эффектами. Также норкветиапин влияет на выделение норадреналина и серотонина в синаптическую щель и обладает свойством частичного агонизма к серотонинергическим рецепторам 5HT1A, повышение активности которых связывают с непосредственным антидепрессивным эффектом.
Также можно говорить и об опосредованном антидепрессивном действии препарата, поскольку его сродство к 5HT2Cрецепторам вызывает высвобождение дофамина в лобной коре. Тут же следует отметить возможное действие препарата на глутаматергические проводящие пути.
Зипразидон
Известно два контролируемых плацебо исследования применения зипразидона в терапии острого маниакального состояния. Необходимо отметить раннее появление эффекта в группе зипразидона (на 2й день), однако количество побочных явлений (хотя и невыраженных) было достаточно высоким. Интересно, что рецепторный (фармакодинамический) профиль зипразидона потенциально не менее обещающий, чем у кветиапина, но количество и характер жалоб, сообщенных биполярными больными в реальной клинической практике, удерживает от позиционирования этого препарата в лечении биполярной депрессии.
Арипипразол
Весьма поучительными выглядят результаты применения в терапии БАР арипипразола – одного из самых современных антипсихотических препаратов. Фармакологически он является частичным агонистом дофаминовых рецепторов. Арипипразол, как и ожидалось, отлично себя зарекомендовал в контролируемых плацебо исследованиях при терапии маниакального полюса БАР. Эффективность проявлялась рано (к 24-му дню) и поддерживалась на протяжении всего исследования. Арипипразол в активной терапии не вызывал прибавки в весе, в отличие от большинства АП II поколения. Но при этом у больных отмечалось достаточно большое количество экстрапирамидных побочных явлений, особенно акатизии. В исследовании профилактической эффективности зипразидона на протяжении 100 недель частота обострений у пациентов в группе зипразидона была существенно ниже, чем в таковой плацебо. Однако больные в группе зипразидона часто предъявляли жалобы на экстрапирамидную симптоматику. Результаты применения данного препарата при биполярной депрессии, как и ожидалось, показали, что эффект проявлялся очень рано – на 26й день терапии. Однако 52% больных в группе зипразидона прервали лечение преждевременно по причине непереносимости возникшей акатизии и других экстрапирамидных нарушений. В свете приведенных данных трудно ожидать, что биполярные больные в реальной клинической практике будут испытывать приверженность к терапии арипипразолом.
В целом можно считать, что АП II поколения эффективны в терапии обоих полюсов БАР и, как минимум, не уступают стандартным стабилизирующим средствам. Необходимо отметить, что при испытании АП II поколения в лечении БАР, в отличие от трициклических антидепрессантов и нейролептиков (АП I поколения), частота случаев инверсии фазы (переключения аффективной полярности) не отличалась от таковой при применении плацебо.
В лечении маникальной фазы существенным преимуществом атипичных АП стало более раннее проявление терапевтического эффекта (на 24й день) по сравнению как с плацебо, так и со стандартными препаратами сравнения – литием, карбамазепином и, в некоторых случаях, вальпроатами. Профиль переносимости атипичных АП в краткосрочных исследованиях активной терапии не уступал таковому у стандартных стабилизаторов, а в случае кветиапина был намного более благоприятным. Результатом такого сочетания ранней эффективности и хорошей переносимости стала меньшая частота преждевременного прекращения лечения биполярными больными.
Только для двух атипичных АП – кветиапина и оланзапина – получены положительные результаты исследований и проведена формальная регистрация как в терапии депрессивной фазы, так и в поддерживающем профилактическом лечении. Именно они могут претендовать на признание стабилизаторами настроения. При этом применение оланзапина в терапии биполярной депрессии рекомендуется только в комбинации с флуоксетином (или другими СИОЗС). Кветиапин может эффективно применяться в монотерапии при биполярной депрессии, а также оказывает положительное действие на профилактическом этапе как в монотерапии, так и в комбинации со стандартными стабилизаторами. Кветиапин стал единственным препаратом с доказанной эффективностью в отношении биполярной депрессии II типа, подпороговой депрессивной симптоматики и биполярной депрессии с частой сменой фаз.
Терапия БАР: рекомендации международных руководств
Как указывалось в начале данного материала, тема БАР является одной из наиболее обсуждаемых в психиатрии с быстро накапливающимся объемом информации, в том числе и из сферы доказательной медицины. Именно поэтому так часто приходится сталкиваться с обновлением практических рекомендаций.
К наиболее признанным руководствам в области БАР относятся регулярно обновляемые материалы следующих профессиональных организаций:
Первые три руководства были обновлены в 2009 г. (WFSBP только для терапии мании), остальные находятся в процессе переработки и ожидаются к публикации в 2010 г. Цели систематического обзора этих рекомендаций, который и так проводится параллельно подготовке руководств, нет. В качестве заключения хотелось бы продемонстрировать значение атипичных АП в современных рекомендациях по терапии БАР.
По данным CANMAT/ISBD, первая линия рекомендованной терапии острого эпизода мании (I уровень доказательности) включает такие шаги.
1. Монотерапия:
2.Комбинированная терапия:
3. Первая линия рекомендованной терапии острого депрессивного состояния при БАР (I уровень доказательности):
4. Первая линия рекомендованной терапии для профилактического поддерживающего лечения (I уровень доказательности):
BAP рекомендует следующий выбор первоначальной терапии эпизода мании или смешанного эпизода.
1. Монотерапия (в скобках уровень доказательности):
2. Выбор первоначальной терапии эпизода мании или смешанного эпизода: комбинированная терапия (в скобках уровень доказательности):
3. Выбор препарата при продолжительной терапии для предотвращения последующего эпизода БАР предполагает рассмотрение монотерапии литием как первоначальной опции. Монотерапия литием более эффективна в предотвращении эпизодов мании (I); продолжительное поддерживающее лечение, в частности литием, существенно снижает риск суицидального поведения у больных БАР (I).
При неэффективности или непереносимости лития необходимо переходить к следующему: