Генетик — о том, можно ли обмануть наследственность и изменить свою ДНК
В конце XX века тогда еще начинающие британские биохакеры совершили настоящий прорыв в генетике и предоставили любому человеку возможность с помощью ДНК-теста узнать больше о своих далеких предках и загадочной наследственности. Тогда, правда, только избранные могли объяснить, зачем и кому это нужно, — генетика была интересна лишь узкой группе специалистов, работающих с редкими заболеваниями. Но теперь за простым любопытством стоит более глобальная задача — разобраться в своей наследственности. А причина этому — надвигающийся тренд на тотальное оздоровление, исцеление и персонализированную медицину.
Сегодня эксперты уже не сомневаются в том, что генетика — основополагающая наука медицины будущего, хотя ее технологии и без того кажутся чем-то из мира научной фантастики. Перспективы развития генетики в России обсудят на площадках форума «БИОТЕХМЕД», который пройдет 16 и 17 сентября в Геленджике. В преддверии этого события «РБК Стиль» пообщался с одним из экспертов форума — врачом-генетиком Екатериной Захаровой — и узнал у нее, как работает ДНК, какие особенности мы можем унаследовать от родителей и безопасно ли вмешательство генетиков в организм.
Екатерина Захарова
Заведующая лабораторией наследственных болезней обмена веществ ФГБНУ «Медико-генетический научный центр им. академика Н.П. Бочкова», член экспертного совета по редким болезням при комитете Государственной думы по охране здоровья
Как устроена клетка
Со школьных времен всем известно, что организм человека состоит из множества клеток, в каждой из которых есть ядро — именно там хранится генетическая информация. Ее мы наследуем от родителей и дальше передаем своим детям. В материальном обличии эта информация представлена в виде той самой нити ДНК — дезоксирибонуклеиновой кислоты. Эта макромолекула была открыта достаточно давно, но то, что именно в ней хранится генетическая информация, стало известно только в XX веке.
Дезоксирибонуклеиновая кислота (ДНК) — макромолекула, которая хранит и передает из поколения в поколение генетическую программу функционирования живых организмов. Биологическая информация в ДНК представлена в виде уникального генетического кода, состоящего из последовательности нуклеотидов.
Говоря о том, зачем нам ДНК и что она делает, можно привести аналогию: каждый белок в нашем организме синтезируется по определенному «рецепту». В нем указано, сколько должно быть аминокислот, в какой последовательности они будут соединяться и куда дальше последуют. В таком случае ДНК — это поваренная книга, в которой записаны рецепты всех наших белков, а мутация — это повреждение белка или изменение текста поваренной книги. Если в рецепте появляется опечатка, то белок получается «неправильный» и не выполняет свои функции должным образом, отчего страдает как клетка, так и весь организм, что приводит к развитию заболевания.
Во всех наших клетках хранятся одинаковые гены. Но функции у клеток разные: одни, например, синтезируют гемоглобин, другие занимаются мышечными белками, третьи — нервными. Это обеспечивается с помощью системы регуляции активности генов: она способна «включать» одни гены и оставлять в молчании другие.
Чем генетика отличается от наследственности
Генетика — большая и очень разнообразная наука. Клиническая генетика изучает, как проявляются наследственные болезни, популяционная — наше происхождение и особенности каждого народа. А вот наследственность — понятие уже более узкое. Люди давно заметили, что есть признаки, которые ярко проявляются у представителей одной семьи и передаются из поколения в поколение.
Если вспомнить живопись и портреты членов династии испанских Габсбургов, то многим сразу придут на ум их наследственные приметы: выступающая «габсбургская губа» и гипертрофированная нижняя челюсть, которая, говорят, даже мешала монарху нормально пережевывать пищу. Совершенно очевидно, что эти признаки связаны с изменениями определенных генов в известном роду.
Что еще хранится в ДНК
Информация, закодированная в ДНК, способна рассказать как о заболеваниях, так и о цвете волос, форме глаз, группе крови и даже вкусовых предпочтениях. Например, в ходе генетических исследований ученые обнаружили, что всех людей можно разделить на две категории: тех, кто любит капусту брокколи, и тех, кто ее просто ненавидит. Оказалось, что у второй группы есть определенные повреждения в гене, ответственные за восприятие этого вкуса, — им брокколи кажется горькой и неприятной.
В ДНК также могут быть записаны наши пагубные привычки, склонность к полноте или употреблению алкоголя. Изменения в некоторых генах делают нас более восприимчивыми к этим факторам. Но, как правило, за них отвечает не один, а сразу множество взаимосвязанных генов. Кроме того, врачи уверены, что более существенную роль в данном вопросе играют воспитание и другие социальные факторы.
Можно ли унаследовать интеллектуальные способности
Считается, что интеллектуальные и эмоциональные способности будущего ребенка определяются большим набором генов, и предсказать, какую именно комбинацию они составят, наука пока не в состоянии. Поэтому утверждать, что у гениальных родителей рождаются только гениальные дети, нельзя. Хотя такой миф до сих пор существует: некоторые женщины даже продолжают выбирать себе избранника, исходя из его интеллектуальных способностей, или искать какого-нибудь выдающегося донора — нобелевского лауреата.
Однако есть теория, согласно которой IQ будущего ребенка в большей степени определяется матерью, поскольку в тех областях мозга, которые отвечают за интеллект, чаще активируется ген, наследуемый от нее. А вот за эмоциональное состояние и характер чаще отвечает отец. И в этом случае нобелевский лауреат может оказаться не самым лучшим кандидатом на отцовство.
Как наследуются болезни
Болезни могут наследоваться по-разному. В некоторых случаях патология должна быть у одного из родителей, который, в свою очередь, передает ее детям (с вероятностью 50%). В других болезнь наследуется только по женской линии, и в итоге страдают ей мальчики, а девочки остаются ее здоровыми носительницами. Есть и заболевания, которые переносят оба родителя — у них больной ребенок может появиться на свет только в 25% случаев.
Кроме того, существует множество патологий, которые не наследуются, а появляются случайным образом. Например, в одной половой клетке матери или отца происходят изменения без особых на то причин, и в семье, где никогда не встречались с генетическими заболеваниями, может родиться малыш с синдромом Дауна (хромосомной патологией) или ахондроплазией — моногенным заболеванием, которое проявляется как карликовость. В такой ситуации одна из главных задач врача-генетика — выяснить, как наследуется болезнь, проинформировать семью о возможных рисках рождения больного ребенка, а также рассказать, что можно сделать, чтобы ребенок родился здоровым.
Наследуются ли онкологические заболевания
Большинство онкологических заболеваний — это мутации в генах. Однако они возникают не в половых, а в соматических клетках и не передаются по наследству. В таком случае на их развитие большое влияние оказывают именно внешние факторы: курение, радиация и канцерогенные химические вещества.
Но, к сожалению, есть отдельные виды онкозаболеваний, к которым приводит мутация в генах: они переходят от родителей к ребенку. Самый известный пример — рак молочной железы, за появление которого отвечают гены BRCA1 и BRCA2. В группу риска попадает подавляющее большинство девушек и женщин, у которых в семье были случаи рака молочной железы, поскольку наличие мутации в генах сильно повышает риск развития этого заболевания в определенном возрасте. Это означает, что рак может появиться вне зависимости от образа жизни, занятий спортом и сбалансированности рациона.
Как разгадать свои гены
Попытаться разобрать загадочную ДНК и узнать больше о своих генах можно при помощи генетических тестов. Как правило, их рекомендуют проводить в первую очередь тем семьям, где уже были зафиксированы случаи наследственных заболеваний. Но есть скрининг-тесты, которые проводятся для всех, вне зависимости от того, есть ли вероятность возникновения наследственного заболевания. Например, сейчас у всех беременных женщин есть возможность сдать анализы на определение генетических заболеваний у эмбриона. Скрининг на раннем сроке проводится специально для того, чтобы определить, входят ли будущая мама и ее малыш в группу риска. Дальше назначаются дополнительные обследования, которые подтверждают или опровергают развитие патологии. В ходе беременности не менее важно своевременно делать УЗИ, потому что пороки развития у плода встречаются намного чаще, чем любые наследственные заболевания.
Будущие родители должны осознавать, что комбинации их генов не всегда могут привести к идеальному результату. Но с некоторыми из наследственных патологий ребенок может жить совершенно нормально, поэтому пугаться их не стоит.
Может ли врач исправить наследственность
Если представить, что врач на начальном этапе сможет скомбинировать гены так, чтобы исправить недочеты в хромосомах будущего ребенка, родители, наверное, согласятся. Хотя стоит взять в расчет то, что часто двигателями прогресса, науки и искусства становятся именно неординарные люди. У талантливых художников, поэтов или музыкантов неоднократно были зафиксированы особенности развития, и если бы отбор по таким критериям существовал сотни лет назад, то мир лишился бы практически всех гениев.
Сейчас мы знаем многое о геноме человека и уже научились читать его последовательность. Но вот понять смысл этого «текста» можем далеко не всегда. Так же, как не всегда знаем, повлияет ли положительно наше вмешательство в структуру одного гена на работу других. Больше того, функция многих участков ДНК до сих пор остается не изучена.
ЭКО и дети из пробирки
Когда начинаешь работать с чем-то малоизвестным (а это часто встречается в генетике), всегда возникает вопрос о том, что делать правильно и этично, а что нет. Сегодня в цивилизованных странах накладывается запрет на генетические манипуляции с половыми клетками, потому что мы не знаем, как их изменения могут передаваться дальше и к каким последствиям это приведет. И, конечно, нельзя проводить эксперименты на живых эмбрионах.
Пока что в случае обнаружения какого-либо генетического заболевания врач может только предложить пренатальную или предимплантационную диагностику — метод, позволяющий произвести генетическую экспертизу одной клетки эмбриона перед процедурой ЭКО (экстракорпорального оплодотворения). Задача такой диагностики — предоставить возможность рождения здоровых детей в семьях, где существует высокий риск рождения ребенка с тяжелыми заболеваниями. Но у любых современных технологий, включая ЭКО, есть свои риски. Даже после подсадки эмбрион может не прижиться. При этом среди нас уже растет множество детей, которые появились благодаря искусственному оплодотворению, и они совершенно ничем не отличаются от обычных малышей.
Что происходит с эволюцией
В глобальном плане человеческие гены могут со временем мутировать и видоизменяться. И онкологические заболевания — одна из самых ярких иллюстраций этого процесса. Теперь, когда продолжительность жизни выросла, увеличилась и вероятность появления опухолей. С другой стороны, прогресс тоже не стоит на месте: появляется все больше методов диагностики и лечения, которые помогают справляться с тяжелыми недугами.
Еще до недавнего времени выявление генетических заболеваний было непростой задачей. Однако методы секвенирования уже позволяют «читать» ДНК не по одной букве-нуклеотиду, а разбирать все буквы одновременно. Так можно выявлять и мутации, передающиеся по наследству и новые, от появления которых не застрахован никто. Конечно, некоторые окружающие факторы тоже могут влиять на то, как ведут себя наши гены. Это и экология, и пища, и привычки. Их изучением наука тоже занимается активно.
Куда движется генетика
Генетика становится всеобъемлющей: по одной капле крови теперь можно определить все, что веками записывалось в ДНК человека. Вместо сотрудников диагностикой занимаются математические алгоритмы. Вполне возможно, что через некоторое время генетическая экспертиза станет обычным делом и без нее не будет обходиться даже рядовой прием у врача-терапевта.
И наверняка будет создаваться все больше препаратов, основанных на принципах персонализированной медицины, которые подбираются в зависимости от особенностей метаболизма пациента и его мутаций. Что же касается детей на заказ, то наука должна помогать нам корректировать гены только в случаях тяжелых наследственных заболеваний, а не для того, чтобы выбирать пол ребенка и цвет его глаз или особенности поведения. В этом вопросе нужно позволить природе комбинировать наши гены для появления на свет совершенно неповторимого чудесного существа — человека.
Переписать код жизни: 12 важных вопросов о редактировании генома
Теперь у нас есть точный способ корректировать, заменять или даже удалять дефектные ДНК. Научный редактор The Guardian Ян Сэмпл объясняет научную сторону редактирования генома и риски, которые могут возникнуть в будущем.
Так что же такое редактирование генома?
Учёные сравнивают это с программами в компьютере, которые находят и заменяют ошибки в тексте. Только вместо исправления слов, редактор генома исправляет ДНК – биологический код, который является своеобразной «инструкцией» к живым организмам. С помощью редактирования генома исследователи могут деактивировать отдельные гены, корректировать вредоносные мутации и изменять активность специфичных генов у растений и животных – в том числе и у людей.
В чем смысл?
Энтузиазм вокруг темы редактирования генома объясняется возможностью лечить или предотвращать заболевания. Существуют тысячи генетических нарушений, которые передаются от поколения к поколению; многие из них – серьёзные и разрушительные. И они не редки: один ребёнок из двадцати пяти рождается с генетическим заболеванием. Среди самых распространённых – муковисцидоз (заболевание, которое характеризуется поражением желез внешней секреции – прим.), серповидноклеточная анемия (изменение строения белка гемоглобина, ведущее к тяжёлой форме анемии – прим.) и мышечная дистрофия.
Редактирование генома вселяет надежду на то, что эти болезни могут быть побеждены путём «переписывания» повреждённых генов в клетках пациента. Однако починка дефектных генов – это ещё не все возможности; уже есть опыт модифицирования иммунных клеток человека для борьбы с раком или для повышения их устойчивости к ВИЧ-инфекции. Также возможно исправление дефектных генов у человеческого эмбриона – таким образом можно предотвратить наследование серьёзных заболеваний. Но эта технология неоднозначна, так как генетические изменения могут распространиться на сперму или яйцеклетки пациента, то есть все внесённые генетические корректировки и любые побочные эффекты могут быть переданы следующим поколениям.
В каких ещё сферах применяется редактирование генома?
Некоторые отрасли медицины также воспользовались потенциалом новой технологии. Компании, работающие над производством антибиотиков нового поколения, разработали вирусы, которые сами по себе безопасны, но умеют находить и атаковать специфичные, вызывающие опасные инфекции штаммы бактерий. Также учёные используют редактор генома, чтобы обезопасить пересадку органов свиньи человеку. Помимо этого, редактирование генома повлияло на фундаментальные исследования, позволив учёным более точно понимать, как работают те или иные гены.
Так как это работает?
Есть множество способов редактировать гены, но настоящим прорывом в последние годы стал молекулярный инструмент Crispr-Cas9. Он использует особый участок бактериальной ДНК – CRISPR (буквально: короткие палиндромные повторы, регулярно расположенные группами) – чтобы найти специфическую область в генетическом коде организма, например, мутировавший ген. Эта область в дальнейшем отсекается с помощью фермента Cas9. В попытках восстановить повреждения клетка часто «отключает» этот ген. Этот способ очень полезен для работы с «вредоносными генами», но возможны и другие способы. Например, чтобы исправить дефектный ген, учёные могут разрезать мутировавшую ДНК и заменить здоровой цепочкой, которая доставляется вместе с молекулами Crispr-Cas9. Вместо Cas9 могут быть использованы другие ферменты, которые могут помочь редактировать ДНК более эффективно — например, Cpf1.
Напомните-ка, что такое гены?
Ген – это биологический шаблон, который организм использует для создания протеинов и ферментов, необходимых для построения и поддержания тканей и органов. Он представляет собой цепочку генетического кода, обозначаемого буквами G, C, T и A. У человека есть около 20 тысяч генов, сгруппированных в 23 пары хромосом, которые, в свою очередь, содержатся в ядре почти каждой клетки тела. Только около 1.5% нашего генетического кода, или генома, состоят из генов. Ещё 10% регулируют их, удостоверяясь, например, что гены включаются и выключаются в нужных клетках в нужное время. Остальная часть ДНК, судя по всему, бесполезна. «Бóльшая часть нашего генома не делает ничего, – говорит Джертон Лантер, генетик из Оксфордского Университета. – Это просто осколок эволюции».
Что за G, C, T и A?
Буквы генетического кода соответствуют молекулам гуанина (G), цитозина (С), тимина (Т) и аденина (А). В ДНК эти молекулы идут попарно: G и С, Т и А. Эти «основные пары» являются ступенями всем знакомой двойной спирали ДНК. Чтобы составить один ген, нужно много таких ступеней. Мутировавший ген, ответственный за муковисцидоз, содержит около 300.000 базовых пар, а за мышечную дистрофию – около 2,5 миллионов пар, это самый длинный ген в человеческом теле. Каждый из нас наследует от наших родителей около 60 новых мутаций, большинство – от отцов.
Но как добраться до нужных клеток?
Это весьма трудная задача. Большинство лекарств – это маленькие молекулы, которые могут путешествовать по телу с потоком крови, именно так они доставляются к органам и тканям. По сравнению с ними, молекулы, используемые в редакторе генома, огромны и доставить их к клеткам сложно. Но возможно. Один способ – добавить молекулы редактора генома в безвредные вирусы, которые инфицируют определённые типы клеток. Миллионы таких вирусов после этого вводятся в кровь или напрямую в поражённые ткани. Оказавшись в теле, вирусы вторгаются в необходимые клетки и высвобождают молекулы редактора генома, чтобы те делали свою работу. В 2017 году учёные из Техаса таким образом вылечили мышей от мышечной дистрофии Дюшена. Следующий шаг – клинические испытания на человеке.
Однако вирусы – не единственный способ доставить молекулы к клеткам. Исследователи использовали жировые наночастицы для переноса молекул Crispr-Cas9 к печени, а также короткие импульсы электричества, чтобы «открыть» поры эмбриона и через них ввести молекулы редактора генома.
Редактирование обязательно делать в самом организме?
Нет. Во время одного из самых первых испытаний редактора генома учёные забирали клетки из крови пациента, выполняли необходимые генетические корректировки и вводили исправленные клетки обратно. Такой метод выглядит многообещающим для лечения для людей, живущих с ВИЧ. Когда вирус попадает в организм, он инфицирует и убивает иммунные клетки. Но чтобы инфицировать иммунную клетку, ВИЧ сначала должен прицепиться к определённым белкам на её поверхности. Учёные выделили иммунные клетки из крови пациента и использовали редактор генома, чтобы вырезать ту ДНК, которая нужна клеткам для образования этих поверхностных белков. Без них ВИЧ не может получить доступ к клеткам.
Подобный способ может использоваться для борьбы с некоторыми типами рака: иммунные клетки выделяются из крови пациента и редактируются так, что они больше не могут синтезировать поверхностные белки, к которым цепляются раковые клетки. Отредактировав иммунные клетки и сделав из них «убийц рака», учёные размножают их и вводят обратно в организм пациента. Прелесть модифицирования клеток вне организма в том, что всё можно перепроверить до того, как вводить обратно, чтобы убедиться, что процесс редактирования проведён верно.
А что может пойти не так?
Современное редактирование генома довольно точное, но не идеальное. Процедура похожа на прицельную стрельбу – надо попасть по нужным клеткам, а по остальным – промахнуться. Даже если Crispr попадает куда нужно, изменения могут отличаться от клетки к клетке, например, в одной нужно исправить две копии мутировавшего гена, а в другой – только одну. Для некоторых генетических заболеваний это не столь важно, но становится проблемой, если заболевание возникает из-за единственного мутировавшего гена. Другая трудность возникает, когда изменения были произведены в неправильном участке генома. Таких «выстрелов не по мишени» может быть сотни, и они могут быть опасны, если разрушают здоровые гены или критически важные регуляторы ДНК.
Приведёт ли это всё к «редактированию» будущих детей?
Огромные усилия в медицине направлены на то, чтобы исправить дефектные гены у детей и взрослых. Но некоторые исследования показали, что есть возможность редактировать гены у эмбрионов. В 2017 году учёные, созванные Национальной Академией Наук и Национальной Академией Медицины США, сдержанно поддержали редактирование генома у человеческих эмбрионов для предотвращения самых серьёзных заболеваний, но только один такой опыт оказался безопасным.
Любые изменения на эмбриональной стадии повлияют на все клетки человека и будут переданы его детям, поэтому очень важно избегать вредоносных ошибок и побочных эффектов. Проектирование человеческих эмбрионов также поднимает вопрос непростой перспективы «дизайна» детей, когда эмбрионы редактируются больше по социальным, чем по медицинским причинам; например, чтобы сделать человека выше или умнее. Однако такие черты могут контролироваться тысячами генов, большинство из которых ещё неизвестны. Поэтому на данный момент перспектива редактирования генома будущего потомства весьма отдалённая.
Когда редактирование будет доступно простым пациентам?
Открытие клиникам доступа к редактированию генома – практически на финишной прямой. Около десятка испытаний Crispr-Cas9 запланированы или проводятся прямо сейчас. Большинство из них ведётся китайскими исследователями с целью борьбы с разными формами рака. Одно из первых исследований было запущено в 2016 году, когда учёные из провинции Сычуань вводили отредактированные иммунные клетки пациентам с поздней стадией рака лёгких. Большинство американских и европейских исследований ожидают своего начала в течение следующих нескольких лет.
Что дальше?
Базовое редактирование
Более мягкая форма редактирования генома – без разрезания ДНК на кусочки – использует химические реакции, чтобы изменить буквы генетического кода. Пока что это выглядит неплохо. В 2017 году исследователи в Китае использовали базовое редактирование для исправления мутаций, которые вызывают серьёзные нарушения кровеносной системы: как, например, гемолитическая анемия у человеческих эмбрионов.
Перемещение генов
Спроектированное перемещение генов может доставить определённые гены целым популяциям организмов. Например, таким образом можно сделать москитов бесплодными и сократить количество заболеваний, которые они распространяют. Но эта технология очень противоречива, так как может иметь широкомасштабные непреднамеренные экологические последствия.
Редактирование эпигенома
Иногда нет цели полностью удалить или заменить ген – необходимо просто ослабить или усилить его активность. Сейчас учёные работают над способностью Crispr выполнять такие задачи, предоставляя его молекулам больше возможностей, чем раньше.
Перевод: Кира Луппова.
Подписывайтесь на страницу СПИД.ЦЕНТРа в фейсбуке
А не замахнуться ли нам на. изменение генома?
А не замахнуться ли нам на. изменение генома?
Ученые научились редактировать молекулу ДНК в интересующем месте
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Человек стремится покорить природу, и ключ для этого — ДНК. Но чтобы подобраться к молекуле ДНК и повлиять на нее, необходимо использовать точнейшие молекулярные инструменты — белки или РНК. В этой статье рассказывается о новейшем инструменте для внесения мутаций в геном in vivo — сиквенс-cпецифичных нуклеазах.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
История изучения ДНК непроста, как и любое значительное исследование. Открыта она была еще в 1868 году Иоганном Фридрихом Мишером, который выделил некое вещество, содержащее азот и фосфор, из остатков клеток в гное [1]. После того, как Мишер обнаружил, что оно обладает кислотными свойствами, вещество назвали нуклеиновой кислотой. Однако долгое время функция ДНК была неясной: ее считали всего лишь способом запасания фосфора в организме. Данная теория считалась правильной почти до середины XX века; в качестве косвенного доказательства ученые ссылались на однообразное, по их мнению, строение молекулы ДНК (состоящей исключительно из четырех различных видов нуклеотидов: дезоксиаденозина — А, дезоксигуанозина — G, дезокситимидина — Т, дезоксицитидина — С).
Функцию ДНК, естественно, открыли раньше, чем ее вторичную структуру, которая оставалась неизвестной вплоть до 1953 года. Соответственно, из-за этого не могли установить, как проходят такие процессы как передача наследственной информации, как белки распознают определенные последовательности в ДНК и т.п.
В 1949–1951 годах Эрвин Чаргафф сформулировал свои знаменитые правила, которые говорят о строгом соотношении количества азотистых оснований внутри каждой молекулы ДНК [4] (в частности, что количество аденина равняется количеству тимина, а количество цитозина — количеству гуанина); затем Морисом Уилкинсом и Розалиндой Франклин были получены рентгеноструктурные данные, несущие структурную информацию о ДНК. На основании этих двух фактов Френсис Крик и Джеймс Уотсон предложили структуру двойной спирали ДНК [5], которая была доказана позднее в опытах Мэтью Мезельсона и Франклина Сталя [6].
Как только была открыта вторичная структура ДНК, стало легче предсказывать, а затем доказывать экспериментами механизмы различных процессов, происходящих с ДНК. Репликация (удвоение молекулы ДНК), транскрипция (перенос генетической информации с ДНК на РНК), различная регуляция экспрессии генов стали главными проблемами, интересующими молекулярных биологов.
Очевидно, что для осуществления этих процессов необходимы определенные белки, которые, в свою очередь, взаимодействуют как друг с другом, так и с ДНК. И если некоторые стадии протекают неспецифично (например, у эукариот репликация ДНК может начаться во множестве участков ДНК [7]), то, например, регуляция экспрессии генов происходит с помощью взаимодействия белков с довольно консервативными, т.е. строгими последовательностями ДНК.
Эндонуклеазы рестрикции: «Режем ДНК в нужном вам месте!»
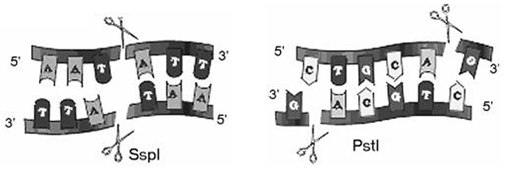
Одними из первых открытых белков, специфически связывающих ДНК, являются эндонуклеазы рестрикции. Это ферменты, которые разрезают ДНК по специфическим нуклеотидным последовательностям, называемым сайтами рестрикции (рис. 1) [8].
Рисунок 1. Рестрикция с образованием а) «тупых» концов; б) «липких» концов
Сам термин «рестрикция» появился благодаря исследованиям фага λ и феномена контролируемой рестрикции и модификации бактериальных вирусов клетками-хозяевами. Этот процесс был впервые обнаружен в результате работ Сальвадора Лурии [9] и Джузеппе Бертани [10] в 1950-х годах. Ученые обнаружили, что если фаг λ хорошо растет в одном штамме Escherichia coli, то в другом штамме его рост падает на несколько порядков, т.е. клетка-хозяин может снижать его биологическую активность. Оказалось, что запрет роста — «рестрикция» — вызывается ферментативным расщеплением ДНК фага. Соответственно, и фермент, отвечающий за этот процесс, назвали ферментом рестрикции.
Сами ферменты были обнаружены в лабораториях Вернера Арбера и Мэттью Мезельсона [11]; причем эндонуклеазы, которые исследовались в их работах, принадлежали, как определили позже, к I классу эндонуклеаз рестрикции. Они разрезают ДНК в случайном месте снаружи от места распознавания, причем как минимум на расстоянии 1000 нуклеотидов.
В 1970-х годах Гамильтон Смит, Томас Келли и Кент Велкокс выделили и охарактеризовали первую эндонуклеазу рестрикции II класса. Этот тип ферментов рестрикции более удобен для лабораторного использования, поскольку расщепляет ДНК внутри своего сайта распознавания, который, как правило, представляет собой палиндром из 4–8 нуклеотидов. Кроме того, эндонуклеазы этого класса не нуждаются в энергетической молекуле АТФ для активности, — только в ионах магния в качестве кофактора.
В 1990-х и ранних 2000-х годах были открыты другие представители данного семейства, которые не соответствовали всем критериям этого класса ферментов [12]. На данный момент уже открыты эндонуклеазы типов IIB, IIE, IIF, IIG, IIM, IIS, IIT. Возможно, в будущем этот список еще значительно расширится.
Существует также III класс эндонуклеаз рестрикции. Они были также открыты как компоненты прокариотической защитной системы против чужеродной ДНК. Эндонуклеазы III типа распознают две отдельных последовательности ДНК длиной 5–6 нуклеотидов и разрезают её примерно через 20–30 пар после сайта распознавания. Для их работы необходимы молекулы АТФ.
Эндонуклеазы рестрикции используют для обработки ДНК в различных лабораторных экспериментах. Обычно их применяют для вставки генов в процессах генного клонирования и экспериментах по исследованию белков.
Кроме того, эндонуклеазы могут быть использованы для выявления различий в аллелях гена [13]. Это возможно только в случае, если мутация произойдет в сайте узнавания, содержащемся внутри аллеля. Таким образом, отпадает нужда в дорогостоящем секвенировании гена; в частности, до изобретения секвенирования обработка эндонуклеазами рестрикции использовалась для картирования геномов.
Одно из новейших применений нуклеаз — внесение с помощью них различных изменений в геном клетки, таких как мутации уже имеющихся генов, вставка новых генов или вырезание исходных. Это очень перспективное направление генной инженерии с широчайшими возможностями практического применения! О нем будет рассказано в следующем разделе.
Эндонуклеазы — это эффекторы, т.е. белки действия. Если они окажутся у цели, то точно ее разрежут. Но природные белки распознают лишь небольшое число последовательностей ДНК, что накладывает огромные ограничения на использование этого уникального инструмента. Ах, если бы можно было доставить эндонуклеазу к любой желаемой последовательности ДНК.
Революция в области ДНК-связывающих белков: «Доставим ваш белок по любому адресу ДНК, используя TAL-эффекторы или CRISPR/Cas9-систему»
Одной из наиболее заманчивых идей для ученых является возможность напрямую точечно влиять на работу клетки. Для этого необходимо прицельно воздействовать на ДНК именно в области интересующего гена. Воздействие может быть разного характера: включение/выключение гена, внесение мутации и др. Для этого потребовалось уметь синтезировать белки, узнающие конкретную последовательность ДНК («следопыты»), к которым можно было бы пришить белки «действия».
Недавно открытые белки TAL-эффекторы и система Cas9 произвели настоящую революцию в нацеливании различных эффекторов на специфическую последовательность ДНК!
TAL-эффекторы: «Используем паразитов во благо»
TAL-эффекторы (Transcription Activator Like Effectors) — белки, синтезируемые многочисленным видами бактерий рода Xanthomonas — паразитами растений. Они были открыты в 2009 году практически одновременно несколькими группами ученых. TAL-эффекторы активируют считывание нужных паразитам генов в растениях-хозяевах (крайне специфично связываясь с хозяйской ДНК), что облегчает бактериальную колонизацию этого растения и выживание бактерий внутри него [14].
TAL-эффектор можно мысленно поделить на три части (рис. 2); наибольший интерес представляет средняя, крайне консервативная центральная область белка, состоящая из повторяющихся блоков размером 34 аминокислоты. В 2009 же году была показана простая и однозначная связь между повторами и узнаваемыми нуклеотидами. Блоки отличаются друг от друга лишь аминокислотами № 12 и № 13, которые и определяют вид нуклеотида, распознаваемый данным мономером. На каждый из четырех нуклеотидов ДНК приходится определенное сочетание этих аминокислот TAL-эффектора [15]; т.е. можно представить себе этот белок как паровозик, состоящий из одинаковых вагонов, центральное окошко которых покрашено в один из четырех цветов.
Рисунок 2. Строение TAL-эффектора на примере avrBs3
Простота «TALE-кода» открывает многочисленные возможности для биологического применения этих белков. Недавние исследования показали, что можно специально подобрать «вагоны» для искусственного «паровозика» и синтезировать ранее не существовавшие в природе белки для узнавания конкретных последовательностей ДНК в различных типах клеток — как растений, так и млекопитающих. Многие группы ученых уже используют искусственные TAL-эффекторы, узнающие новые последовательности ДНК, например, в томатах, Arabidopsis thaliana [16] и клетках человека [17].
Синтезированные TAL-эффекторы также сшивают с каталитическим доменом нуклеазы (см. раздел «Эндонуклеазы рестрикции») для создания TAL-эффекторных нуклеаз. Эти нуклеазы могут быть полезны для генной инженерии и генной терапии [18].
TAL-нуклеазы используют для создания двуцепочечных разрывов в строго определенном месте ДНК. Известно, что нарушенные таким образом гены клетка может чинить двумя путями: либо просто соединением концов (что может привести к случайным мутациям), либо заново синтезируя поврежденную цепь по комплементарной ей цепи ДНК (т.н. гомологичная рекомбинация).
Во втором случае вырезается значительный по длине участок ДНК, а вместо него по комплементарной (на краях разрыва) матрице синтезируется вставка, закрывающая брешь [19]. Если в клетку поместить ДНК специально мутированного гена, то он будет использован в качестве донорной матрицы, и в геном встроится желаемая мутация. Можно таким методом даже вырезать отдельные гены — или вставлять новые! Таким образом, благодаря разработанной технике сборки ДНК-узнающих повторов, TAL-эффекторы в составе гибридных белков предоставляют возможность направить желаемый эффектор к любой специфической последовательности ДНК — и добиться самых разных воздействий на ДНК: от регуляции транскрипции до внесений мутаций.
CRISPR/Cas9 система: «Неожиданное альтернативное применение защитного комплекса бактерий»
В нашем организме, после того, как мы переболели какой-то болезнью, остаются клетки памяти иммунной системы, которые при повторном попадании в организм вредителей активизируются и помогают ускоренно справиться с ними.
Бактерии справляются со своими патогенами с помощью аналогичной «системы памяти»: CRISPR/Cas-системы обеспечивают иммунитет бактерий и архей против вирусов и плазмид. Этот защитный комплекс состоит из:
Этот комплекс был открыт в 2012 году при совместной работе ученых из США, Швейцарии, Австрии и Швеции [20], [21].
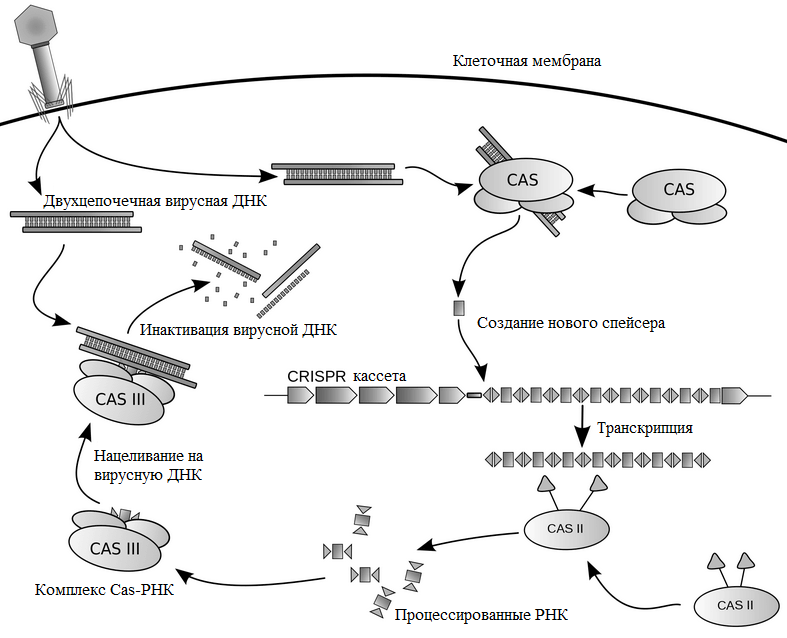
Иммунитет, обусловленный CRISPR/Cas, возникает за три стадии (рис. 3). В первой фазе бактерии или археи, у которых в геноме есть «блокнотик для записи» — CRISPR-кассета, — отвечают на появление вируса включением в конец кассеты коротких фрагментов чужеродной ДНК. На следующей стадии происходит транскрипция — считывание этой свежевключенной последовательности (образование описанных выше двух РНК) и обработка их нуклеазами. Теперь эти РНК могут специфично связаться с вирусной ДНК, и это взаимодействие через цепь событий приводит к ее расщеплению и «смерти» вредителя.
Рисунок 3. Схема работы комплекса Cas—РНК и CRISPR-кассеты
Грубо говоря, ситуация напоминает сказку про репку: первая РНК связывается с «репкой» — чужеродной ДНК — и «зовёт» вторую, вторая — специальный белок Cas9, который уже осуществляет двухцепочечный разрыв цепи чужой ДНК [22].
Несмотря на то, что в природе две РНК системы Cas9 разделены, учёные показали, что химерная РНК, представляющая собой сшитые в одну цепь вышеуказанные РНК, так же способна направлять Cas9 к ДНК-мишени. Более того, при соблюдении ряда условий можно менять последовательность первой внутри химерной РНК так, чтобы нацеливать Cas9 на желаемые гены.
Эта система даже проще TAL-эффекторов, поскольку для распознавания одного дезоксирибонуклеотида ДНК не нужен громоздкий «вагон» белка: один рибонуклеотид РНК легко и точно узнаёт комплементарный ему дезоксирибонуклеотид ДНК мишени! Экономия как в размере инструмента, так и в легкости его синтеза.
К настоящему времени показано, что эта система работает не только в археях и бактериях, но и в организмах рыб (Danio rerio), а также в клетках млекопитающих [23]. Уже установлено, что, как и в случае TAL-эффекторных нуклеаз, обработка ДНК Cas9-системой приводит к эффективному (10–30% случаев) возникновению мутаций.
Человек стремится покорить природу, и ключ для этого — ДНК. Но чтобы подобраться к ДНК и повлиять на нее, необходимо спуститься на молекулярный уровень и использовать белки или РНК. Сейчас развитие данных направлений идет стремительно, каждый месяц случаются значительные прорывы в этой области. Кто знает, какие чудеса ожидают нас через год? Возможно, будет найдена новая система, максимально упрощающая исходно сложный и кропотливый процесс вмешательства человека в работу природы.