Что мы знаем о вирусах и методах защиты от них?
Что такое вирус?
Как устроен вирус?
В центре агента находится генетический материал РНК или ДНК, вокруг которого располагается белковая структура — капсид.
Капсид служит для защиты вируса и помогает при захвате клетки. Некоторые вирусы дополнительно покрыты липидной оболочкой, т.е. жировой структурой, которая защищает их от изменений окружающей среды.
Вирусолог Дэвид Балтимор объединил все вирусы в 8 групп, из которых некоторые группы вирусов содержат 1-2 цепочки ДНК. Другие же содержат 1 цепочку РНК, которая может удваиваться или достраивать на своей матрице ДНК. При этом каждая группа вирусов производит себя в различных органеллах зараженной клетки.
Вирусы имеют определенный диапазон хозяев, т.е. он может быть опасен для одних видов и абсолютно безвреден для других. Например, оспой болеет только человек, а чумкой только некоторые виды плотоядных. Вирус не способен выжить сам по себе, поэтому активируется только в хозяйской клетке, используя ее ресурсы и питательные вещества. Цель вируса — создание множества копий себя, чтобы инфицировать другие клетки!
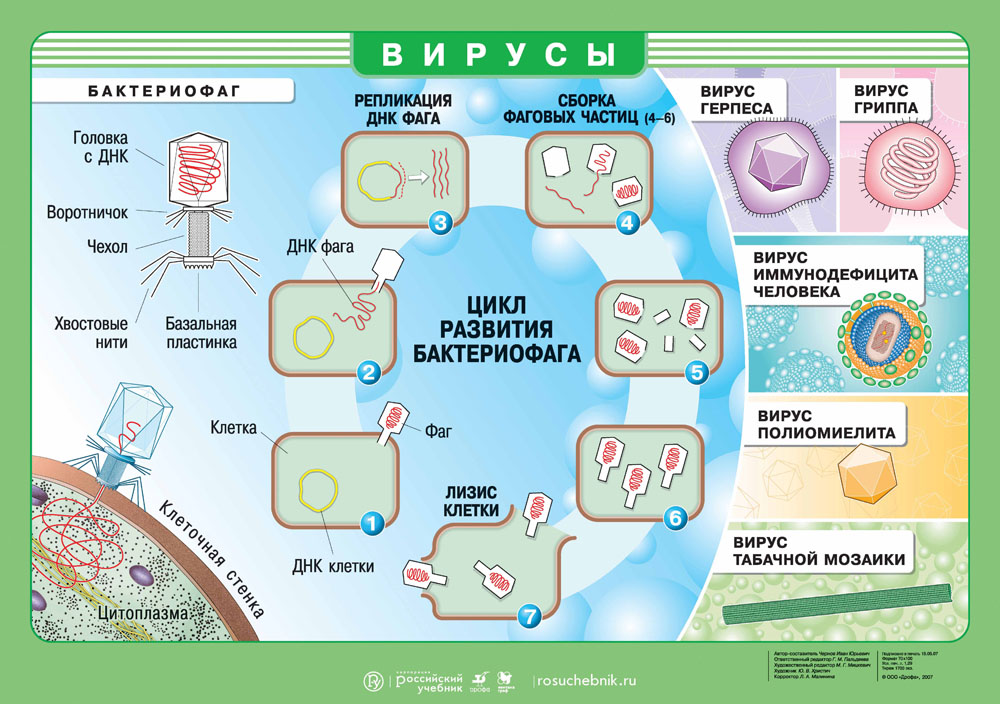
Вирусы. Цикл развития бактериофага. Скачать наглядное пособие в большом разрешении можно здесь.
Как вирус попадает в организм?
Геном вируса встраивается в одну из органелл или цитоплазму и превращает клетку в настоящий вирусный завод. Естественные процессы в клетке нарушаются, и она начинает заниматься производством и сбором белка вируса. Этот процесс называется репликацией. И его основная цель — это захват территории. Во время репликации генетический материал вируса смешивается с генами клетки хозяина — это приводит к активной мутации самого вируса, а также повышает его выживаемость. Когда процесс репликации налажен, вирусная частица отпочковывается и заражает уже новые клетки, в то время как инфицированная ранее клетка продолжает производство.
«Для проникновения в клетку белки поверхности вируса связываются со специфическими поверхностными белками клетки. Прикрепление, или адсорбция, происходит между вирусной частицей и клеточной мембраной. В мембране образуется дырка, и вирусная частица или только генетический материал попадают внутрь клетки, где будет происходить размножение вируса. Сегодня ученые всего мира сделали важное открытие о том, что заражение коронавирусом людей преклонного возраста объясняется тем, что у пожилых людей накапливается специфический белок, который помогает COVID-19 проникать внутрь клетки эпителия».
Выход вируса
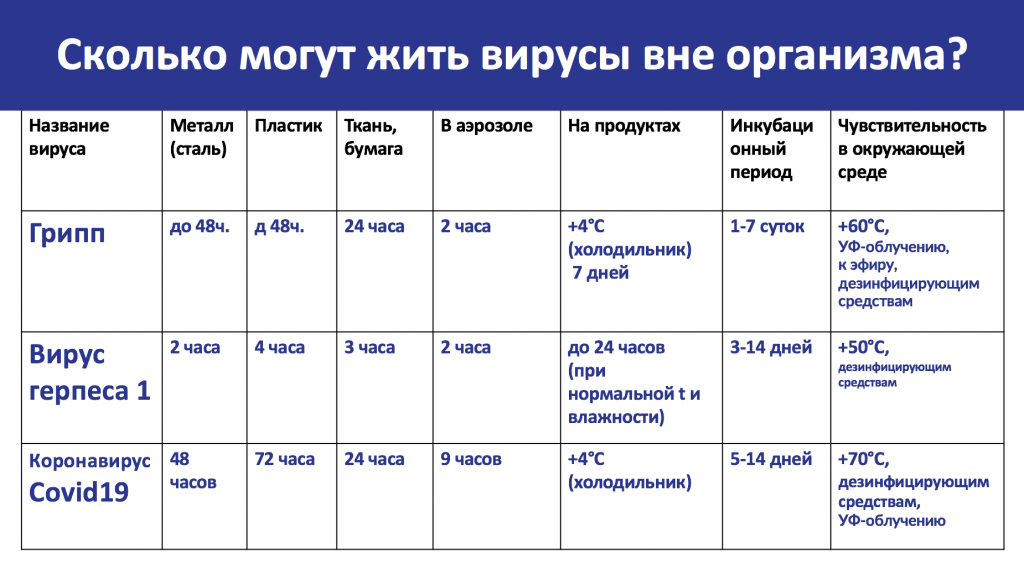
Скорость распространения вирусной инфекции
Вирусная латентность
Как вирус распространяется?
Почему с вирусами так тяжело бороться?
Сегодня людям уже удалось победить некоторые вирусы, а некоторые взять под жесткий контроль. Например, Оспа (она же черная оспа). Болезнь вызывается вирусом натуральной оспы, передается от человека к человеку воздушно-капельным путем. Больные покрываются сыпью, переходящей в язвы, как на коже, так и на слизистых внутренних органов. Смертность, в зависимости от штамма вируса, составляет от 10 до 40 (иногда даже 70%), На сегодняшний день вирус полностью истреблен человечеством.
Кроме того, взяты под контроль такие заболевания, как бешенство, корь и полиомиелит. Но помимо этих вирусов существует масса других, которые требуют разработок или открытия новых вакцин.
Коронавирус
К наиболее распространенным симптомам COVID-19 относятся повышение температуры тела, сухой кашель и утомляемость. К более редким симптомам относятся боли в суставах и мышцах, заложенность носа, головная боль, конъюнктивит, боль в горле, диарея, потеря вкусовых ощущений или обоняния, сыпь и изменение цвета кожи на пальцах рук и ног. Как правило, эти симптомы развиваются постепенно и носят слабо выраженный характер. У некоторых инфицированных лиц болезнь сопровождается очень легкими симптомами.
Поскольку пока не изобретено вакцины от COVID-19, в целях защиты от инфекции самым важным для нас является соблюдение гигиены.
Гигиена — раздел медицины, изучающий влияние жизни и труда на здоровье человека и разрабатывающая меры (санитарные нормы и правила), направленные на предупреждение заболеваний, обеспечение оптимальных условий существования, укрепление здоровья и продление жизни.
Сегодня следует соблюдать определенные правила гигиены:
«Мы пытались рассказать Вам не только о существующих научных фактах о вирусах, но и показать, что определенные знания помогают нам в нынешней практической ситуации сохранить свое здоровье и здоровье своих близких. Мы понимаем, что сегодня коронавирус может находиться практически везде: на поверхностях любых предметов, в окружающей среде и т.д. Поэтому самоизоляция – это один из важнейших способов защиты от инфекции. Находясь дома, вы защищаете не только свое здоровье, но и помогаете медикам и ученым, которые сражаются с этим вирусов и день и ночь. Ведь, чем меньше шансов у нас с вами заболеть, тем больше шансов появляется у них, чтобы победить коронавирус. Пожалуйста, оставайтесь дома и соблюдайте режим самоизоляции и нормы гигиены».
Природа — неисчерпаемый резервуар инфекций
Р оссийская академия наук провела в онлайн-режиме собрание Научного совета РАН «Науки о жизни» на тему «Коронавирус — глобальный вызов науке», на котором выступили ведущие российские ученые-вирусологи, эпидемиологи, биологи с докладами о причинах коронавирусной эпидемии, ее происхождении и о методах борьбы с ней и с возможными новыми эпидемиями.
«Стимул» публикует краткое изложение некоторых из этих докладов.
Мы мало знаем об инфекциях
Академик РАН Виктор Малеев:
— Не могу не отметить, что в медицине последние десятилетия существовала недооценка потенциала инфекционных болезней, инфекционного фактора. Много лет объявляется, что мы их фактически победили. Всемирная организация здравоохранения уже много лет реализует программу ликвидации ряда инфекций — туберкулез, гепатиты, ВИЧ-инфекция, малярия. Считается, что к 2030 году все это будет уже ликвидировано. Мне кажется, что это нереально и научно не обосновано, хотя на эти программы тратятся значительные финансовые средства. Всем известно, что к настоящему времени нам удалось ликвидировать только натуральную оспу. Но одновременно активизировались ортопоксвирусные инфекции другой этиологии, например оспа обезьян. На протяжении уже тридцати лет мы пытаемся безуспешно ликвидировать полиомиелит, корь в отдельных регионах. Корь уже где-то была ликвидирована, но на американском континенте возникла вновь.
Эпидемии продолжаются. Это неудивительно, потому что инфекции, по сути, представляют собой природную сущность. И несмотря на научный прогресс последнего времени, нам лишь в малой степени удалось получить полноценные знания о биологическом и генетическом разнообразии на Земле, а ведь на 90 процентов они обусловлены микроорганизмами, которые оказывают существенное влияние на эволюцию биосферы, в том числе на человеческую популяцию.
Мы до сих пор не знаем всего спектра инфекционных заболеваний. Каждый год появляются новые инфекции, только за последний год около тридцати. ВИЧ-инфекция, которая только в 1980 году появилась, уже не считается новой. Многие инфекции возвращаются через значительный промежуток времени. Пример — лихорадка Зика, которая вернулась вновь через шестьдесят лет абсолютного молчания. Нельзя исключить, что и оспа через какое-то времени вернется.

За последние десятилетия сложилось представление, что инфекционные болезни больше распространены в отсталых странах, а вот неинфекционные — это «преимущество» развитых стран. На мой взгляд, это совершенно не так. Инфекционный фактор является триггером при различных патологических состояниях. Пример — язвенная болезнь желудка и двенадцатиперстной кишки, ведь только выявление ее инфекционной этиологии позволило повысить эффективность, поменять стратегию и тактику лечения. Многие хронические инфекции становятся предтечей онкологии. Сейчас признано, что в патологии сердечно-сосудистой системы ведущую роль играют системные воспаления, которые, по сути, тоже являются хроническим инфекционным заболеванием. Огромное количество инфекций, передающихся половым путем.
Кроме того, если соматические заболевания имеют локальное значение, то инфекции обладают эпидемическим потенциалом и способны к глобальному распространению. И для них характерна непредсказуемость. Эффективный контроль над ними возможен лишь в планетарном масштабе. А пока чаще всего мы не умеем их прогнозировать.
Мне кажется, многие проблемы эпидемиологии, можно было эффективно решить с помощью искусственного интеллекта, который, например, определил бы рациональные подходы к тому, кого куда направлять. Нужна робототехника. У нас происходит заражение медперсонала. Может быть, надо применять чаще элементы робототехники, чтобы у медработников не было прямого контакта с больными.
Меня удивляет, что до сих пор применяются защитные костюмы, которые применялись еще в 1300 году, когда была чума. Наверное, надо подумать над использованием новых материалов, новых методов дезинфекции.
И конечно, я переживаю, что производство вакцины может начаться тогда, когда все уже закончится. У нас очень долгие процедуры их согласования. Может быть, тут нужно применять прогнозное моделирование, чтобы какие-то этапы с помощью компьютеров быстрее преодолеть.
Наконец, меня удивляет, что у нас последние годы в патофизиологи, патологоанатомы практически не занимаются инфекционными болезнями. А ведь такие известные российские ученые, как Давыдовский, Абрикосов и другие, были впереди планеты всей в исследованиях патогенеза инфекционных болезней. А для нас очень важно знать, как и куда коронавирус проникает, что он там делает конкретно, почему так внезапно все происходит. И поэтому нужны серьезные патофизиологические генетические исследования при инфекциях. А они сейчас вообще не проводятся: эту инфекцию пройдем и ожидаем другие.
Источник коронавируса все же летучие мыши
Доктор биологических наук, заведующий лабораторией биотехнологии Института вирусологии имени Д. И. Ивановского Национального исследовательского центра эпидемиологии и микробиологии Сергей Альховский:
— С начала 2000-х годов мы уже три раза столкнулись с появлением новых зооантропоморфных коронавирусов, патогенных для человека, которые обладают эпидемическим и даже пандемическим потенциалом.
Коронавирусы представляют собой очень обширное семейство зоонозных РНК-содержащих вирусов, которые повсеместно распространены и инфицируют очень широкий круг позвоночных хозяев, включая различные виды млекопитающих, птиц и даже земноводных. До 2000-х годов мы рассматривали коронавирусы исключительно как возбудители ОРВИ, которые участвуют в сезонном подъеме заболеваемости и не вызывают серьезных осложнений.
Первой такой инфекцией пандемического рода был тяжелый острый респираторный синдром — ТОРС, или SARS, который возник в 2002 году в Китае. Далее с 2012 года мы начали регистрировать новую коронавирусную инфекцию — ближневосточный респираторный синдром, MERS, в Саудовской Аравии и других странах. И наконец, сейчас мы переживаем уже третью эпидемию, пандемию COVID-19, вызванную новым коронавирусом, который получил название SARS-CoV-2 или SARS-2. Все эти инфекции характеризуются тем, что первичным источником инфицирования людей являются животные. Это или сельскохозяйственные животные, как в случае с MERS, где в этой роли выступали верблюды, или же различные дикие или экзотические животные, которые выращиваются на фермах и продаются в живом виде на рынках. Но масштабные исследования, которые начали проводить с 2000-х годов, показали, что истинным и природным резервуаром этих вирусов являются летучие мыши, от которых впоследствии получено очень много штаммов коронавирусов.
И сегодня мы знаем, что рукокрылые — основной природный резервуар как коронавирусов, так и многих других зоонозных вирусов. В циркуляцию альфа-коронавирусов и бета-коронавирусов вовлечены не менее 30 видов из 11 различных семейств этого отряда, причем выявляются они практически во всех географических регионах мира.
По современной классификации вирусы SARS и SARS-CoV-2 относятся к подроду Sarbecovirus, тогда как вирусы MERS и родственные вирусы относятся к подроду Merbecovirus в составе рода Beta-coronavirus. Это, в принципе, две очень близкие группы вирусов, но между ними существует и ряд отличий, прежде всего связанных с использованием разного типа рецепторов, и ряд экологических особенностей, связанных с тем, что их резервуаром являются разные виды летучих мышей.
Резервуаром SARS-подобных коронавирусов являются подковоносые. Множество штаммов изолированы и в Китае, и в европейских популяциях этих летучих мышей. Общую зараженность подковоносов оценивают в 10 процентов. Но в некоторых колониях, популяциях зараженность этих мышей SARS-подобными вирусами может составлять и 30, и 40, и даже 60 процентов, причем вирус у них выделяется в очень больших количествах с фекалиями.

С MERS-подобными вирусами ситуация тоже схожая: их резервуар — это гладконосые летучие мыши. Эти вирусы выделялись практически во всех регионах внутри их ареала. И здесь надо отметить, что эти ареалы двух резервуаров во многом перекрываются и охватывают территорию России. То есть нет никаких сомнений, что и в наших российских популяциях летучих мышей точно так же циркулируют вирусы, сходные с MERS и SARS.
Тропизм коронавирусов определяется белком S. Это тот белок, который формирует характерные выросты на поверхности вириона. Этот белок несет на себе так называемый рецептор-связывающий домен, который непосредственно взаимодействует с клеточным рецептором. Основные отличия вирусов летучих мышей от вирусов человека связаны непосредственно со структурой данного домена. То есть вирусы летучих мышей в большинстве своем не могут связывать человеческий ACE2-рецептор и не могут инфицировать человека напрямую, им для этого необходимо изменить свою рецепторную специфичность.
А рецепторная специфичность связана с очень высокой гетерогенностью рецептор-связывающего региона. В этом рецепторе выявлено уже несколько ключевых для связывания аминокислот, и по сути своей мутаций в этих ключевых позициях достаточно для того, чтобы вирус прошел адаптацию к человеку.
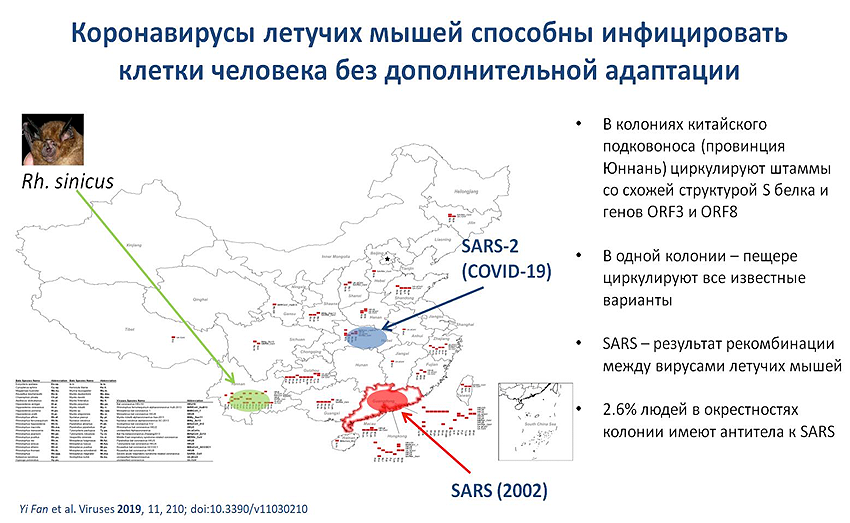
Мы долгое время считали, что, поскольку вирусы летучих мышей не способны напрямую инфицировать человека, они должны пройти адаптацию в некоем промежуточном хозяине. И в качестве промежуточного хозяина рассматривались верблюды или какие-то другие экзотические животные. Однако последние исследования показывают, что в популяциях летучих мышей циркулирует огромное количество вариантов SARS-подобных вирусов, среди которых встречаются вирусы, которые уже способны связывать человеческий рецептор и инфицировать человеческие клетки. То есть те варианты вируса, которые уже циркулируют среди летучих мышей, не требуют никакой дополнительной адаптации в промежуточном хозяине, и наиболее вероятным сценарием появления этих вирусов сейчас рассматриваются непосредственно колонии, в частности, китайских подковоносов, где эти вирусы возникают в результате серии рекомбинаций.
Это в полной мере соответствует и новому вирусу SARS-2, где ближайший к нему вирус был еще в 2013 году получен от летучих мышей, — это вирус RaTG13, и у него некоторые белки имеют стопроцентную схожесть с SARS-2. И появление этого вируса, вероятнее всего, также связано с серией рекомбинаций, а его предшественники или отдельные куски генома циркулировали в популяциях летучих мышей еще в 2013 году.
Суммируя все сказанное, нужно сказать, что пандемические коронавирусы являются типичным представителем новых и вновь возвращающихся инфекций. В природе существует огромный резервуар зоонозных вирусов, в котором постоянно формируются новые и новые варианты, и эти варианты периодически выплескиваются в человеческую популяцию. И этот процесс продолжается и в наше время. Главная проблема в том, что мы не можем прогнозировать эти события. И начинаем действовать только тогда, когда вирус выплеснулся из резервуара в человеческую популяцию, и мы абсолютно не застрахованы от появления новых и новых вариантов этих вирусов. Мы сейчас боремся с эпидемией COVID, и мы ее победим. Но эти природные резервуары и эти зоонозные вирусы никуда не денутся, и такие события будут продолжаться и дальше. А какие типы вирусов будут выплескиваться, мы сейчас не знаем, будут ли это коронавирусы, или, может быть, буньявирусы, или флавивирусы — это покажет время. Но чтобы быть готовым к таким ситуациям, нам необходимо действовать на упреждение. И прежде всего необходимо глубокое изучение природных резервуаров и процессов, которые в них происходят.
Одним из первых шагов в этом направлении должна стать задача выявить все зоонозные вирусы, которые обладают патогенным потенциалом в природных резервуарах. У нас с 1970-х годов развивалось направление, посвященное экологии вирусов, которое именно и было направлено на изучение природных резервуаров и зоонозных вирусов, которые в них циркулируют. Сегодняшние события показывают, что нам необходимо возобновить эти исследования уже с использованием новых технологий. И в этом случае к следующим таким ситуациям мы будем подготовлены намного лучше.
Убить невидимого убийцу. Все о вирусах и методах борьбы с ними
Алевтина Боголюбова-Кузнецова СПИД.ЦЕНТР
Вирусы у всех на слуху. С одними мы неизбежно сталкиваемся лично, например, с вирусами гриппа или теми, что вызывают простуду. Другие будоражат медицинское сообщество, наводняют новости и становятся зловещими прообразами для популярной литературы и кино.
И это неудивительно хотя бы потому, что вирусы — штука довольно непонятная. Неясно даже, считать их живыми или нет. С одной стороны, это просто хрупкий набор молекул, который не может существовать автономно, без живой клетки. Он не производит и не накапливает энергии, а также не поддерживает постоянства внутренней среды — ее попросту нет. Но когда вирус попадает в клетку, он проходит жизненный цикл, копирует себя и эволюционирует. Невидимое глазу нечто существует в огромном количестве, постоянно меняется, переходит от одних хозяев к другим и причиняет страдания разной степени тяжести всему человечеству.
Как устроены вирусы?
Вирусная частица, или вирион, — это нуклеиновая кислота (ДНК или РНК) в обертке из белков. В некоторых случаях она покрыта дополнительным слоем липидов, «украденных» у клетки-хозяина. У вирусов есть своя классификация: царства, семейства и прочие таксоны (группы), за списком которых следит Международный комитет по таксономии вирусов. Самый большой таксон — реалм. Сейчас ученые выделяют четыре реалма, из которых три — ДНК-содержащие вирусы. К ним относятся, например, вирусы оспы, герпеса и папилломавирусы.
РНК-содержащие вирусы можно разделить на собственно РНК-вирусы и ретровирусы. Первые — это вирусы гриппа, бешенства, гепатита С, а также коронавирусы и вирус Эбола. Они содержат РНК и используют для размножения РНК-зависимую РНК-полимеразу, с ее помощью на исходной молекуле РНК сразу синтезируется новая. А к ретровирусам относится, например, ВИЧ. Он содержит РНК, но в ходе жизненного цикла она превращается в ДНК и встраивается в геном клетки-хозяина. После чего новая РНК синтезируется уже на основе молекулы ДНК — то есть так же, как у нас.
Как с ними бороться?
Можно выделить три стратегии борьбы с вирусами. Первая — «пожар проще предотвратить, чем потушить». Защититься от заражения можно по-разному, например, избегать незащищенного секса или контакта с зараженной кровью. Более изощренный способ — контроль природных резервуаров вируса: осушение болот (чтобы предотвратить вспышки желтой лихорадки), карантин, вакцинация или отстрел животных.
Еще одна стратегия — активная и пассивная иммунопрофилактика. Активная — это простая и всем знакомая вакцинация. Человеку вводят неактивную форму вируса или его кусочек, в организме срабатывает иммунный ответ и синтезируются антитела, которые защитят человека в будущем, если он когда-нибудь встретится с настоящим живым вирусом. Но вакцину не всегда можно создать, да и уже существующие порой не работают на все сто. Так, вакцина от гриппа защищает только от нескольких — самых распространенных в текущем сезоне — штаммов (видов) вируса. Пассивная иммунопрофилактика — это введение готовых антител тем, кто уже встретился с вирусом или с большой вероятностью сделает это. Такие лекарства существуют для респираторно-синцитиального вируса (рекомендованы недоношенным младенцам) и ветряной оспы (для людей с подавленным иммунитетом).
И, наконец, последняя стратегия на случай, если ничто не помогло и человек заболел, — антивирусные препараты. Их развитие подстегивали научный прогресс и насущные проблемы. Чтобы придумать противовирусный препарат, нужно сначала изучить вирус и его жизненный цикл и выбрать возможные мишени для атаки. Причем такие, чтобы они как можно сильнее отличались от человеческих аналогов. Иначе лекарство будет бороться и с вирусами, и с невинными человеческими клетками, вызывая сильные побочные эффекты.
Первые клеточные культуры, в которых можно было имитировать взаимодействие вируса с хозяином, появились в 1950-х годах. До этого удобных моделей in vitro (в пробирке) не существовало, и изучение вирусов было затруднено. Уже в 1963 году появился первый антивирусный препарат — идоксуридин. Это был нуклеозидный аналог дезоксиуридина — одного из четырех «кирпичиков» молекулы ДНК. Препарат до сих пор используется при лечении герпеса.
В 80-е произошло другое громкое открытие — вирус иммунодефицита человека. Это породило шквал научных работ, посвященных разработке новых противовирусных лекарств. К тому времени связанный с ним СПИД уже распространился по миру, а в США началась эпидемия.
Какие бывают антивирусные препараты?
Их можно разделить на 13 групп, причем к шести относятся различные лекарства против ВИЧ. Это ингибиторы входа вируса в клетку, вирусных ферментов интегразы и протеазы, а также три вида ингибиторов вирусного фермента обратной транскриптазы, или ревертазы. Все они действуют на разные этапы жизненного цикла вируса:
1. Проникновение в клетку
Это первое, что должен сделать вирус, попав в организм. То, какую клетку он поразит, определяется рецептором на ее поверхности. У ВИЧ это рецептор CD4, который есть у Т-хелперов, макрофагов, а также некоторых других видов клеток. Кроме него в связывании вируса и его проникновении участвуют: рецепторы CXCR4 и CCR5 со стороны клетки и поверхностные гликопротеины gp120 и gp41 — со стороны вируса.
Сейчас FDA (американское Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) одобряет четыре лекарства, работающие на этой стадии. Каждый связывается с каким-то из участников процесса и мешает его работе. Например, к этой группе принадлежит самый новый препарат против ВИЧ — фостемсавир, его одобрили в США в июле 2020 года. В организме он превращается в активную форму темсавир, соединяется с вирусным гликопротеином gp120 и мешает ему связаться с клеточным рецептором CD4. Другой препарат — ибализумаб — связывается с самим CD4, причем так, что рецептор не может участвовать в проникновении вируса, но выполняет свою нормальную иммунную функцию — связывает и узнает антигены на поверхности антигенпрезентирующих клеток.
Подобные препараты также используются для лечения респираторно-синцитиального вируса, вирусов ветряной оспы и простого герпеса. Они тоже действуют на вирусные гликопротеины и их связывание с клеточными рецепторами. К этой же группе можно отнести препараты для пассивной иммунопрофилактики антителами.
2. Подготовка к размножению, часть 1
Когда вирус попал в клетку, он должен в ней размножиться, то есть создать копии себя, используя ресурсы самой клетки. Так как ВИЧ — ретровирус, его генетический материал — РНК, которая должна достроиться до двухцепочечной ДНК и встроиться в ДНК клетки. Процесс достраивания называется обратной транскрипцией, и для него необходим вирусный фермент обратная транскриптаза, ее еще называют ревертазой. Это самая популярная мишень препаратов против ВИЧ, которые делятся на две группы: нуклеозидные и ненуклеозидные.
3. Подготовка к размножению, часть 2
Чтобы наконец размножиться, ВИЧ, уже в виде молекулы ДНК, необходимо встроиться в геном клетки-хозяина. В этом участвует другой вирусный фермент — интеграза. Ее ингибируют несколько одобренных лекарств, причем они часто используются вместе с другим препаратом — кобицистатом. Он никак не действует на вирус, но ингибирует некоторые ферменты печени и увеличивает биодоступность самих антивирусных препаратов.
Попав в геном, вирус может запустить транскрипцию и синтезировать новые РНК и белки. А может и «заснуть». Именно поэтому ВИЧ почти нельзя вылечить: всегда останутся клетки со «спящим» вирусом, который себя не проявляет, а значит, не может быть мишенью для атаки. Активация вируса связана с активацией клетки. Так как ВИЧ инфицирует в основном иммунные клетки, именно те из них, что борются с инфекцией, и становятся его жертвой.
4. Созревание
Белки ВИЧ синтезируются в виде длинных полипротеинов, которые нужно «нарезать», чтобы получить зрелые формы. Для этого необходим вирусный фермент протеаза. Это — вторая по популярности мишень антивирусных препаратов. Большинство из них — белковые аналоги вирусного полипептида. Они ингибируют работу фермента, и зрелые вирусные белки и новые вирусные частицы не образуются. Подобно ингибиторам обратной транскриптазы, к препаратам из этой группы тоже очень быстро развивается резистентность. И, как и с ингибиторами вирусной интегразы, с ними часто используется кобицистат.
Препараты ингибирования вирусной протеазы также существуют для лечения вируса гепатита С. Несмотря на большие отличия в структуре и способе репликации, белки этого вируса тоже синтезируются в незрелой форме, которую нужно «нарезать».
Другие препараты
Есть три группы антивирусных препаратов, которые мы еще не упоминали. Во-первых, это ингибиторы белков NS5A и NS5B вируса гепатита С, которые играют важную роль в репликации РНК вируса. Во-вторых, лекарства против вируса гриппа: три ингибитора вирусного белка нейраминидазы и один ингибитор РНК-полимеразы вируса. И, наконец, сборная солянка препаратов, которые не действуют прицельно на вирусные компоненты. Это интерфероны, а также иммуностимуляторы и ингибиторы митоза клеток.
Первые заслуживают особого внимания из-за обилия отечественных лекарств против гриппа и простуды на их основе. FDA одобряет инъекции (!) интерферонов только для лечения гепатита B и С, причем на практике они используются очень осторожно из-за серьезных побочных эффектов. Отечественные противовирусные препараты с интерферонами, которые выпускаются в форме мазей, спреев и суппозиториев, вряд ли работают. И слава богу. Иммуностимуляторы и ингибиторы митоза клеток выпускаются в виде мазей и используются для лечения генитальных бородавок, то есть папилломавируса человека.
Наука не стоит на месте, и разработка противовирусных препаратов продолжается, подстегиваемая новыми вирусами, эпидемиями, а также развитием резистентности к существующим лекарствам. Но по-прежнему самыми изученными и многочисленными препаратами остаются ингибиторы вирусных обратной транскриптазы или ДНК-полимеразы и протеазы. Для разработки других стратегий борьбы ученым еще предстоит изучить детали работы вирусов — как давно известных, так и совершенно новых.
Да, вирусы остаются источником зловещих идей в популярной культуре. Но существующих препаратов и методов уже достаточно, чтобы мы могли избежать заражения, быстро вылечиться или свести негативные последствия болезни к нулю.