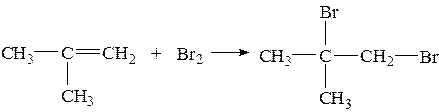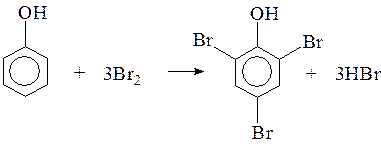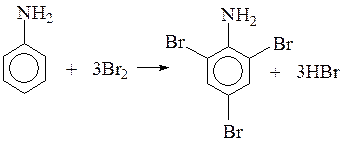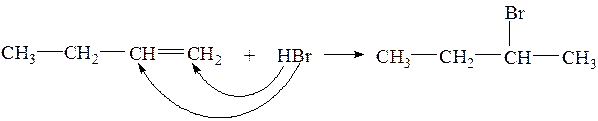Кто может обесцвечивать бромную воду и что это значит? (алкены, алкины, диены, фенол, анилин, стирол почему именно они)



Обесцвечивать бромную воду – это значит взаимодействие с бромом Br2 растворенным в воде при обычных условиях.
Алкены (также стирол) алкины и диены могут реагировать с бромной водой, присоединять бром с разрывом кратных связей, при этом бурая вода обесцвечивается. Также циклопропан и циклобутан может присоединять бром, при этом цикл разрывается, так как они имеют очень слабый цикл.
|
Анилин и фенол могут обесцвечивать бромную воду, вступают в реакции замещения с бромом, при этом бурая вода обесцвечивается и выпадают белые осадки.
|
|
34. Правило Зайцева и Марковникова. (хим св-ва алкенов)
Правило Марковникова: в реакциях гидрогалогенирования и гидратации водород присоединяется всегда к более гидрированному атому углерода при двойной связи(к атому углерода с большим числом атомов водорода).
|
|
Правило Зайцева: в реакциях дегидратации и дегидрогалогенирования водород отщепляется от наименее гидрированного атома углерода по соседству с функциональной группой (-ОН или –Cl, к примеру)
Химия, Биология, подготовка к ГИА и ЕГЭ
Качественные реакции органической химии
В качественном анализе используют легко выполнимые, характерные химические реакции, при которых наблюдается появление или исчезновение окрашивания, выделение или растворение осадка, образование газа и др. Реакции должны быть как можно более селективны и высокочувствительны.
Итак, классы органических соединений и соответствующие им качественные реакции:
| Класс органических соединений | Качественные реакции |
| Алканы | У алканов нет качественных реакций. Их определяют методом исключения |
| Алкены | 1. Обесцвечивание бромной воды: 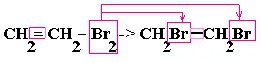 2. Изменение окраски раствора 2. Изменение окраски раствора 3СH2=CH2 + 2 KMnO4 + 4H2O → 3C2H4(OH)2 + 2 MnO2 + 2KOH |
| Циклоалканы | Обесцвечивание бромной воды: 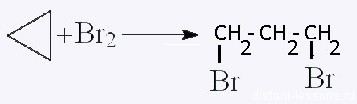 |
| Алкины | 1. Обесцвечивание бромной воды, 2. Образование ацетиленидов серебра и меди:  3. Изменение окраски перманганата калия: (KMnO4 → MnO2) C2H2 → HOOC-COOH |
| Алкадиены | Т.к. алкадиены содержат 2 двойные связи, то они так же как и алкены, обесцвечивают бромную воду |
| Арены | 1. Взаимодействие с бромом (в присутствии катализатора) 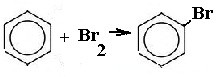
|
| Спирты | Реакция с оксидом меди — в осадок выпадает медь: 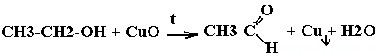 |
| Многоатомные спирты | С гидрокисдом меди (II) — Cu(OH)2 образуется комплекс синего цвета |
| Альдегиды | Реакция «серебряного зеркала» и реакция «медного зеркала»: 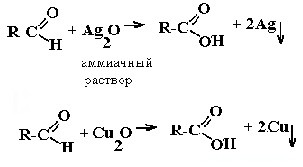 |
| Кислоты органические | Дают окрашенные соли тяжелых металлов — см. таблицу растворимости |
| Амины | Качественных реакций нет (только анилин — имеет характерный запах) |
Как вы видите, все вещества, имеющие кратные связи (кратные=двойные и тройные), обесцвечивают бромную воду. Многие из них изменяют окраску раствора перманганата калия. Поэтому эти вещества надо разделять по их индивидуальным, характерным только для них качественным реакциям.
Здесь перечислены самые основные качественные реакции органической химии. Если говорить о высокомолекулярных соединениях — белках, жирах, углеводах, то для них качественные реакции определяются функциональными группами, входящими в состав. Зная функциональную группу, вы легко сможете подобрать реактив, т.к. в таблице они разобраны именно по классам.
Почему обесцвечивается бромная вода
Бромная вода представляет собой водный раствор брома. Она способна окислять металлы, а также ряд органических соединений. При реакции с соединениями, содержащими кратные связи, она обесцвечивается. Этот процесс представляет собой качественную реакцию на непредельность органических соединений. Исчезновение окраски раствора является доказательством непредельности.
Примеры реакций обесцвечивания бромной воды
При реакции бромной воды с алкинами и алкенами, полученный раствор обесцвечивается. Алкенам свойственна ненасыщенная двойная связь, а для алкинов – тройная связь, чем определяются их свойства. В ходе взаимодействия разрываются двойные и тройные связи, присоединяется бром. В результате образуются бромистые соединения. Алканы не обесцвечивают бромную воду.
Водный раствор брома также теряет цвет при взаимодействии с непредельными маслами, которые также имеют двойные и тройные связи.
При реакции йодистого калия и водного раствора брома, выводятся молекулы свободного йода, и происходит обесцвечивание раствора.
Для того, чтобы убедиться в приведенных примерах, достаточно простого смешивания указанных веществ в лабораторных условиях. Нагревание, воздействие света, участие катализаторов при этом не требуется. Такие эксперименты проводят во время обучения в школе и учреждениях профессионального образования, а вот проводить их в домашних условиях не стоит, так как бром токсичен и обладает сильным неприятным запахом.
Методические рекомендации для подготовки к ЕГЭ по химии
Методические рекомендации к решению задания 25
«Качественные реакции на неорганические вещества и ионы. Качественные реакции органических соединений».
Качественная реакция на алканы.
Алканы не обесцвечивают раствор перманганата калия и бромную воду.
Качественная реакция на алкены.
а) При взаимодействии алкена с водным раствором перманганата калия при комнатной температуре (0 0 С-25 0 С) происходит обесцвечивание характерной окраски раствора с образованием бурого осадка:
3СН 2 = СН 2 + 2 KMnO 4 + 4 H 2 O → 3 CH 2 ( OH ) − CH 2 ( OH ) + 2 MnO 2 ↓ + 2 KOH
Если использовать кислый раствор перманганата калия, то раствор становится совершенно бесцветным:
б) Алкены обесцвечивают бромную воду. При этом бромная вода (иодная вода), имеющая желтую окраску, обесцвечивается.
Рекомендации учителю : при демонстрации опыта бромную воду лучше заменить иодной водой (разбавленный водой аптечный спиртовый раствор иода) как менее токсичным раствором.
Нейтральный раствор перманганата калия брать слабоокрашенным, тогда при взаимодействии с алкеном происходит не побурение раствора, а почти полное обесцвечивание его, что лучше убеждает учащихся.
Качественная реакция на алкины.
а) Алкины, так же как и алкены, обесцвечивают раствор перманганата калия и бромную воду:
3 CH ≡ CH + 8 KMnO 4 → 3 KOOC − COOK + 8 MnO 2 ↓ + 2 KOH + 2 H 2 O
б) Алкины с тройной связью у крайнего атома углерода реагируют с аммиачным раствором оксида серебра Ag [( NH 3 ) 2 ] OH
СН ≡ СН + 2 Ag [( NH 3 ) 2 ] OH → Ag – С ≡ С – Ag ↓ + 4 NH 3 + 2 H 2 O
Признаком реакции является образование коричневого осадка.
СН ≡ СН + 2 Cu [( NH 3 ) 2 ] Cl → Cu – С ≡ С – Cu ↓ + 2 NH 3 + 2 NH 4 Cl
СН 3 –С ≡ СН + Cu [( NH 3 ) 2 ] Cl → СН 3 – С ≡ С – Cu ↓ + NH 4 Cl + NH 3
Алкины у которых тройная связь в середине ( R – С ≡ С – R ) в реакцию замещения не вступают. Эти реакции позволяют отличить алкины с концевой тройной связью от алканов, алкенов и алкинов с тройной связью в середине углеродной цепи.
Качественная реакции на алкадиены.
Алкадиены как непредельные углеводороды, обесцвечивают раствор перманганата калия и бромную воду.
5) Качественная реакция на арены.
а) Бензол не обесцвечивает бромную воду и раствор перманганата калия. Но при действии нитрующей смеси образует желтую жидкость с запахом горького миндаля – нитробензол.
б) гомологи бензола окисляются раствором перманганата калия и обесцвечивают его.
в) Стирол как непредельное соединение обесцвечивает бромную воду и раствор перманганата калия
6) Качественная реакция на спирты.
Спирты по числу гидроксильных групп бывают одно-и многоатомными. Для одно- и многоатомных спиртов качественные реакции различны.
а) Качественные реакции на одноатомные спирты:
Окисление спирта оксидом меди ( II ). Для этого пары спирта пропускают над раскаленным оксидом меди.
СН 3 − СН 2 − OH + CuO → СН 3 − CHO + H 2 O + Cu
Черный цвет проволоки меняется на красный. Появляется резкий запах альдегида.
Рекомендации учителю: для получения черного оксида меди ( II ) медную проволоку скручивают в спираль и прокаливают в пламени спиртовки. Раскаленную, покрытую оксидным слоем, проволоку опускают в спирт. Следят за изменением цвета проволоки и появлением нового запаха.
б) Качественная реакция на многоатомные спирты.
Качественной реакцией на многоатомные спирты, содержащие гидроксильные группы у соседних атомов углерода, является их взаимодействие со свежеосажденным гидроксидом меди ( II ). При этом наблюдается растворение голубого осадка и образование ярко синего раствора.
Рекомендации учителю : получая осадок гидроксида меди( II ), добавляют избыток щелочи. Это условие позволяет растворить осадок и получить ярко синий раствор.
7 ) Качественная реакция на фенол.
а) Качественной реакцией на фенол является его взаимодействие с раствором хлорида железа (III), в результате которого образуется интенсивно окрашенное комплексное соединение фиолетового цвета.
б) Взаимодействие фенола с бромной водой также является качественной реакцией на фенол. Образуется осадок белого цвета-2,4,6-трибромфенол:
а) Реакция «серебряного зеркала».
CH 3 − CHO + 2[ Ag ( NH 3 ) 2 ] OH CH 3 − COONH 4 + 2 Ag ↓ + 3 NH 3 ↑ + H 2 O
HCOH + 4[ Ag ( NH 3 ) 2 ] OH (избыток) CO 2 ↑ + 3 H 2 O + 4 NH 3 ↑ + 4 Ag ↓
Образуется серебристый зеркальный налет на стенках пробирки при нагревании аммиачного раствора оксида серебра с альдегидами.
Рекомендации учителю : на успех опыта в большей степени влияет чистота стенок сосуда и в меньшей степени характер нагревания. Мельчайшее загрязнение мешает серебру зацепиться за стекло и заставляет его выпадать в виде рыхлого черного осадка, что, тем не менее, доказывает восстановление серебра.
б) Образование красного осадка при нагревании альдегидов со свежеосажденным гидроксидом меди (II).
Для этого к свежеприготовленному гидроксиду меди (II) добавляют альдегид и нагревают смесь:
CuSO 4 + 2 NaOH = Na 2 SO 4 + Cu ( OH ) 2 ↓( получение гидроксида Cu (II))
CH 3 − CHO + 2 Cu ( OH ) 2 CH 3 − COOH + Cu 2 O ↓ + 2 H 2 O
HCOH + 4 Cu ( OH ) 2 (избыток) CO 2 + 2 Cu 2 O ↓ + 5 H 2 O
Выпадает красный осадок оксида меди ( I ).
9 ) Качественные реакции на карбоновые кислоты .
Качественные реакции на предельные одноосновные карбоновые кислоты:
а) Изменение цвета индикатора (лакмус на красный, метилоранжевый на красный, фенолфталеин остается бесцветным).
Окраску индикатора изменяют растворимые и слаборастворимые кислоты.
Стеариновая и пальмитиновая кислоты, как нерастворимые вещества, окраску индикатора изменить не могут.
б) Более сильные карбоновые кислоты вытесняют углекислый газ из карбонатов и гидрокарбонатов. Наблюдается вспенивание. Выделяющийся углекислый газ вызывает помутнение известковой воды:
Эта реакция позволяет отличить карбоновые кислоты от фенолов.
в) Качественные реакции на метановую (муравьиную кислоту) кислоту HCOOH.
— При добавлении концентрированной серной кислоты к раствору муравьиной кислоты образуется угарный газ и вода:
Угарный газ можно поджечь. Горит синим пламенем:
2CO + O 2 2CO 2
— Реакция «серебряного зеркала»
— Образование красного осадка с гидроксидом меди (II).
г) Качественная реакция на олеиновую кислоту.
— обесцвечивание раствора перманганата калия
— обесцвечивание бромной или иодной воды
R− CH = CH − RCOOH + Br 2 → R− CHBr – CHBr − RCOOH
10) Качественные реакции на амины.
а) Растворы аминов изменяют окраску индикаторов, так как среда раствора щелочная. Анилин как нерастворимое вещество окраски индикаторов не меняет.
б) Первичные амины при взаимодействии с азотистой кислотой HNO 2 образуют газ.
Рекомендации учителю: азотистую кислоту для начала нужно приготовить
NaNO 2 + HCl → NaCl + HNO 2
а затем добавить амин:
в) Вторичные амины с азотистой кислотой дают вещества с резким запахом — нитрозоамины:
CH 3 − NH − CH 3 + HNO 2 → CH 3 − N ( NO )− CH 3 + H 2 O
г) Третичные амины в мягких условиях с HNO 2 не реагируют.
д) Анилин образует осадок при добавлении бромной воды:
Анилин также можно обнаружить по сиреневой окраске при добавлении хлорной извести.
Качественные реакции на углеводы.
а) Качественные реакции на глюкозу:
— реакция «серебряного зеркала»
— взаимодействие с гидроксидом меди ( II )
без нагревания глюкоза дает ярко синий раствор как многоатомный спирт,
при нагревании глюкоза окисляется до глюконовой кислоты (реакция на альдегидную группу) и образуется красный осадок оксида меди ( I )
CH 2 ОН( CHO Н) 4 СНО + Cu ( OH ) 2 CH 2 ОН( CHO Н) 4 СОО H + Cu 2 O ↓ + 2 H 2 O
б) Качественная реакция на крахмал:
Крахмал в присутствии иода окрашивается в темно-синий цвет. При нагревании окраска исчезает, при охлаждении появляется вновь.
Белки выявляются в основном на реакциях, основанных на окрасках.
Ксантопротеиновая реакция. При действии на белки концентрированной азотной кислотой образуется желтая окраска, связанная с нитрованием ароматических колец в соответствующих аминокислотах
Обнаружение серосодержащих аминокислот:
Белок + (CH 3 COO) 2 Pb + NaOH →PbS↓ (осадок черного цвета).
Биуретовая реакция для обнаружения пептидной связи (CO-NH)
Белок + CuSO 4 + NaOH → фиолетовое окрашивание.