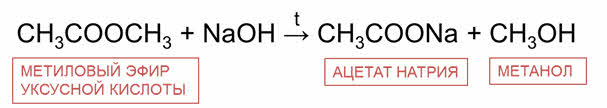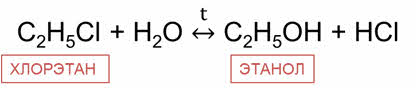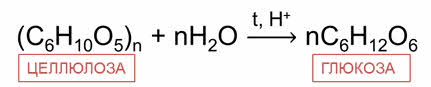Гидролиз белков
Общие понятия о белках
Мономерными звеньями белков выступают пептиды, которые состоят из аминокислот. Если вещество содержит более, чем 100 аминокислотных остатков его классифицируют как протеин, менее 100 – это ещё пептид. Образование белков (пептидная связь) схематично можно изобразить следующим образом:
Гидролиз белков
Белки способны частично гидролизоваться. Если представить, что гидролиз протекает до конца, т.е. полностью, то в качестве продуктов реакции получается смесь аминокислот. Кроме этих веществ в растворе после гидролиза были найдены углеводы, пиримидиновые и пуриновые основания, ортофосфорная кислота. Гидролиз белков протекает при определенных условиях: кипячение в растворе кислоты или щелочи.
Если в составе белков имеются амидные связи за счет наличия аминокислот с разветвленными боковыми радикалами, создающими стерические препятствия, как например в лейцине или валине, то гидролиз невозможен.
Если белок распадается на составляющие в щелочной среде, то гидролиз проводят в кислой и наоборот.
Условно уравнение реакции гидролиза белков можно записать как:
Для чего нужен гидролиз белков?
Поскольку белки являются высокомолекулярными соединения, то они могут плохо восприниматься организмом, так как любой продукт питания, растительного или животного происхождения имеет в составе белки. Гидролиз разрушает белки до низкомолекулярных продуктов, поэтому его используют для ускорения усвояемости белков (спортивное питание), снижения аллергических реакций (детское питание, в особенности молочные смеси), получения аминокислот.
Примеры решения задач
| Задание | Напишите уравнение реакции гидролиза белков имеющих общую формулу (-NH-CH(R)-CO-)n. |
| Решение | Уравнение реакции будет выглядеть следующим образом: |
| Задание | В чем заключается суть гидролиза белков под действием ферментов (энзимов)? |
| Решение | Гидролиз белков под действием ферментов является естественным процессом, который протекает в человеческом организме в ходе пищеварения. Под действием энзимов белки распадаются до аминокислот и усваиваются организмом. Подобную реакцию можно провести и в лабораторных условиях: сначала осуществляют реакцию денатурации белка – нарушение структуры – под действием нагревания, а затем полученную фракцию смешивают с ферментами. Так получают спортивное питание. |
Копирование материалов с сайта возможно только с разрешения
администрации портала и при наличие активной ссылки на источник.
Типы гидролиза белка. Какие промежуточные и конечные продукты образуются при гидролизе белка?
Гидролиз – распад сложного вещества на более простые составные части, связанный с присоединением воды по месту разрыва связей. В зависимости от применяющегося катализатора различают кислотный, щелочной и ферментативный гидролиз.
Кислотный гидролиз осуществляется кипячением раствора белка в течение 16-92 часов, при температуре 110 0 с нормальным раствором кислоты. Щелочной гидролизпроизводится кипячением раствора белка в течение 4 – 8 часов, при 110 0 с нормальным раствором NaOH. Ферментативный гидролиз происходит при участии ферментов протеиназ (пептидаз): трипсин, пепсин. В отличие от кислотного и щелочного гидролиза ферментативный гидролиз (протеолиз) наиболее специфичен, при нём ферменты расщепляют только определённые связи в белках. Окончание процесса гидролиза оценивают по двум признакам: а) отсутствие положительной биуретовой реакции на пептидные связи и б) окончание прироста концентрации аминогрупп и карбоксильных групп в гидролизате. Динамику прироста аминогрупп и карбоксильных групп определяют методом формольного титрования, связывая формальдегидом аминогруппы аминокислот, освобождающихся при гидролизе белка. Образовавшиеся при гидролизе аминокислоты идентифицируют методом хроматографического анализа, основанном на разных физико-химических свойствах аминокислот.
В организме гидролиз белка постоянно протекает в процессе как пищеварения, так и жизнедеятельности клеток под действием протеолитических ферментов. Действие протеолитических ферментов может быть разделено на две различные категории:
При кислотном гидролизе белка разрушаются некоторые аминокислоты (триптофан подвергается полному разрушению, серин, треонин, цистин, тирозин, фенилаланин – частичному). При щелочномм гидролизе отмечается значительно более сильное разрушение аминокислот.
Продуктами полного гидролиза белков являются аминокислоты. В качестве промежуточных продуктов гидролиза образуются пептиды и полипептиды.
Биосинтез жирных кислот: этапы, последовательность реакций, ферменты.
Источником синтеза ЖК является малонил КоА, образующийся из ацетил КоА.
Образование малонил КоА из ацетил КоА.
Ацетил КоА поступает из матрикса митохондрий в цитоплазму с помощью карнитина и фермента ацетил КоА карнитинтрансферазы, которые переносят ацетильные остатки.
Стадии синтеза ЖК.
1)Перенос ацетила с ацетил КоА на синтетазу с участием ацетилтрансацилазы. Ацетил является затравкой в синтезе.
2)Перенос малоноила с малонил КоА на синтетазу с участием малонилтрансацилазы.
3)Конденсация ацетила с малонилом и декарбоксилирование образовавшегося продукта с участием бета-кетоацилсинтетаза.
4)Первое восстановление промежуточного продукта с участием НАДФН2.
5)Дегидратация промежуточного продукта с участием гидроксиацил-гидратазы.
6) Второе восстановление промежуточного продукта с участием НАДФН2.
Образуется бутирил, связанный с ферментом. Синтезированный бутирил переносится с участием ацетилртансацилазы на ту SH-группу, с которой вначале был связан затравочный ацетил. На освободившуюся SH-группу поступает новый малонильный остаток. Цикл синтеза повторяется.
Белки
Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями.
Образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот:
Макромолекулы белков имеют стереорегулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Структуры белков
| Первичная структура — последовательность α-аминокислотных звеньев в полипептидной цепи | Вторичная структура – спиральная структура полипептидной цепи, закрепленная водородными связями между группами N-H и С=О |
 |  |
Химические свойства белков
Качественные реакции на белки
Денатурация белка
Это разрушение структуры белка при нагревании, изменении кислотности среды, действии излучения, спирта, тяжелых металлов, радиации.
Пример денатурации — свертывание яичных белков при варке яиц.
Денатурация бывает обратимой и необратимой.
Анализируя продукты гидролиза, можно установить количественный состав белков.
Классификация белков и их гидролиз
Общая характеристика и классификация белков как высокомолекулярных органических соединений. Процесс разрушения первичной структуры белков. Особенности кислотного, энзимного и щелочного гидролиза белков. Значение аминокислот для организма человека.
| Рубрика | Биология и естествознание |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 28.05.2015 |
| Размер файла | 19,3 K |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Белки разделяются на протеины (простые белки), состоящие только из аминокислот и при гидролизе почти не образующие других продуктов, и протеиды (сложные белки), состоящие из собственно белковой части, построенной из б-аминокислот, и из соединенной с ней небелковой части, иначе называемой простетической группой. При гидролизе протеиды кроме б-аминокислот образуют и другие вещества, например, фосфорную кислоту, глюкозу, гетероциклические соединения и т. д.
1. Протеины разделяются на группы в зависимости от их растворимости и положения изоэлектрической точки:
1) Альбумины. Растворимы в воде, при нагревании свертываются. Осаждаются насыщенными растворами солей (не осаждаются насыщенным раствором хлорида натрия NaCl, но могут быть осаждены при насыщении раствора сульфатом аммония). Имеют сравнительно небольшую молекулярную массу. При гидролизе дают мало гликоколя. Входят в состав белка яйца, сыворотки крови, молока, а также ферментов и семян растений.
2) Глобулины. Нерастворимы в воде. Растворяются в разбавленных растворах солей и осаждаются концентрированными растворами солей. Свертываются при нагревании. Имеют большую молекулярную массу, чем альбумины. Входят в состав мышечных волокон (миозин), яйца, молока, крови, растительных семян (конопля, горох).
3) Проламины. Нерастворимы в воде. Растворяются в 60—80 %-ном спирте. Не свертываются при кипячении. Содержат много пролина. Входят в состав растительных белков (глиадин пшеницы, гордеин ячменя, зеин кукурузы).
2. Протеиды разделяются на группы в зависимости от состава небелковой части:
1) Нуклеопротеиды. Гидролизуются на простой белок (чаще всего гистоны или протамины) и нуклеиновые кислоты. Последние в свою очередь гидролизуются с образованием углевода, фосфорной кислоты, гетероциклического основания. Растворимы в щелочах и нерастворимы в кислотах. Входят в состав протоплазмы, клеточных ядер, вирусов.
3) Гликопротеиды. Гидролизуются на простой белок и углевод. Нерастворимы в воде. Растворяются в разбавленных щелочах. Нейтральны. Не свертываются при нагревании. Входят в состав слизей. Представитель: муцин, входящий в состав слюны.
4) Хромопротеиды. Распадаются при гидролизе на простой белок и красящее вещество. Примером является гемоглобин крови; при гидролизе он расщепляется, образуя белок глобин и красящее вещество гем красного цвета.
5) Липопротеиды. Это соединения белка с липидами. Содержатся в протоплазме клеток, в сыворотке крови, в яичном желтке.
Белки классифицируются также по форме их молекул:
1) фибриллярные (волокнистые) белки, молекулы которых имеют нитевидную форму; к ним относят фиброин шелка, кератин шерсти;
2) глобулярные белки, молекулы которых имеют округлую форму; к ним относятся, например, альбумины, глобулины и ряд других, в том числе и сложные белки.
классификация гидролиз белок
Процесс гидролиза белков
2.1 Кислотный гидролиз
2.2 Энзимный (ферментативный) гидролиз белка
На первом этапе ферментного гидролиза сырье подвергают легкой температурной обработке. В итоге белок частично денатурирует (разрушается). После чего полученную фракцию смешивают с ферментами, которые завершают процесс гидролиза.
2.3 Щелочной гидролиз белка
При щелочном гидролизе происходит рацемизация большинства аминокислот и полное разрушение аргинина, лизина, цистина и цистеина. В результате такого гидролиза образуется комплекс дефектных, чуждых организму компонентов.
А насчет применения гидролиза в органике, то чаще это связано с получением тех или иных соединений, активные группы которых защищают для того, чтобы на этапе синтеза они не вступали в ненужные реакции. А затем путем гидролиза блокировку групп снимают. Очень часто гидролиз применяют в пептидном синтезе.
Например, щелочным гидролизом (омылением) кокосового жира получают основу для производства мыла. Триглицериды кокосового жира при этом распадаются на натриевые (калиевые) соли жирных кислот и глицерин.
3. Роль отдельных аминокислот для организма человека
Гамма-аминомасляная кислота незаменима в случаях заболевания артериальной гипертензией и эпилепсией.
Глутаминовая кислота необходима в случае язв или дистрофии мышц.
Глицин отвечает за скорейшее восстановление поврежденных тканей.
Изолейцин необходим для правильной регулировки уровня сахара в крови.
Лейцин ускоряет восстановлению или лечению мышечной ткани, костей и кожи.
Лизин необходим для правильного усвоения кальция, правильно распределяет его для роста и питания костей. Также он необходим для укрепления сердечного тонуса, усиливает резистентность организма, понижает уровень вредного холестерина в крови.
Метионин нужен для лечения аллергии химического происхождения, а также при остеопорозе.
Пролин отвечает за укрепление сердечной мышцы.
Серин балансирует обмен жирных кислот и жиров в организме.
Таурин просто необходим при гипогликемии, при заболевании атеросклерозом, отвечает за метаболизм желчной кислоты.
Треонин необходим для поддержания иммунитета, регулирует обмен белков и жиров, предотвращает отложение в печени жиров.
Тирозин очень полезен, если у человека хроническая усталость, данная аминокислота стоит перед гормонами щитовидки, также она отвечает за образование адреналина и норадреналина.
Триптофан, полезен сердечникам, а также при хронической бессоннице. Вообще триптофан синтезирует в организме огромное количество витамина РР, стоит непосредственно перед нейромедиатором серотонином. Именно серотонин отвечает за эмоциональное состояние человека, при недостатке человек впадает в депрессию.
Цистеин необходим для лечения ревматоидного артрита, используется при лечении рака и болезнях артерий.
Размещено на Allbest.ru
Подобные документы
Понятие белков как высокомолекулярных природных соединений (биополимеров), состоящих из остатков аминокислот, которые соединены пептидной связью. Функции и значение белков в организме человека, их превращение и структура: первичная, вторичная, третичная.
презентация [564,0 K], добавлен 07.04.2014
Физические, биологические и химические свойства белков. Синтез и анализ белков. Определение первичной, вторичной, третичной и четвертичной структуры белков. Денатурация, выделение и очистка белков. Использование белков в промышленности и медицине.
реферат [296,5 K], добавлен 10.06.2015
Физические и химические свойства, цветные реакции белков. Состав и строение, функции белков в клетке. Уровни структуры белков. Гидролиз белков, их транспортная и защитная роль. Белок как строительный материал клетки, его энергетическая ценность.
реферат [271,2 K], добавлен 18.06.2010
Белки (протеины) – высоко молекулярные, азотосодержащие природные органические вещества, молекулы которых построены из аминокислот. Строение белков. Классификация белков. Физико-химические свойства белков. Биологические функции белков. Фермент.
реферат [4,0 M], добавлен 15.05.2007
контрольная работа [199,0 K], добавлен 13.03.2013
Гидролиз органических веществ
Урок 24. Химия 11 класс ФГОС
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Гидролиз органических веществ»
Гидролиз – это реакция обменного разложения веществ водой.
К органическим веществам, которые подвергаются гидролизу относят: сложные эфиры и жиры, углеводы, белки, галогеналканы и другие.
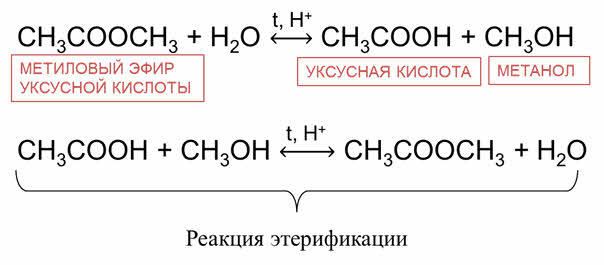
Например, при гидролизе сложного эфира образуется кислота и спирт. Так, при гидролизе метилового эфира уксусной кислоты образуется уксусная кислота и спирт метанол. Эта реакция обратимая, так как продукты реакции могут взаимодействовать друг с другом с образованием сложного эфира и воды.
Реакция получения сложного эфира из карбоновой кислоты и спирта называется реакцией этэрификации. Эта реакция также является обратимой.
В щелочной среде образуется не карбоновая кислота, а её соль и процесс гидролиза становится необратимым. Например, в реакции метилового эфира уксусной кислоты с гидроксидом натрия образуется соль – ацэтат натрия и спирт метанол.
Жиры – это сложные эфиры глицерина и высшей жирной кислоты. При гидролизе жиров образуются высшие карбоновые кислоты и многоатомный спирт глицерин.
В щелочной среде эта реакция становится необратимой. Сам процесс называется омылением, так как в результате его образуется соль высшей карбоновой кислоты – мыло. Так, в результате щелочного гидролиза трипальмитат глицерина образуется пальмитат натрия – мыло и спирт глицерин.
Впервые в 1817 году Шеврель осуществил синтез мыла из жира.
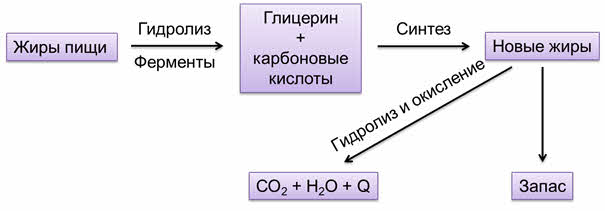
В организме человека и животных жиры пищи гидролизуются под действием ферментов с образованием глицерина и высших карбоновых кислот. В процессе синтеза эти вещества образуют новые жиры, которые откладываются про запас. Либо образовавшиеся жиры гидролизуются и окисляются до углекислого газа и воды, высвобождая при этом энергию.
Жиры используются для получения мыла. Энергия, которая образуется при расщеплении жиров превращается в тепловую, благодаря высвобождению энергии осуществляются биохимические реакции, осуществляется работа мышц, передаются нервные импульсы.
При гидролизе галогеналканов образуются спирты. Так, при гидролизе хлорэтана образуется спирт этанол.
Если идёт щелочной гидролиз, то реакция гидролиза является необратимой. В результате щелочного гидролиза хлорэтана также образуется спирт этанол, но данная реакция является необратимой.
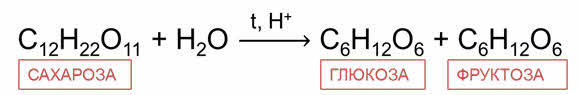
Из углеводов гидролизу подвергаются дисахариды и полисахариды. Так, при гидролизе сахарозы образуется глюкоза и фруктоза.
При гидролизе крахмала конечным продуктом является глюкоза.
Ступенчатый ферментативный гидролиз крахмала идёт следующим образом: сначала образуются декстрины, затем мальтоза и на конечной стадии образуется глюкоза.
При гидролизе целлюлозы также образуется глюкоза, которую затем можно использовать для получения этанола, сорбита, этиленгликоля, глицерина, карбоновых кислот.
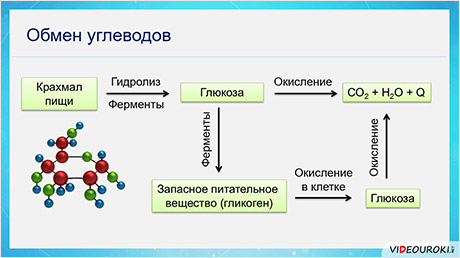
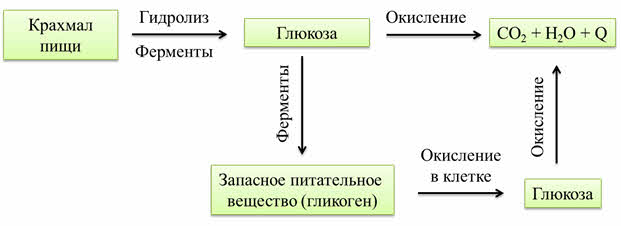
При попадании углеводов с пищей они подвергаются гидролизу под действием ферментов с образованием глюкозы. Эта глюкоза может сразу окисляться до углекислого газа и воды с высвобождением энергии, а может под действием ферментов использоваться как запасное питательное вещество – гликоген, который затем также окисляется и превращается опять в глюкозу, при окислении которой образуется углекислый газ и вода, и высвобождается энергия.
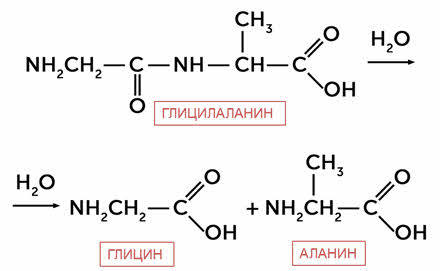
Гидролиз белков идёт с образованием конечных продуктов – альфа-аминокислот. Так, при гидролизе глицил-аланина образуется глицин и аланин.
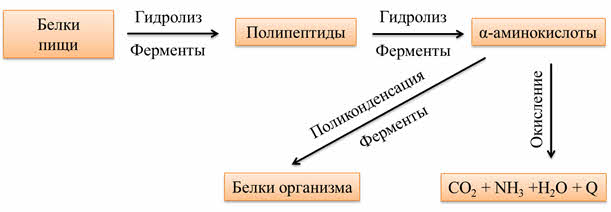
При попадании белков с пищей под действием ферментов они гидролизуются до полипептидов и дальше до альфа-аминокислот. Эти альфа-аминокислоты могут сразу окисляться до углекислого газа, аммиака и воды, при этом ещё выделяется энергия. Но альфа-аминокислоты могут под действием ферментов образовывать полипептиды, которые являются белками организма.
Гидролиз играет огромную роль в живых организмах и в научно-исследовательской деятельности.
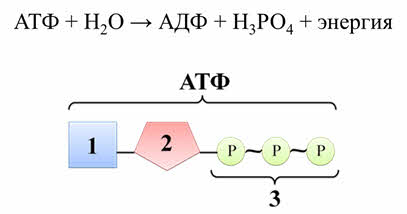
Гидролиз веществ требует затрат энергии. Эта энергия в живых организмах образуется в результате гидролиза а-тэ-эф. При гидролизе а-тэ-эф образуется а-дэ-эф, фосфорная кислота и выделяется энергия.
Энергия может переходить из одной формы в другую. Например, энергия химической связи, которая выделяется при гидролизе а-тэ-эф может превращаться в тепловую (которая необходима для поддержания температуры), механическую (которая необходима для сокращения мускулатуры), энергия может выделяться в виде электричества, как рыб скатов, энергия может выделяться в виде света, например, у насекомых, светящихся в темноте, кроме того, энергия используется и для передачи нервных импульсов.
Гидролиз органических веществ играет огромную роль в получении кормовых добавок, в пищевой и других видах промышленности. Таким образом, в органической химии гидролизу подвергаются сложные эфиры, жиры, углеводы, белки, галогеналканы и другие соединения.