Пиелонефрит (воспаление почек)
Пиелонефрит (воспаление почек) – инфекционно-воспалительный процесс, развивающийся в паренхиме (ткани почки) и чашечно-лоханочной системе.
Пиелонефрит (воспаление почек)
Принципиально пиелонефрит классифицируют на острый и хронический.
Острый пиелонефрит (воспаление почек)
– стремительно развивающееся и угрожающее жизни заболевание. Оно характеризуется нарастающим серозно-гнойным воспалением в почке, приводящим к выраженной интоксикации (отравлению организма инфекционными и прочими токсинами).
При этом пациент чаще всего предъявляет жалобы на боль в поясничной области («невозможно прикоснуться»), лихорадку (до 39 градусов с ознобом), выраженную общую слабость, головную боль, тошноту, рвоту, сухость во рту, вздутие живота. При отсутствии адекватного лечения воспаления почек может развиваться картина инфекционно-токсического шока: падение артериального давления, потеря сознания, тахикардия, бледность кожных покровов.
Основная отличительная черта острого воспаления почек – возможность быстрого прогрессирования с летальным исходом. Причина тому – особенности кровоснабжения. Через почки «проходит» 20-25 процентов циркулирующей крови, поэтому в ситуации, когда почка превращается, по сути, в гнойник существует опасность генерализации воспаления (распространения на весь организм).
Причины острого пиелонефрита
– инфекционный процесс в почке, вызываемый бактериями. Возбудители (чаще кишечная палочка – E.Coli) могут попадать в орган двумя основными способами: из нижних мочевых путей (например, из мочевого пузыря при хроническом цистите) и из крови (например, при наличии где-либо очага инфекции – кариес, тонзиллит, гайморит и т.д.). Однако на «ровном месте» пиелонефрит (воспаление почек) развивается крайне редко. Чаще всего существуют так называемые «предрасполагающие факторы»: мочекаменная болезнь, аномалии развития мочеполовых органов, наличие сужений мочеточников, аденома простаты и др.
При подозрении на острый пиелонефрит больного необходимо немедленно госпитализировать в специализированную клинику.
Хронический пиелонефрит (воспаление почек)
– вялотекущее инфекционно-воспалительное заболевание, характеризующееся поражением ткани (паненхимы) и чашечно-лоханочной системы почки.
В течении данного заболевания можно выделить две фазы. Ремиссия – затихание патологического процесса. Обострение – манифестация яркой клинической, лабораторной и патоморфологической симптоматики.
В основе хронического воспаления почек, как правило, лежат два компонента: нарушение оттока мочи из почек и наличие инфекции мочевыводящих путей.
Причины хронического пиелонефрита
— обычно развивается после острого пиелонефрита. Основные причины хронизации воспаления почек заключаются в следующем:
Хронический пиелонефрит – чрезвычайно распространенное заболевание. У взрослых воспаление почек встречается более чем у 200 человек на тысяч населения. При этом женщины страдают данным заболеванием в 4-5 раз чаще мужчин. Хронический пиелонефрит является самой частой причиной развития хронической почечной недостаточности.
Хроническое воспаление почек вялотекущее, но опасное заболевание. Суть его заключается в том, что по мере развития (периодические активизации и затухания воспаления) происходит постепенное рубцевание ткани почки. В конечном итоге орган полностью замещается рубцовой тканью и перестает выполнять свою функцию.
В фазе ремиссии хронический пиелонефрит может годами протекать без четкой клинической симптоматики. В начальных фазах воспаления почек больные могут периодически отмечать легкое недомогание, повышение температуры тела до субфебрильных значений (до 37,5 градусов), снижение аппетита, повышение утомляемости, слабые тупые боли в поясничной области, бледность кожных покровов. В анализе мочи наблюдается умеренное повышение количества лейкоцитов, бактериурия. При дальнейшем развитии воспаления почек отмечается прогрессирование описанных жалоб. Нарушение функции почек приводит к жажде, сухости во рту, образованию повышенного количества мочи, ночным мочеиспусканиям. В лабораторных анализах снижается плотность мочи. По мере углубления патологического процесса в почках развивается нефрогенная артериальная гипертензия (повышение давления), которая отличается особой «злокачественностью»: высокое диастолическое давление (более 110 мм.рт.ст) и устойчивость к терапии. В финальных стадиях заболевания отмечаются симптомы хронической почечной недостаточности.
Особую опасность имеет так называемый «пиелонефрит беременных». Суть его заключается в том, что увеличенная матка сдавливает мочеточники и нарушается отток мочи. На этом фоне возможно развитие тяжелых форм пиелонефрита, лечение которого весьма затруднительно, так как при беременности большинство антибиотиков противопоказаны. В этой связи у беременных необходим постоянный мониторинг показателей мочи. А при возникновении пиелонефрита (воспаления почек) часто требуется установка внутренних мочеточниковых стентов, осуществляющих отток мочи из почек.
Лечение пиелонефрита
Что главное? Больной должен понимать, что хронический пиелонефрит – «ласковый убийца» почек. И если с ним не бороться – он наверняка приведет вас в отделение гемодиализа. Современные же методы лечения воспаления почек вполне позволяют эффективно предупреждать развитие этого недуга.
Неотложная помощь при остром пиелонефрите и гематурии
Острый пиелонефрит — неспецифическое инфекционное воспаление чашечно-лоханочной системы и паренхимы почек. ОПН вызывают Escherichia соli, Klebsiella, Proteus, Pseudomonas.
Пути проникновения инфекционного агента в почку:
Предрасполагающие факторы развития острого пиелонефрита — нарушения гемо- или уродинамики в почке или верхних мочевых путях. Острый пиелонефрит чаще наблюдается у женщин.
Инфекция, попав в почку, получает благоприятные условия для своего развития в зонах гипоксии, где и возникает воспалительный процесс. Инфицированный тромб или эмбол в конечных сосудах коркового вещества почки вызывают инфаркт с последующим нагноением. Возникновение множественных мелких нагноившихся инфарктов в корковом веществе квалифицируют как апостематозный нефрит. Развитие обширного инфаркта с последующим нагноением ведет к формированию карбункула почки.
В отношении патогенеза заболевания различают первичный и вторичный пиелонефрит (рис. 1). В основе вторичного пиелонефрита лежат органические или функциональные изменения в почках и мочевых путях.
В зависимости от пассажа мочи по верхним мочевым путям, т. е. из почки в лоханку и далее по мочеточнику, различают острый пиелонефрит необструктивный (если он сохранен) и обструктивный (если нарушен).
Проявления острого пиелонефрита:
Часто острому пиелонефриту предшествует учащенное, болезненное в конце мочеиспускание (клиническая картина острого цистита).
Необструктивный острый пиелонефрит может начаться с дизурии и в тот же день или через 1–2 дня привести к высокой температуре тела, ознобу и боли со стороны пораженной почки. Озноб может сменяться проливным потом с кратковременным снижением температуры тела; боль в поясничной области в некоторых случаях появляется во время мочеиспускания и предшествует ознобу и лихорадке (пузырно-мочеточниковый рефлюкс!), а после них больше не повторяется (разрыв форникса одной или нескольких чашечек и резорбция мочи — форникальный рефлюкс!).
Обструктивный острый пиелонефрит (окклюзия мочеточника камнем, продуктами хронического воспаления почки, внешнее сдавление — ретроперитонеальный фиброз, рак внутренних половых органов, увеличенные лимфатические узлы и т. д.) начинается с постепенно нарастающей или острой боли в пояснице со стороны поражения с последующим ознобом и повышением температуры тела.
Осложнения обструктивного острого пиелонефрита:
Диагностика
При сборе анамнеза обращают внимание:
Проверяют соответствие частоты пульса температуре тела, выявляют боль в подреберье при пальпации живота и положительный симптом поколачивания по пояснице (симптом Пастернацкого) со стороны пораженной почки.
Лабораторная диагностика. В общем анализе мочи часто отмечается лейкоцитурия, которая при обструктивном остром пиелонефрите может отсутствовать, так как моча из пораженной почки не попадает в мочевой пузырь.
В общем анализе крови отмечается лейкоцитоз, нередко со сдвигом формулы крови влево (число палочкоядерных нейтрофилов составляет 20% и выше).
В биохимическом анализе крови возможно повышение показателей мочевины и креатинина, часто у пожилых и ослабленных больных, при хронической почечной недостаточности или поражении единственной функционирующей почки.
При посеве мочи (проводят до антибактериальной терапии) выделяют возбудителя заболевания и определяют его чувствительность к антибактериальным препаратам.
Для уточнения диагноза и формы острого пиелонефрита проводят:
Острый пиелонефрит дифференцируют со следующими состояниями:
Основные направления терапии
Алгоритм неотложной помощи при остром пиелонефрите представлен на рисунке 2.
Клиническая фармакология отдельных препаратов
Гентамицин эффективен в отношении инфекций, вызываемых грамположительными и грамотрицательными микроорганизмами, бактериями кишечной группы. Препарат быстро всасывается при внутримышечном введении, терапевтическая концентрация в крови достигается через 1 ч и сохраняется в течение 8–12 ч. Разовая доза составляет 80–160 мг, суточная — 160–320 мг. Побочное действие: нефро- и ототоксичность. Противопоказания к применению: снижение функции почек и пониженный слух.
Фторхинолоны (ципрофлоксацин, норфлоксацин, офлоксацин) активны в отношении большого числа грамположительных и грамотрицательных бактерий, выпускаются в формах для перорального и парентерального введения. Препараты хорошо всасываются в кишечнике и широко распределяются в жидкостях и тканях организма, секретируются главным образом почками. Период полувыведения — 3–7 ч. Наиболее широко при лечении острого пиелонефрита применяют ципрофлоксацин (медоциприн, сифлокс, ципровин) — 500 мг 2 раза в день, норфлоксацин (нолицин, норбактин) — 400 мг 2 раза в день и офлоксацин (зоноцин, офло, офлоксацин) — 200 мг 2 раза в день. Применение фторхинолонов противопоказано у детей до 14 лет, беременных женщин, а также при их индивидуальной непереносимости.
Часто встречающиеся ошибки терапии:
Показанием к госпитализации является большинство случаев острого пиелонефрита, в особенности если имеется подозрение на обструктивный характер поражения.
Разбор клинических случаев
Больная С., 18 лет. Жалобы на боли в левой поясничной области, повышение температуры тела до 38°С, сопровождающееся ознобом, тошноту, учащение и болезненность мочеиспусканий. Анамнез: 3 дня назад имело место переохлаждение, после чего мочеиспускания участились и стали болезненными, повысилась температура и появились боли. Принимала нитроксолин без эффекта. При осмотре: болезненность при пальпации в левых боковых отделах живота, симптом Пастернацкого резко положительный слева. Диагноз: острый необструктивный пиелонефрит слева. Больная госпитализирована в урологический стационар. Лечение: антибактериальная терапия гентамицином (80 мг 2 раза в сутки в/м).
Больная К., 29 лет. Жалобы на резкие боли в правой поясничной области, иррадиирующие в промежность, повышение температуры тела до 39°С с потрясающим ознобом, тошноту, неоднократную рвоту. Анамнез: длительное время страдает мочекаменной болезнью, ранее неоднократно самостоятельно отходили мелкие конкременты. Двое суток назад появились резкие боли в правой поясничной области, принимала баралгин и но-шпу с временным эффектом. Через день после начала болей отметила повышение температуры с ознобом, тошноту и рвоту. При осмотре: больная стонет от боли. Язык сухой, ЧСС 90 уд/мин. Живот мягкий, резко болезненный при пальпации в правых боковых отделах, симптом Пастернацкого резко положительный справа. Диагноз: правосторонняя почечная колика. Острый обструктивный пиелонефрит справа. Больная госпитализирована в урологический стационар. Лечение: катетеризация правого мочеточника, при невозможности ее выполнения — нефростомия справа. Интенсивная дезинтоксикационная и антибактериальная терапия.
Больной Ш., 67 лет. Жалобы на озноб, повышение температуры тела до 39,5°С, боли в пояснице справа. Анамнез: 3 мес назад произведена радикальная цистопростатэктомия по поводу рака мочевого пузыря, пластика мочевого пузыря кишечным лоскутом по Штудеру. При предоперационном обследовании у больного выявлена аплазия левой почки. Через месяц после операции появились постоянные тянущие боли в правой поясничной области, к врачам не обращался. В течение последней недели уменьшилось количество выделяемой мочи, появились отеки ног. Трое суток назад отметил повышение температуры на фоне усиления болей в правой поясничной области, температура прогрессивно повышалась, достигла 39,5°С и сопровождалась ознобами, объем мочи в сутки не превышал 200 мл. При осмотре: больной бледный, астенического сложения, отмечаются отеки нижних конечностей. Пальпаторно определяется выраженная болезненность в правых боковых отделах живота, симптом Пастернацкого резко положительный справа. Диагноз: острый обструктивный пиелонефрит справа. Стриктура правого уретеронеоцистанастомоза. Олигурия. Больной госпитализирован в урологический стационар. Лечение: экстренная нефростомия справа.
Гематурия — патологический симптом, характеризующийся примесью крови в моче.
Основные причины почечных кровотечений представлены в таблице 1.
Эссенциальная гематурия (табл. 2) объединяет ряд состояний, при которых неизвестны этиология и патогенез, а клинико-рентгенологические и морфологические исследования не позволяют точно указать причину кровотечения.
К гематурии может приводить прием ненаркотических анальгетиков, антикоагулянтов, циклофосфамида, оральных контрацептивов, винкристина.
При новообразованиях почки при прорастании опухоли в лоханке или чашечках нарушается целостность сосудистой стенки. Если опухоль не сообщается с чашечно-лоханочной системой, венозный отток из зоны почки с опухолевым узлом нарушается, форникальные вены расширяются и разрываются.
При раке предстательной железы опухоль прорастает в стенки мочевого пузыря или простатического отдела уретры, вены мочевого пузыря в его шеечном отделе сдавливаются опухолью, возникает венозный стаз. Свободно флотирующие ворсинчатые опухоли мочевого пузыря, располагающиеся поблизости от его шейки, во время мочеиспускания увлекаются током мочи в мочеиспускательный канал, закупоривают его просвет и, ущемляясь, набухают, лопаются и начинают кровоточить.
При цистите и простатите слизистая шейка мочевого пузыря воспаляется, травмируется и легко кровоточит при соприкосновении с другими стенками в конце акта мочеиспускания.
При нарушении почечной гемо- и уродинамики венозные сплетения форниксов при нарушенном венозном оттоке или значительном повышении внутрилоханочного давления переполняются кровью, вены, кольцевидно охватывающие своды чашечек, расширяются и нарушается их целостность, что приводит к гематурии из верхних мочевых путей.
При некрозе почечных сосочков нарушается кровоснабжение сосочка, а иногда и всей мальпигиевой пирамиды, некротизированная ткань отторгается, возникает кровотечение.
При доброкачественной гиперплазии простаты возникает венозный застой в органах малого таза, нарушается целостность сосудов.
Различают два вида гематурии:
Клиническая картина
Появление в моче эритроцитов придает ей мутный вид и розовую, буро-красную или красновато-черную окраску в зависимости от степени гематурии. Гематурия может возникать внезапно, быть однократной или повторяться. Ее прекращение обманчиво, так как причина гематурии, как правило, оказывается не устранена, и обследование при повторных кровотечениях с большим опозданием часто выявляет уже запущенную опухоль.
При опухоли почки гематурия может быть первым и длительное время единственным симптомом заболевания. В большинстве случаев она безболезненна, но при профузном кровотечении с образованием сгустков в почечной лоханке и их прохождении через мочеточники возникают тупые, реже коликообразные боли в поясничной области. При папиллярных опухолях мочевого пузыря гематурия обычно безболезненная и носит профузный характер без образования сгустков. При ворсинчатых опухолях мочевого пузыря, располагающихся около его шейки, струя мочи во время мочеиспускания может прерываться.
При туберкулезном поражении почек в самых ранних стадиях процесса наблюдается тотальная гематурия, которая может сопровождаться стойкой пиурией.
При доброкачественной гиперплазии простаты гематурия возникает без видимой причины либо при катетеризации мочевого пузыря вследствие нарушения целостности разрыхленной слизистой оболочки задней уретры.
При остром цистите и простатите терминальная гематурия отмечается на фоне выраженной дизурии.
При мочекаменной болезни гематурия обычно развивается вслед за приступом почечной колики, струя мочи может внезапно прерываться во время мочеиспускания.
Возможные осложнения: при массивном кровотечении с образованием бесформенных сгустков возможна острая задержка мочи из-за тампонады мочевого пузыря этими сгустками. Редко в этом случае может развиться шок вследствие кровопотери и боли.
Диагностика
При опросе необходимо выяснить:
Визуальная оценка мочи:
Цвет мочи может меняться при приеме лекарственных средств и пищевых продуктов:
При синдроме длительного сдавливания и размозжения тканей миоглобин из мышц попадает в кровь и проникает в мочу, что придает ей красно-бурую окраску.
Для определения характера и источника кровотечения в условиях стационара проводят:
Лабораторная диагностика включает:
При гемоглобинурии цвет мочи не меняется даже при длительном ее стоянии, а при гематурии эритроциты оседают на дно сосуда и верхние слои мочи приобретают желтоватую окраску.
Гематурию у женщин следует дифференцировать с кровотечением из половых органов. Для этого исследуют среднюю порцию мочи при самостоятельном мочеиспускании или мочу, полученную из мочевого пузыря путем катетеризации.
Основные направления терапии
Алгоритм неотложной помощи при гематурии представлен на рисунке 3.
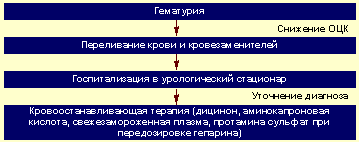 |
| Рисунок 3. Алгоритм неотложной помощи при гематурии |
При развитии гиповолемии и артериальной гипотензии восстановление ОЦК: кристаллоидные и коллоидные растворы внутривенно.
При подозрении на острый цистит после забора мочи для посева ее на стерильность назначают антибиотик широкого спектра действия.
Терапия гемостатическими препаратами должна проводиться в условиях урологического стационара, после установления диагноза, под контролем свертываемости крови.
Клиническая фармакология отдельных препаратов
Этамзилат (дицинон) активирует формирование тромбопластина, образование III фактора свертывания крови, нормализует адгезию тромбоцитов. Препарат не влияет на протромбированное время, не обладает гиперкоагуляционными свойствами, не способствует образованию тромбов. Этамзилат вводят по 2–4 мл (0,25–0,5 г) внутривенно одномоментно либо капельно, добавляя к обычным растворам для инфузий.
Гемостатическое действие развивается:
Не следует применять этамзилат при геморрагиях, вызванных антикоагулянтами.
Аминокапроновая кислота угнетает фибринолиз, блокируя активаторы плазминогена и частично угнетая действие плазмина, оказывает специфическое кровоостанавливающее действие при кровотечениях, связанных с повышением фибринолиза. Для быстрого достижения эффекта под контролем коагулограммы вводят стерильный 5% раствор препарата на физрастворе внутривенно капельно до 100 мл.
Протамина сульфат оказывает противогеморрагическое действие при кровоточивости, вызываемой гепарином при его передозировке, после операций с применением экстракорпорального кровообращения и использованием гепарина. Применяют 1 мл 1% раствора внутривенно струйно медленно за 2 мин или капельно, 1 мг протамина сульфата нейтрализует примерно 85 ЕД гепарина. Противопоказан при гипотензии, недостаточности коры надпочечников, тромбоцитопении.
Часто встречающиеся ошибки терапии: назначение гемостатических препаратов до выявления источника гематурии.
Макрогематурия является показанием для экстренной госпитализации в урологический стационар.
Разбор клинических случаев
Больная М., 30 лет. Жалобы на схваткообразные боли в поясничной области слева, усиливающиеся при движении, после физической нагрузки, примесь крови в моче, повышение температуры тела до 38,2°С. Заболевание началось с дизурии в виде учащенного, болезненного мочеиспускания, спустя сутки появились боли в поясничной области, примесь крови в моче. Анамнез: 7 лет назад был установлен диагноз — нефроптоз I степени слева. Заболевание проявляло себя периодическими атаками пиелонефрита. При осмотре: больная беспокойна. Область почек визуально не изменена, при пальпации безболезненная, симптом поколачивания слабо положительный слева, болезненности по ходу мочеточников нет, мочевой пузырь перкуторно пуст. Диагноз: острый восходящий левосторонний пиелонефрит. Нефроптоз слева. Пациентка госпитализирована в урологический стационар.
Больной Ж., 77 лет. Вызов СМП в связи с интенсивной примесью крови в моче, выделением кровяных сгустков при мочеиспускании. Анамнез: урологические заболевания отсутствуют. При осмотре: больной астеничен, кожные покровы бледные. Область почек визуально не изменена, при бимануальной пальпации правой почки определяется объемное образование нижнего сегмента, симптом поколачивания отрицательный с обеих сторон. При пальцевом ректальном исследовании — простата увеличена в 1,5–2 раза, тугоэластической консистенции, срединная бороздка сглажена, слизистая прямой кишки над железой подвижна, пальпация безболезненна. Диагноз: опухоль правой почки. Больной госпитализирован в урологическое отделение.
Больной Ч., 24 года. Жалобы на постоянное выделение крови по мочеиспускательному каналу. Анамнез: около часа назад упал и ударился промежностью о трубу. При осмотре: кровоподтек в области промежности, выделение алой неизмененной крови из уретры, вне акта мочеиспускания. При пальцевом ректальном исследовании — предстательная железа нормальных размеров, тугоэластической консистенции, срединная бороздка выражена, слизистая прямой кишки над железой подвижна, пальпация безболезненна. Диагноз: травма уретры. Больному показана госпитализация в стационар для обследования и определения тактики лечения.
Таким образом, успех лечения больных пиелонефритом и гематурией во многом определяется принятием адекватных мер при оказании неотложной медицинской помощи.
Е. Б. Мазо, доктор медицинских наук, профессор, член-корреспондент РАМН
РГМУ, Москва
Антибиотики в лечении и профилактике инфекций мочевыводящих путей у детей
Инфекция мочевыводящих путей (ИМП) — рост микроорганизмов в различных отделах почек и мочевыводящих путей (МП), способный вызвать воспалительный процесс, по локализации соответствующий заболеванию (пиелонефриту, циститу, уретриту и т. д.). ИМП детей
Инфекция мочевыводящих путей (ИМП) — рост микроорганизмов в различных отделах почек и мочевыводящих путей (МП), способный вызвать воспалительный процесс, по локализации соответствующий заболеванию (пиелонефриту, циститу, уретриту и т. д.).
ИМП детей встречается в России с частотой около 1000 случаев на 100 000 населения. Довольно часто ИМП имеют тенденцию к хроническому, рецидивирующему течению. Это объясняется особенностью строения, кровообращения, иннервации МП и возрастной дисфункцией иммунной системы растущего организма ребенка. В связи с этим принято выделять ряд факторов, способствующих развитию ИМП:
В детском возрасте ИМП в 80% случаев развиваются на фоне врожденных аномалий верхних и нижних МП, при которых имеются нарушения уродинамики. В таких случаях говорят об осложненной ИМП. При неосложненной форме анатомических нарушений и расстройств уродинамики не определяется.
Среди наиболее часто встречающихся пороков развития мочевого тракта пузырно-мочеточниковый рефлюкс встречается в 30–40% случаев. Второе место занимает мегауретер, нейрогенная дисфункция мочевого пузыря. При гидронефрозе инфицирование почки происходит реже.
Диагностика ИМП строится на многих принципах. Необходимо помнить, что симптоматика ИМП зависит от возраста ребенка. Например, у новорожденных детей отсутствуют специфические симптомы ИМП и инфекция редко генерализуется.
Для детей младшего возраста характерны такие симптомы, как вялость, беспокойство, периодические подъемы температуры, анорексия, рвота и желтуха.
Для детей старшего возраста характерны лихорадка, боли в спине, животе и дизурические явления.
Перечень вопросов при сборе анамнеза включает следующие пункты:
Врач всегда должен стремиться более точно установить локализацию возможного очага инфекции: от этого зависит вид лечения и прогноз заболевания. Для уточнения топики поражения мочевого тракта необходимо хорошо знать клиническую симптоматику инфекций нижних и верхних мочевых путей. При инфекции верхних мочевыводящих путей значимым является пиелонефрит, который составляет до 60% всех случаев госпитализации детей в стационар (таблица).
Однако основу диагностики ИМП составляют данные анализов мочи, в которых главное значение имеют микробиологические методы. Выделение микроорганизма в посеве мочи служит основанием для постановки диагноза. Существует несколько способов забора мочи:
Распространенным непрямым методом оценки бактериурии является анализ на нитриты (нитраты, в норме имеющиеся в моче, при наличии бактерий преобразуются в нитриты). Диагностическая ценность данного метода достигает 99%, но у маленьких детей в связи с коротким пребыванием мочи в мочевом пузыре значительно снижена и достигает 30–50%. Необходимо помнить, что у маленьких мальчиков может быть ложноположительный результат из-за аккумуляции нитритов в препуциальном мешке.
В большинстве случаев ИМП вызывается одним видом микроорганизма. Определение в образцах нескольких видов бактерий чаще всего объясняется нарушениями техники сбора и транспортировки материала.
При хроническом течении ИМП в некоторых случаях возможно выявление микробных ассоциаций.
К другим методам исследования мочи относятся сбор общего анализа мочи, проба Нечипоренко и Аддиса–Каковского. Лейкоцитурия наблюдается во всех случаях ИМП, однако необходимо помнить, что она может быть, например, и при вульвите. Макрогематурия встречается у 20–25% детей с циститом. При наличии симптомов инфекции протеинурия подтверждает диагноз пиелонефрита.
Инструментальные обследования проводятся детям в период ремиссии процесса. Целью их является уточнение локализации инфекции, причины и степени повреждения почек. Обследование детей с ИМП на сегодняшний день включает:
Проведение инструментального и рентгенологического обследования должно выполняться по следующим показаниям:
Бактериальная этиология ИМС при урологических заболеваниях имеет отличительные особенности в зависимости от остроты процесса, частоты осложненных форм, возраста пациента и состояния его иммунного статуса, условий возникновения инфекции (амбулаторно или в стационаре).
Результаты исследований (данные НЦЗД РАМН, 2005) показывают, что у амбулаторных больных с ИМП в 50% случаев выделяются E. coli, в 10% — Proteus spp., в 13% — Klebsiella spp., в 3% — Enterobacter spp., в 2% — Morganella morg. и с частотой 11% — Enterococcus fac. (рисунок). Другие микроорганизмы, составившие 7% выделения и встречавшиеся с частотой менее 1%, были следующими: S. epidermidis — 0,8%, S. pneumoniae — 0,6%, Acinetobacter spp. — 0,6%, Citrobacter spp. — 0,3%, S. pyogenes — 0,3%, Serratia spp. — 0,3%.
В структуре внутрибольничных инфекций ИМП занимают второе место, после инфекций дыхательных путей. Следует отметить, что у 5% детей, находящихся в урологическом стационаре, развиваются инфекционные осложнения, обусловленные хирургическим или диагностическим вмешательством.
У стационарных больных этиологическая значимость кишечной палочки значительно снижается (до 29%) за счет увеличения и/или присоединения таких «проблемных» возбудителей, как Pseudomonas aeruginosa (29%), Enterococcus faec. (4%), коагулазонегативные стафилококки (2,6%), неферментирующие грамотрицательные бактерии (Acinetobacter spp. — 1,6%, Stenotrophomonas maltophilia — 1,2%) и др. Чувствительность этих возбудителей к антибактериальным препаратам часто непредсказуема, так как зависит от ряда факторов, в том числе и от особенностей циркулирующих в данном стационаре внутрибольничных штаммов.
Не вызывает сомнений, что основными задачами в лечении больных с ИМП являются ликвидация или уменьшение воспалительного процесса в почечной ткани и МП, при этом успех лечения во многом определяется рациональной антимикробной терапией.
Естественно, при выборе препарата уролог руководствуется прежде всего сведениями о возбудителе инфекции и о спектре антимикробного действия препарата. Антибиотик может быть безопасным, способным создавать высокие концентрации в паренхиме почек и моче, но если в его спектре нет активности против конкретного возбудителя, назначение такого препарата бессмысленно.
Глобальной проблемой в назначении антибактериальных препаратов является рост резистентности микроорганизмов к ним. Причем наиболее часто резистентность развивается у внебольничных и нозокомиальных больных. Те микроорганизмы, которые не входят в антибактериальный спектр какого-либо антибиотика, естественно, считаются резистентными. Приобретенная же резистентность означает, что изначально чувствительный к определенному антибиотику микроорганизм становится устойчивым к его действию.
На практике часто заблуждаются в отношении приобретенной резистентности, считая, что ее возникновение неизбежно. Но наука располагает фактами, опровергающими такое мнение. Клиническое значение этих фактов состоит в том, что антибиотики, которые не вызывают резистентности, можно использовать, не опасаясь ее последующего развития. Но если же развитие резистентности потенциально возможно, то и появляется она достаточно быстро. Другое заблуждение заключается в том, что развитие резистентности связывают с использованием антибиотиков в больших объемах. Примеры с наиболее часто назначаемым в мире антибиотиком цефтриаксоном, а также с цефокситином и цефуроксимом поддерживают концепцию о том, что использование антибиотиков с низким потенциалом развития резистентности в любых объемах не приведет к ее росту в последующем.
Многие считают, что для одних классов антибиотиков возникновение антибиотикорезистентности характерно (это мнение относится к цефалоспоринам III поколения), а для других — нет. Однако развитие резистентности связано не с классом антибиотика, а с конкретным препаратом.
Если антибиотик обладает потенциалом развития резистентности, признаки резистентности к нему появляются уже в течение первых 2 лет применения или даже на этапе клинических испытаний. Исходя из этого, мы можем с уверенностью прогнозировать проблемы резистентности: среди аминогликозидов — это гентамицин, среди цефалоспоринов II поколения — цефамандол, III поколения — цефтазидим, среди фторхинолонов — тровофлоксацин, среди карбапенемов — имипенем. Внедрение в практику имипенема сопровождалось быстрым развитием резистентности к нему штаммов P. aeruginosa, этот процесс продолжается и сейчас (появление меропенема не было сопряжено с такой проблемой, и можно утверждать, что она не возникнет и в ближайшем будущем). Среди гликопептидов — это ванкомицин.
Как уже указывалось, у 5% больных, находящихся в стационаре, развиваются инфекционные осложнения. Отсюда и тяжесть состояния, и увеличение сроков выздоровления, пребывания на койке, повышение стоимости лечения. В структуре внутрибольничных инфекций ИМП занимают первое место, на втором месте — хирургические (раневые инфекции кожи и мягких тканей, абдоминальные).
Сложности лечения госпитальных инфекций обусловлены тяжестью состояния больного. Часто имеет место ассоциация возбудителей (два и более, при раневой или катетер-ассоциированной инфекции). Также большое значение имеет возросшая в последние годы резистентность микроорганизмов к традиционным антибактериальным препаратам (к пенициллинам, цефалоспоринам, аминогликозидам), применяемым при инфекции мочеполовой системы.
На сегодняшний день чувствительность госпитальных штаммов Enterobacter spp. к Амоксиклаву (амоксициллин + клавулановая кислота) составляет 40%, к цефуроксиму — 30%, к гентамицину — 50%, чувствительность S. aureus к оксациллину составляет 67%, к линкомицину — 56%, к ципрофлоксацину — 50%, к гентамицину — 50%. Чувствительность штаммов P. aeruginosa к цефтазидиму в разных отделениях не превышает 80%, к гентамицину — 50%.
Существуют два потенциальных подхода к преодолению резистентности к антибиотикам. Первый заключается в профилактике резистентности, например путем ограничения применения антибиотиков, обладающих высоким потенциалом ее развития; столь же важными являются эффективные программы эпидемиологического контроля для предотвращения распространения в лечебном учреждении госпитальных инфекций, вызываемых высокорезистентными микроорганизмами (стационарный мониторинг). Второй подход — устранение или коррекция уже имеющихся проблем. Например, если в отделении интенсивной терапии (или в стационаре вообще) распространены резистентные штаммы P. aeruginosa или Enterobacter spp., то полная замена в формулярах антибиотиков с высоким потенциалом развития резистентности на антибиотики-«чистильщики» (амикацин вместо гентамицина, меропенем вместо имипенема и т.п.) позволит устранить или минимизировать антибиотикорезистентность грамотрицательных аэробных микроорганизмов.
В лечении ИМП на сегодняшний день используются: ингибиторозащищенные пенициллины, цефалоспорины, аминогликозиды, карбапенемы, фторхинолоны (ограничены в педиатрии), уроантисептики (производные нитрофурана — Фурагин).
Остановимся на антибактериальных препаратах в лечении ИМП подробнее.
Рекомендуемые препараты при инфекции нижних мочевых путей.
При инфекции верхних мочевых путей.
При госпитальной инфекции.
Для периоперационной антибактериальной профилактики.
Для антибактериальной профилактики при инвазивных манипуляциях: ингибиторозащищенные аминопенициллины — амоксициллин + клавулановая кислота.
Принято считать, что антибактериальная терапия амбулаторных больных с ИМП может проводиться эмпирически, основываясь на данных антибиотикочувствительности основных уропатогенов, циркулирующих в конкретном регионе в данный период наблюдения, и клиническом статусе пациента.
Стратегическим принципом антибиотикотерапии в амбулаторных условиях является принцип минимальной достаточности. Препаратами первого ряда служат:
Ошибочным является использование в амбулаторных условиях ампициллина и ко-тримоксазола, в связи с возросшей резистентностью к ним E. coli. Неоправданно назначение цефалоспоринов I поколения (цефалексин, цефрадин, цефазолин). Производные нитрофуранового ряда (Фурагин) не создают терапевтических концентраций в почечной паренхиме, поэтому их назначают только при цистите. В целях снижения роста резистентности микроорганизмов следует резко ограничить применение цефалоспоринов III поколения и полностью исключить назначение аминогликозидов в амбулаторной практике.
Анализ резистентности штаммов возбудителей осложненных уроинфекций показывает, что активность препаратов группы полусинтетических пенициллинов и защищенных пенициллинов может быть достаточно высокой в отношении кишечной палочки и протеев, однако в отношении энтеробактерий и синегнойной палочки их активность составляет до 42 и 39% соответственно. Поэтому препараты этой группы не могут быть препаратами эмпирической терапии тяжелых гнойно-воспалительных процессов органов мочевыделения.
Активность цефалоспоринов I и II поколений в отношении энтеробактера и протеев также оказывается очень низкой и колеблется в пределах 15–24%, в отношении кишечной палочки — несколько выше, однако не превышает активности полусинтетических пенициллинов.
Активность цефалоспоринов III и IV поколений существенно выше, чем у пенициллинов и цефалоспоринов I и II поколений. Наиболее высокая активность отмечена в отношении кишечной палочки — от 67 (цефоперазон) до 91% (цефепим). В отношении энтеробактера активность составляет от 51 (цефтриаксон) до 70% (цефепим), также высокая активность препаратов этой группы отмечается в отношении протеев (65–69%). В отношении синегнойной палочки активность этой группы препаратов низкая (15% у цефтриаксона, 62% у цефепима). Спектр антибактериальной активности цефтазидима наиболее высокий в отношении всех актуальных грамотрицательных возбудителей осложненных инфекций (от 80 до 99%). Высокой сохраняется активность карбапенемов — от 84 до 100% (у имипенема).
Активность аминогликозидов несколько ниже, особенно в отношении энтерококков, но в отношении энтеробактерий и протея высокая активность сохраняется у амикацина.
По этой причине антибактериальная терапия ИМП у урологических больных в стационаре должна основываться на данных микробиологической диагностики возбудителя инфекции у каждого больного и его чувствительности к антибактериальным препаратам. Начальная эмпирическая антимикробная терапия урологических больных может назначаться только до получения результатов бактериологического исследования, после которого она должна быть изменена согласно антибиотикочувствительности выделенного микроорганизма.
В применении антибиотикотерапии в стационаре следует придерживаться другого принципа — от простого к мощному (минимум использования, максимум интенсивности). Спектр используемых групп антибактериальных препаратов здесь значительно расширен:
Важной в работе детского уролога является периоперационная антибиотикопрофилактика (пре-, интра- и постоперационная). Конечно, не следует пренебрегать влиянием других факторов, снижающих вероятность развития инфекции (сокращение сроков пребывания в стационаре, качество обработки инструментария, катетеров, использование закрытых систем для отведения мочи, обучение персонала).
Основные исследования показывают, что послеоперационные осложнения предотвращаются в том случае, если высокая концентрация антибактериального препарата в сыворотке крови (и в тканях) создана к началу оперативного вмешательства. В клинической практике оптимальное время для антибиотикопрофилактики — 30–60 мин до начала операции (при условии внутривенного введения антибиотика), т. е. в начале анестезиологических мероприятий. Отмечен значительный рост частоты возникновения послеоперационных инфекций, если профилактическая доза антибиотика была назначена не в пределах 1 ч до проведения операции. Любой антибактериальный препарат, введенный после закрытия операционной раны, не повлияет на вероятность развития осложнений.
Таким образом, однократное введение адекватного антибактериального препарата в целях профилактики не менее эффективно, чем многократное. Только при длительном оперативном вмешательстве (более 3 ч) требуется дополнительная доза. Антибиотикопрофилактика не может продолжаться более 24 ч, так как в этом случае применение антибиотика рассматривается уже как терапия, а не как профилактика.
Идеальный антибиотик, в том числе и для периоперационной профилактики, должен быть высокоэффективен, хорошо переноситься больными, обладать невысокой токсичностью. Его антибактериальный спектр должен включать вероятную микрофлору. Для пациентов, длительно находящихся в стационаре до проведения оперативного вмешательства, необходимо принимать во внимание спектр нозокомиальных микроорганизмов с учетом их антибиотикочувствительности.
Для антибиотикопрофилактики при урологических операциях желательно использовать препараты, создающие высокую концентрацию в моче. Многие антибиотики отвечают этим требованиям и могут использоваться, например цефалоспорины II поколения и ингибиторозащищенные пенициллины. Аминогликозиды должны быть зарезервированы для пациентов, входящих в группы риска или с аллергией на b-лактамы. Цефалоспорины III и IV поколений, ингибиторозащищенные аминопенициллины и карбапенемы должны использоваться в единичных случаях, когда место операции обсеменено мультирезистентными нозокомиальными микроорганизмами. Все-таки желательно, чтобы назначение этих препаратов было ограничено лечением инфекций с тяжелым клиническим течением.
Существуют общие принципы антибактериальной терапии ИМП у детей, которые включают в себя следующие правила.
При фебрильном течении ИМП начинать терапию следует с парентерального антибиотика широкого спектра (ингибиторозащищенные пенициллины, цефалоспорины II, III поколений, аминогликозиды).
Необходимо учитывать чувствительность микрофлоры мочи.
Длительность лечения пиелонефрита составляет 14 дней, цистита — 7 дней.
У детей с пузырно-мочеточниковым рефлюксом антимикробная профилактика должна быть длительной.
При бессимптомной бактериурии антибактериальная терапия не показана.
В понятие «рациональная антибиотикотерапия» должен входить не только правильный выбор препарата, но и выбор его введения. Необходимо стремиться к щадящим и в то же время наиболее эффективным методам назначения антибактериальных препаратов. При использовании ступенчатой терапии, которая заключается в смене парентерального использования антибиотика на пероральный, после нормализации температуры, врач должен помнить о следующем.
Ниже представлены антибактериальные препараты в зависимости от пути их введения.
Препараты для перорального лечения ИМП.
• II поколения: цефуроксим;
• III поколения: цефиксим, цефтибутен, цефподоксим.
Препараты для парентерального лечения ИМП.
• II поколения: цефуроксим (Цефурабол).
• III поколения: цефотаксим, цефтриаксон, цефтазидим.
• IV поколения: цефепим (Максипим).
Несмотря на наличие современных антибиотиков и химиотерапевтических препаратов, позволяющих быстро и эффективно справляться с инфекцией и уменьшать частоту рецидивов путем назначения на длительный период препаратов в низких профилактических дозах, лечение рецидивов ИМП все еще представляет собой довольно сложную задачу. Это обусловлено:
Как известно, до 30% девочек имеют рецидив ИМП в течение 1 года, 50% — в течение 5 лет. У мальчиков до 1 года рецидивы встречаются в 15–20%, старше 1 года — рецидивов меньше.
Перечислим показания к антибиотикопрофилактике.
а) пузырно-мочеточниковый рефлюкс;
Длительность антибиотикопрофилактики чаще всего определяется индивидуально. Отмена препарата осуществляется при отсутствии обострений за время профилактики, но при возникновении обострения после отмены требуется назначение нового курса.
В последнее время на отечественном рынке появился новый препарат для профилактики рецидивов ИМП. Этот препарат представляет собой лиофилизированный белковый экстракт, полученный путем фракционирования щелочного гидролизата некоторых штаммов E. coli и носит название Уро-Ваксом. Проведенные испытания подтвердили его высокую эффективность с отсутствием выраженных побочных явлений, что возлагает надежду на его широкое использование.
Важное место в лечении больных с ИМП занимает диспансерное наблюдение, которое заключается в следующем.
Литература
С. Н. Зоркин, доктор медицинских наук, профессор
НЦЗД РАМН, Москва



