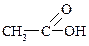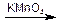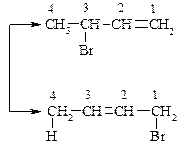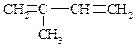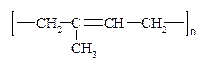Ациклические углеводороды



УГЛЕВОДОРОДЫ
Угеводороды – простейшие органические соединения, молекулы которых построены только из атомов углерода и водорода.
Алканы (парафины, предельные или насыщенные углеводороды) CnH2n+2 – это углеводороды, у которых атомы углерода связаны между собой простой (одинарной) связью.
Каждый последующий член гомологического ряда отличается от предыдущего на гомологическую разность (СН2).
Молекула алкана, потеряв водород, превращается в радикал: • СН3 – метил, • С3Н7 – пропил и т. д.; отсюда даются соответствующие названия соединениям: СН3–СН2–NH2 – этиламин; CH3I –йодистый метил; СН3–О–СН3 – диметиловый эфир и пр.
Химические свойства алканов определяются высокой прочностью ковалентных связей (σ-связей), поэтому химическая активность предельных углеводородов мала. Алканы могут вступать в реакции только в жёстких условиях: при повышенной температуре, облучении, действии активных реагентов, использовании катализаторов. Для предельных углеводородов характерны следующие типы реакций:
а) Реакции замещения, когда атомы водорода замещаются на другие атомы или группы атомов. Типичной реакцией, протекающей по радикальному механизму замещения, является реакция галогенирования, идущая при облучении светом:
СН4 + Cl2 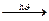
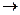
б) Реакция термического расщепления С–С – связей (крекинг). Обычно идет с образованием алканов и алкенов через свободные радикалы:
СН3–СН2–СН2–СН2–CН2–СН3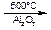
+ СН2=СН2.
в) Реакция окисления. Может происходить в жестких условиях, т.е. при горении: 2СН3–СН3 + 7О2 
СН3–(СН2)16–СН3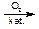
октадекан стеариновая кислота
Предельные углеводороды используются для синтеза этилена, пропилена, ацетилена, бензола, толуола, ксилолов, нафталина и т.д. Путём крекинга нефти, а затем ректификации полученных продуктов по фракциям вырабатывают такие нефтепродукты, как моторное топливо, растворители, смазочные масла, вазелин, гудрон и др. Алканы входят в состав природных газов, обычно это смеси метана (основное количество), этана (от 2–5%), пропана и других более тяжёлых углеводородов.
Некоторые примеры использования метана:
СН4 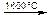
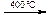 |
СН4 + О2 100 атм. СН3ОН метиловый спирт;
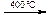
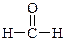
СН4 + Сl2 
Алкены (олефины, непредельные, этиленовые углеводороды) –это углеводороды, в структуре углеродного скелета которых имеется двойная (σ и π) связь. Их молекулярная формула СnН2n.
По физическим свойствамалкены мало отличаются от алканов. Низшие гомологи С2 – С4 – газы; С5 – С17 – жидкости; высшие гомологи – твёрдые вещества. В воде алкены нерастворимы, хорошо растворимы в органических растворителях.
СН2=СН2 этен (этилен), его радикал СН2=СН • – винил;
Для алкенов характерна изомерия:
а) структурная (изомерия углеродного скелета, изомерия положения двойной связи);
б) пространственная (цис-, трансизомерия).
Химические свойстваопределяются наличием двойной связи в этиленовых углеводородах – это реакции электрофильного присоединения, окисления и полимеризации, сопровождающиеся разрывом π-связи.
Примеры реакций присоединения:
а) Реакция гидробромирования:
СН3–СН=СН2 + НВr 
Реакции с галогеноводородами идут по правилу Марковникова, т.е. водород присоединяется к более гидрированному атому углерода в несимметричных алкенах.
б) Реакция гидрирования:
СН2=СН2 + Н2 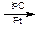
в) Реакция галогенирования:
СН2=СН2 + Вr2 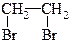
г) Реакция гидратации:
присоединение по правилу Марковникова

СН2=СН–СН3 + НОН 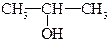
д) Реакции окисления:
полное окисление (горение)
С2Н4 + 3О2 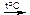
окисление в мягких условиях
СН2=СН2 + [О] + НОН 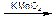
Это качественная реакция на двойную связь.
е) Реакции полимеризации:
nCH2=CH2 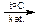
nCH2=CH–CH3 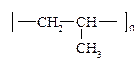
Алкины (ацетиленовые углеводороды) СnH2n-2 – это ненасыщенные углеводороды, которые имеют одну тройную связь.
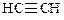
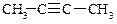
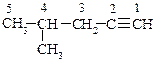
Структурная изомерия алкинов, как и алкенов, обусловлена строением углеродной цепи и положением в ней тройной связи.
Физические свойства.Ацетилен, метил- и этилацетилены – газы; следующие гомологи ацетилена (от С5 до С15) – жидкости; высшие ацетиленовые углеводороды (от С15Н28) – твердые вещества.
Химические свойстваалкинов определяются наличием тройной связи.
1. Реакции присоединения:
а) Гидрирование (гидрогенизация):
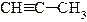
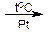
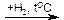
пропин пропен пропан
б) Присоединение галогеноводородных кислот согласно правилу Марковникова:
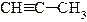

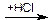
пропин 2-хлорпропен 2,2-дихлорпропан
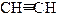

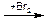
г) Гидратация (реакция Кучерова):
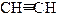
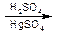

уксусный альдегид уксусная кислота
2. Реакции окисления:
а) СН≡СН + 5О2
б) СН≡СН+2[О]+2НОН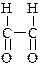
3. Образование ацетиленидов по реакции замещения:
СН≡СН + 2[Cu(NH3)2]ОН
а) циклическая ЗНС≡СН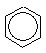
б) линейная 2СН≡СН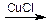
Ацетиленовые углеводороды используются для получения поливинилацетата, акрилацетата (для синтеза каучуков, пластмасс), бензола и его производных.
Алкадиены СnН2n-2 – это углеводороды, содержащие две двойные связи. Для них характерна структурная изомерия и цис-, трансизомерия.
По физическим свойствамдиеновые углеводороды могут быть газами и твердыми веществами.
Промышленное значение имеют диены с сопряжёнными двойными связями (дивинил, изопрен).
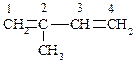
Химические свойстваалкадиенов определяются особенностями строения молекул этих углеводородов.
1. Реакция гидрирования:
СН2=СН–СН=СН2 + Н2 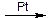
2. Реакция гидробромирования:
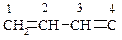

3. Реакция полимеризации:
n
Для получения синтетических каучуков с необходимыми свойствами используется процесс совместной полимеризации бутадиена-1,3 с другими непредельными соединениями, например с винилхлоридом СН2=СНСl, стиролом СН2=СНС6Н5, акрилонитрилом СН2=CHCN. Так, бутадиен – стирольный каучук износостоек и идёт на изготовление автошин и подошв к обуви.
Углеводороды, виды и их классификация
Углеводороды, виды и их классификация.
Углеводороды – это органические соединения, состоящие из атомов углерода и водорода. Они служат фундаментальной основой органической химии
Углеводороды:
Углеводороды – это органические соединения, состоящие из атомов углерода и водорода. Углеводороды служат фундаментальной основой органической химии – молекулы любых других органических соединений рассматривают как их производные.
Если в углеводороде один или несколько атомов водорода замещён на другой атом или группу атомов, называемую функциональной группой, то данное соединение называется производным углеводорода.
Атом углерода имеет 4 электрона на внешней оболочке, а потому способен образовывать четыре химические связи с другими атомами. Поэтому атом углерода является стабильным только в том случае, если все из этих связей – все четыре связи используются.
Существует огромное количество совершенно различных соединений углеводородов, которые различаются количеством атомов углерода и водорода, строением углеродного скелета и типом связей между атомами.
Большинство углеводородов в природе Земли встречаются в сырой нефти. Кроме того, основными источниками углеводородов являются природный газ, сланцевый газ, попутный нефтяной газ, горючие сланцы, уголь, торф.
Классификация и виды углеводородов:
При систематизации (классификации) углеводородов принимают во внимание строение углеродного скелета и тип связей, соединяющих атомы углерода.
В зависимости от строения углеродного скелета углеводороды подразделяют на ациклические и карбоциклические.
Ациклические соединения (ациклические углеводороды) – класс органических соединений, в молекулах которых отсутствуют циклы (кольца), и все атомы углерода соединены между собой в прямые или разветвлённые (открытые) цепи.
Ациклические соединения также в литературе называются алифатическими соединениями.
Карбоциклические соединения (карбоциклические углеводороды) – класс органических соединений, характеризующихся наличием колец (циклов) из атомов углерода. Карбоциклические соединения отличаются от гетероциклических соединений отсутствием в кольцах каких-либо других атомов, помимо атомов углерода.
В зависимости от кратности углерод-углеродных связей ациклические углеводороды подразделяют на предельные (алканы) и непредельные (алкены, алкины, диены) углеводороды. Предельные ациклические углеводороды также называются насыщенными, а непредельные – ненасыщенными.
В свою очередь циклические углеводороды в зависимости от кратности углерод-углеродных связей подразделяются на алициклические (циклоалканы, циклоалкены, циклоалкины) и ароматические (арены) углеводороды.
Предельные (насыщенные) ациклические углеводороды:
Насыщенными алканы называются потому, что они содержат максимально возможное число атомов водорода для заданного числа атомов углерода.
Непредельные (ненасыщенные) ациклические углеводороды:
Атомы углерода при двойной связи находятся в состоянии sp² гибридизации и имеют валентный угол 120°. Связи C=C представляют собой π-связи. Длина связи C=C составляет 0,134 нм.
По номенклатуре IUPAC названия алкенов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ен»; положение двойной связи указывается арабской цифрой.
Алкены образуют гомологический ряд, также называемый рядом этилена. К алкенам относятся: этен (этилен) C2H4, пропен (пропилен) C3H6, бутен (бутилен) C4H8, пентен C5H10, гексен C6H12, гептен C7H14, октен C8H16, нонен C9H18, децен C10H20 и т.д., которые имеют формулу CnH2n.
Алкены, число атомов углерода в которых больше двух (т.е. кроме этилена), имеют изомеры. Для алкенов характерны изомерия углеродного скелета, положения двойной связи, межклассовая и геометрическая (пространственная). С ростом числа атомов углерода в молекуле количество изомеров быстро возрастает.
Алкины (также именуемые ацетиленовые углеводороды) – ациклические непредельные углеводороды, содержащие тройную связь между атомами углерода, образующие гомологический ряд с общей формулой CnH2n-2.
Атомы углерода при тройной связи находятся в состоянии sp-гибридизации и имеют валентный плоский угол 180°. Таким образом у алкинов связь С≡С линейна (угол 180°) и находится в одной плоскости. Связи C≡C образованы одной σ-связью и двумя π-связями. Длина связи C≡C составляет 0,121 нм.
По номенклатуре IUPAC названия алкинов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ин»; положение тройной связи указывается арабскими цифрами.
Алкины образуют гомологический ряд, также называемый рядом ацетилена. К алкинам относятся: этин (ацетилен) C2H2, пропин C3H4, бутин C4H6, пентин C5H8, гексин C6H10, гептин C7H12, октин C8H14, нонин C9H16, децин C10H18 и т.д., которые имеют формулу CnH2n-2.
Алкины, число атомов углерода в которых больше трех (т.е. кроме ацетилена и пропина), имеют изомеры. Для алкинов характерны изомерия углеродного скелета, положения тройной связи и межклассовая. С ростом числа атомов углерода в молекуле количество изомеров быстро возрастает.
Диены (именуемые также алкадиены) – ациклические непредельные углеводороды, содержащие две двойных связи между атомами углерода, образующие гомологический ряд с общей формулой CnH2n-2.
В зависимости от взаимного расположения кратных связей, диены подразделяются на три группы:
– сопряжённые диены, в которых двойные связи разделены одинарной (1,3-диены)
– аллены с кумулированными двойными связями (1,2-диены)
– диены с изолированными двойными связями, в которых двойные связи разделены несколькими одинарными.
По номенклатуре IUPAC названия диенов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-диен»; положение двух двойных связей указывается двумя арабскими цифрами.
Атомы углерода при двойной связи находятся в состоянии sp² гибридизации. Связи C=C представляют собой π-связи. В сопряженных диенах длина связи C=C составляет 0,137 нм, а C-C – 0,146 нм.
Диены образуют гомологический ряд. К диенам относятся: пропадиен (С3Н4), бутадиен (С4Н6), пентадиен (С5Н8), гексадиен (С6Н10), гептадиен (С7Н12), октадиен (С8Н14), нонадиен (С9Н16), декадиен (С10Н18) и т.д., которые имеют формулу CnH2n-2.
Диены, число атомов углерода в которых больше четырех (т.е. кроме пропадиена и бутадиена), имеют изомеры. Для диенов характерны изомерия углеродного скелета, положения двойной связи, межклассовая и геометрическая (пространственная, цис-транс-изомерия). С ростом числа атомов углерода в молекуле количество изомеров быстро возрастает.
Алициклические углеводороды:
Алициклические углеводороды – циклические углеводороды, молекулы которых содержат замкнутые кольца из атомов углерода (но не имеющие ароматического кольца), которые являются частично или полностью насыщенными. Алициклические соединения классифицируют по числу атомов в кольце, по числу колец, по наличию или отсутствию кратных связей.
К алициклическим углеводородам относятся циклоалканы, циклоалкены, циклоалкины.
Алициклические углеводороды имеют изомеры. Для них характерны изомерия углеродного скелета (кольца и боковых цепей), положения заместителей в цепи, положения двойной или тройной связи, межклассовая и геометрическая (пространственная, оптическая, цис-транс-изомерия, конформационная). С ростом числа атомов углерода в молекуле количество изомеров быстро возрастает.
Циклоалканы (именуемые также полиметиленовые углеводороды, нафтены, цикланы, циклопарафины) – насыщенные алициклические углеводороды, имеющие циклическое строение (т.е. имеющие замкнутое кольцо атомов углерода), содержащие только простые (одиночные) связи между атомами углерода и образующие гомологический ряд с общей формулой CnH2n (n⩾3).
По номенклатуре IUPAC названия циклоалканов образуются от названий соответствующих алканов добавлением приставки «цикло-».
Атомы углерода при С-С связи находятся в состоянии sp 3 гибридизации.
Циклоалканы образуют гомологический ряд. К циклоалканам относятся: циклопропан C3H6, циклобутан C4H8, циклопентан C5H10, циклогексан C6H12, циклогептан C7H14, циклооктан C8H16, циклононан C9H18, циклодекан C10H20 и т.д., которые имеют формулу CnH2n.
Циклоалкены (также именуемые циклоолефины) – ненасыщенные алициклические углеводороды, имеющие циклическое строение (т.е. имеющие замкнутое кольцо атомов углерода), содержащие одну двойную связь между атомами углерода и образующие гомологический ряд с общей формулой CnH2n-2 (n⩾3).
По номенклатуре IUPAC названия циклоалкенов образуются от названий соответствующих алкенов добавлением приставки «цикло-».
Циклоалкены образуют гомологический ряд. К циклоалкенам относятся: циклопропен C3H4, циклобутен C4H6, циклопентен C5H8, циклогексен C6H10, циклогептен C7H12 и т.д., которые имеют формулу CnH2n-2.
Циклоалкины – ненасыщенные алициклические углеводороды, имеющие циклическое строение (т.е. имеющие замкнутое кольцо атомов углерода), содержащие одну тройную связь между атомами углерода и образующие гомологический ряд с общей формулой CnH2n-4 (n⩾5).
По номенклатуре IUPAC названия циклоалкинов образуются от названий соответствующих алкинов добавлением приставки «цикло-».
Циклоалкины образуют гомологический ряд. К циклоалкинам относятся: циклопентин C5H6, циклогексин C6H8, циклогептин C7H10 и т.д., которые имеют формулу CnH2n-4.
Ароматические углеводороды:
Ароматические углеводороды (арены) – циклические углеводороды, которые имеют в своём составе ароматическую систему.
Ароматическая система – это электронная система молекулы, содержащая (в кольце), в соответствии с правилом Хюккеля, 4n+2 электронов (где n = 0, 1, 2, …).
Различают бензоидные (арены и структурные производные аренов, которые содержат бензольные ядра) и небензоидные (все остальные) ароматические углеводороды.
Состав аренов с одним бензольным кольцом отвечает общей формуле CnH2n-6 (n⩾6).
Атомы углерода в бензольном кольце находятся в состоянии sp 2 гибридизации и имеют валентный угол 120°. Каждый атом углерода образует 3 σ-связи. Бензольное кольцо имеет плоскую форму и образуют шестигранник. У каждого атома есть негибридная р-обиталь, на которой находится неспаренный электрон. Эта орбиталь перпендикулярна плоскости и поэтому все 6 π-электронов образует единую π-электронную систему. Длина связи между атомами углерода в бензольном кольце составляет 0,139 нм.
Ароматические углеводороды имеют множество изомеров.