Что значит ki67 в онкологии
ИГХ, иммуногистохимическое исследование ткани, исследование образца опухолевой ткани, исследование ткани опухоли.
Какой биоматериал можно использовать для исследования?
Локализация б/м: образец ткани (биоптат) опухолевого образования любой локализации.
Общая информация об исследовании
Антиген Ki-67 представляет собой специфический белок, находящийся в ядерном материале опухолевой клетки, и является необходимым для осуществления ее пролиферации, т.е. деления. Обнаружение Ki-67 указывает на опухолевые клетки, которые находятся в фазе деления клеточного цикла. Это позволяет понять, насколько активно и быстро происходит деление опухолевых клеток, а следовательно, и скорость роста новообразования, оценить риск метастазирования, определиться с тактикой терапии и вероятным ответом на нее, прогнозом заболевания.
Считается, что выявление маркера Ki-67 наиболее показательно при раке молочной железы, однако ряд исследований доказывает целесообразность проведения анализа при раке любой локализации, при подозрении на злокачественный процесс, а также при наличии доброкачественных новообразований с оценкой риска их озлокачествления.
Совместное гистологическое и иммуногистохимическое исследование опухолевого материала позволяет сначала получить морфологическое описание процесса, а затем определить его пролиферативную активность – степень и скорость деления клеток. Это дает достаточно точную и объективную оценку степени злокачественности опухоли и прогноз ее дальнейшего развития.
Гистологическое исследование проводится путем изучения срезов опухолевого материала под микроскопом после предварительного окрашивания, которое позволяет выявить и описать отклонения от нормы в структуре ткани, дать характеристику изменениям и сделать вывод о доброкачественности или злокачественности процесса. Далее проводится иммуногистохимическое исследование (ИГХ), направленное на выявление активности роста опухоли. В ходе ИГХ в образец патологической ткани, имеющей в своем составе клетки с антигенами Ki-67, добавляют специально синтезированные меченые антитела. В процессе реакции образуется комплексы «антиген-антитело», доля которых свидетельствует о количестве клеток, находящихся в активной фазе деления. В заключении указывается индекс Ki-67 – индекс пролиферативной активности, выраженный в процентах. При низких значениях индекса опухоль считается менее агрессивной, при высоких – высокоагрессивной. Также по индексу пролиферативной активности можно судить о возможном ответе опухолевого процесса на терапию, оценить эффективность уже проведенного лечения.
Комплексное гистологическое и иммуногистохимическое исследование опухолевого процесса является достаточно сложным и трудоемким анализом. Однако объективность и целесообразность его проведения оправдана точными результатами диагностики, наиболее верным выбором терапии и ответом на нее, более качественным прогнозом течения заболевания.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Результат исследования представляет собой морфологическое описание препарата и подсчет количества клеток, имеющих или не имеющих антиген Ki-67. Высчитывается индекс пролиферативной активности (процент клеток с наличием экспрессии белка Ki-67). Интерпретация полученного результата проводится врачом, назначившим исследование, в зависимости от локализации опухолевого процесса, его типа, проведенного лечения и т.д.
Кто назначает исследование?
Что значит ki67 в онкологии
ИГХ, иммуногистохимическое исследование ткани, исследование образца опухолевой ткани, исследование ткани опухоли;
Белок p16 INK4a ; онкопротеин; гистологическое исследование, иммуногистохимическое исследование (ИГХ).
Какой биоматериал можно использовать для исследования?
Образец ткани (биоптат) образования шейки матки.
Общая информация об исследовании
Дисплазия и рак шейки матки занимают значительное место в структуре онкологических заболеваний среди женщин. Дисплазия представляет собой изменение эпителия влагалищной части шейки матки и появление в нем клеток с признаками атипии. Считается предраковым заболеванием, но при своевременном обнаружении и лечении процесс обратим и не приводит к развитию рака шейки матки. Рак шейки матки является достаточно распространенной и важной проблемой среди всех онкологических заболеваний у женщин. Доказано, что в развитии данной патологии играет роль наличие некоторых типов вируса папилломы человека (ВПЧ), способных при определенных условиях вызывать озлокачествление дисплазии (или других предраковых заболеваний).
На современном этапе диагностики рака шейки матки одним из достоверных методов исследования является комплексное гистологическое и иммуногистохимическое исследование по экспрессии p16INK4a, дающее наиболее объективную и полную оценку происходящим процессам.
p16INK4a – это белок, который обладает функцией регулирования клеточного цикла и предотвращает процесс бесконтрольного деления клеток. При определенных условиях вирус папилломы человека (ВПЧ) способен встраиваться в геном клетки и оказывать влияние на процесс ее деления, что приводит к усиленной пролиферации. При этом в опухолевых клетках, процесс деления которых происходит уже под контролем измененного генома, происходит реактивное увеличение количества белка p16INK4a. Таким образом, в опухолевых клетках увеличивается экспрессия белка p16INK4a, что сигнализирует о встраивании ВПЧ в геном клетки и ее перерождении в опухолевый процесс.
Гистологическое исследование, являющееся первым этапом комплексной диагностики, представляет собой морфологическое описание патологического процесса, в том числе определение «злокачественности». Иммуногистохимическое исследование (ИГХ) выполняется вторым этапом и позволяет определить «пролиферативный потенциал» новообразования, т.е. возможность злокачественного перерождения клеток, а также спрогнозировать течение уже имеющейся опухоли. ИГХ проводится путем добавления к исследуемому материалу специальных антител, которые связываются с белком p16INK4a. Затем происходит качественная оценка образовавшегося комплекса антиген-антитело и делается вывод об экспрессии белка p16INK4a на поверхности клеток.
Антиген Ki-67 представляет собой специфический белок, находящийся в ядерном материале опухолевой клетки, и является необходимым для осуществления ее пролиферации, т.е. деления. Обнаружение Ki-67 указывает на опухолевые клетки, которые находятся в фазе деления клеточного цикла. Это позволяет понять, насколько активно и быстро происходит деление опухолевых клеток, а следовательно, и скорость роста новообразования, оценить риск метастазирования, определиться с тактикой терапии и вероятным ответом на нее, прогнозом заболевания.
Считается, что выявление маркера Ki-67 наиболее показательно при раке молочной железы, однако ряд исследований доказывает целесообразность проведения анализа при наличии доброкачественных новообразований с оценкой риска их озлокачествления.
Совместное гистологическое и иммуногистохимическое исследование опухолевого материала позволяет сначала получить морфологическое описание процесса, а затем определить его пролиферативную активность – степень и скорость деления клеток. Это дает достаточно точную и объективную оценку степени злокачественности опухоли и прогноз ее дальнейшего развития.
Гистологическое исследование проводится путем изучения срезов опухолевого материала под микроскопом после предварительного окрашивания, которое позволяет выявить и описать отклонения от нормы в структуре ткани, дать характеристику изменениям и сделать вывод о доброкачественности или злокачественности процесса. Далее проводится иммуногистохимическое исследование (ИГХ), направленное на выявление активности роста опухоли. В ходе ИГХ в образец патологической ткани, имеющей в своем составе клетки с антигенами Ki-67, добавляют специально синтезированные меченые антитела. В процессе реакции образуется комплексы «антиген-антитело», доля которых свидетельствует о количестве клеток, находящихся в активной фазе деления. В заключении указывается индекс Ki-67 – индекс пролиферативной активности, выраженный в процентах. При низких значениях индекса опухоль считается менее агрессивной, при высоких – высокоагрессивной. Также по индексу пролиферативной активности можно судить о возможном ответе опухолевого процесса на терапию, оценить эффективность уже проведенного лечения.
Комплексное гистологическое и иммуногистохимическое исследование опухолевого процесса является достаточно сложным и трудоемким анализом. Однако объективность и целесообразность его проведения оправдана точными результатами диагностики, наиболее верным выбором терапии и ответом на нее, более качественным прогнозом течения заболевания.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
1) Результат исследования представляет собой морфологическое описание препарата и подсчет количества клеток, имеющих или не имеющих антиген Ki-67. Высчитывается индекс пролиферативной активности (процент клеток с наличием экспрессии белка Ki-67). Интерпретация полученного результата проводится врачом, назначившим исследование, в зависимости от локализации опухолевого процесса, его типа, проведенного лечения и т.д.
2) Повышение экспрессии p16INK4a:
Результат представлен в виде морфологического описания исследуемой ткани после окрашивания специальными красителями и характера изменений. Значения зависят от типа опухоли, анамнеза, проведенного лечения и других факторов. Окончательную интерпретацию проводит врач в каждом конкретном случае.
Цитологическое исследование мазков (соскобов) с поверхности шейки матки (наружного маточного зева) и цервикального канала на атипию
Human Papillomavirus 16/18 (HPV 16/18), ДНК [реал-тайм ПЦР]
Лабораторные маркеры рака шейки матки
Кто назначает исследование?
Маркер бесконечности Ki-67
Белок Ki-67 — самый широко используемый маркер пролиферации как в нормальных, так и в опухолевых клетках. Впервые описан в 1983 году в Институте патологии в немецком городе Киль, где и были синтезированы первые антитела к нему в 67 лунке планшета [1].
Негистоновый белок Ki-67 кодируется геном MKI67. Он участвует в клеточном цикле, вовлекаясь в биогенез рибосом, организацию гетерохроматина и разделение митотических хромосом. Полный спектр его функций все еще неясен. Трудности исследования Ki-67 связаны с отсутствием гомологичных белков с уже известной функцией, а также с его большой молекулярной массой и высокой чувствительностью к разрушению протеазами [2].
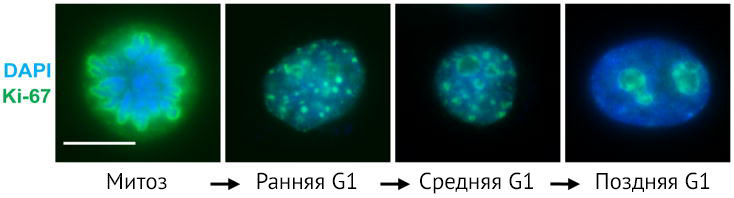
Ki-67 обнаруживается в ядрах клеток во все активные фазы клеточного цикла: G1, S, G2, M. Ki-67 весьма «ветреный» белок: его распределение и количество вариабельно и зависит от конкретного момента жизни клетки (рис. 1) [3]. От фазы G1 к фазе М его количество увеличивается, достигая максимума во время метафазы митоза. В самом начале фазы G1 локализация Ki-67 совпадает с локализацией сателлитной ДНК в центромерах и теломерах хромосом. Далее при прогрессии фазы G1 эта колокализация исчезает. К середине фазы G1 белок Ki-67 начинает выявляться в ядрышках, затем, в фазу G2, — и в ядрышках, и в кариоплазме.
.
Но все меняется, когда происходит митоз. В профазу Ki-67 в виде тонкой сети связан с конденсированным хроматином. В метафазу эта сетчатая структура окружает уже отдельные хромосомы. После разрушения ядерной мембраны часть Ki-67 распределяется диффузно в цитоплазме. В анафазу и телофазу митоза количество Ki-67 в клетках начинает быстро снижаться.
При переходе клетки после митоза в фазу G0 Ki-67 быстро подвергается катаболизму (путем опосредованной протеасомами деградации) и перестает выявляться в ядрах интерфазных клеток [4].
Ki-67 также обнаруживается при гиперэкспрессии p53 и p21, вызванной блокированием репликации или повреждением ДНК [2].
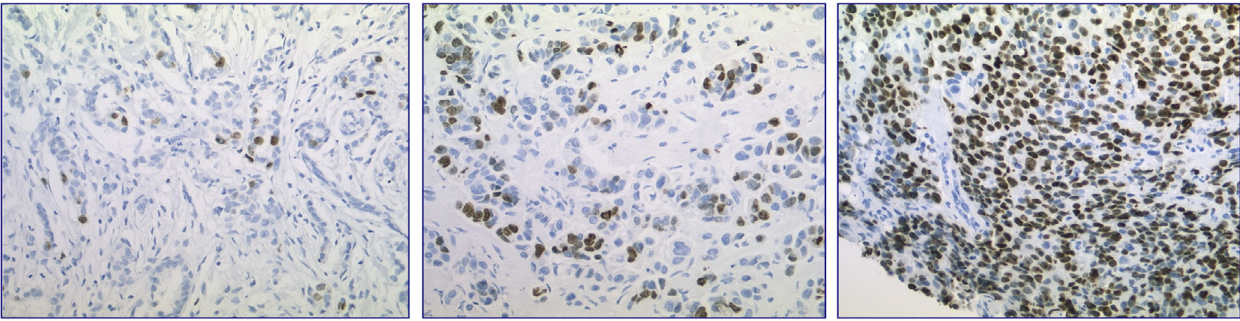
Длительное время Ki-67 определялся как иммуногистохимический маркер, отражающий лишь активность пролиферации. Это обусловило его важную роль в классификации злокачественных новообразований, таких как рак молочной железы, нейроэндокринные опухоли и лимфомы [5]. Определение индекса Ki-67 является более чувствительным методом для оценки пролиферативной активности, чем подсчет фигур митоза, поскольку позволяет выявлять клетки во всех активных фазах клеточного цикла и уменьшает вероятность неверной интерпретации микроскопической картины. Переход патоморфологов в своей рутинной практике к расчету индекса пролиферации по уровню Ki-67 стал начальным этапом движения в сторону стандартизации и объективизации гистологических исследований. От двоичной системы «есть экспрессия» (1) / «нет экспрессии» (0) фокус сместился к оценке степени выраженности маркера в исследуемых образцах.
Индекс пролиферации — это процент клеток с ядерным окрашиванием от общего числа опухолевых клеток. Интенсивность и тип экспрессии маркера не учитывается (перинуклеолярный, нуклеоплазменный, перихромосомный). Подсчет включает в себя не менее 500 опухолевых клеток (в идеале не менее 1000) не менее чем в 3 полях зрения при увеличении ×400. В случае гетерогенности опухоли выбирают участки с наибольшей митотической активностью [6].
Общие характеристики уровня пролиферации для опухолевой ткани различных локализаций:
В лабораториях используют антитела к Ki-67 клонов MIB-1 (для работы с материалом, полученным от человека, крупного рогатого скота, собак, овец и лошадей) и MIB-5 (для работы с материалом, полученным от крыс и других грызунов). Эти структуры показали более высокое сродство к эпитопу антигена Ki-67 в условиях формалиновой фиксации доставляемого материала [2].
Особую значимость этот маркер приобрел при патоморфологическом исследовании опухолей молочной железы. Гистологический подтип гормон-позитивных люминальных опухолей определяется на основании индекса Ki-67: подтип А (Ki-67
.
Прогностические горизонты применения маркера Ki-67 постоянно расширяются. Уточняется и дополняется его значение в предикции результатов лекарственной терапии опухолей. Например, для рака молочной железы, который не отвечает на химиотерапию, повышение Ki-67 является плохим прогностическим маркером. Напротив, в опухолях, реагирующих на химиотерапию, этот эффект не наблюдается, и даже присутствует корреляция увеличения Ki-67 с улучшением прогноза.
Объяснение этому феномену можно логически вывести из понимания биологии каждого подтипа опухоли:
В настоящее время методы иммуногистохимической детекции Ki-67 представляются в виде несколько упрощенной картины, как будто Ki-67 «включен» во время клеточной пролиферации (характерное коричневое окрашивание ядер) и «выключен» во время покоя и старения клетки (нет окрашенных ядер, может обнаруживаться в цитоплазме). Но важное клиническое значение может иметь также интерпретация факта неуклонного роста экспрессии Ki67 от фазы G1 к фазе М. Также выяснено, что чем дольше клетка находится в состоянии покоя, тем ниже будет уровень Ki-67 при повторном входе в клеточный цикл [5,7]. Для анализа этих данных требуются методы системной биологии с выведением формулы, позволяющей учесть все характеристики Ki-67 в доставленном материале. Это позволит более точно отразить пролиферативный статус клеток и определить клиническую стратегию. Ключевым моментом эффективности таких многофакторных алгоритмов является, несомненно, точность «сырых» данных. И здесь мы уже говорим о стандартизации патоморфологического исследования, которое в современной практике должно базироваться на цифровой обработке гистологических изображений.
Что значит ki67 в онкологии
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
Сравнение цифрового и визуального методов для оценки индекса Ki-67 в инвазивных карциномах молочной железы
Журнал: Архив патологии. 2018;80(2): 38-42
Кушнарев В. А., Артемьева Е. С., Кудайбергенова А. Г. Сравнение цифрового и визуального методов для оценки индекса Ki-67 в инвазивных карциномах молочной железы. Архив патологии. 2018;80(2):38-42.
Kushnarev V A, Artemyeva E S, Kudaybergenova A G. Comparison of digital and visual methods for Ki-67 assessment in invasive breast carcinomas. Arkhiv Patologii. 2018;80(2):38-42.
https://doi.org/10.17116/patol201880238-42
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
Цель исследования — cравнить два метода количественной оценки индекса пролиферативной активности (ИПА): визуального метода оценки несколькими исследователями и цифрового анализа изображений. Использование индекса Ki-67 в ежедневной клинической практике патолого-анатомического отделения связано с проблемой воспроизводимости количественной оценки ИПА Ki-67. В связи с развитием цифровых методов визуализации в морфологии предлагаются новые методы оценки ИПА с помощью цифрового анализа изображений (ЦАИ). Материал и методы. Сравнивали данные ИПА Ki-67, полученные при визуальной оценке и с помощью цифрового анализа изображений 104 случаев карцином молочной железы G2—G3. Препараты были отсканированы с помощью сканера гистологических препаратов Panoramic III (3D Histech, Венгрия) и получены цифровые изображения. ЦАИ проведен с помощью программного обеспечения 3D Histech QuantCenter (3D Histech, Венгрия) c разметкой 3—10 зон. Полученные препараты оценивали два исследователя онкопатоморфолога независимо друг от друга. Результаты. Уровень согласия между визуальным и цифровым методом анализа достоверно не отличался (p>0,001). Нами была выделена серая зона в пределах 10—35% ИПА, где значения индекса Ki-67 показали слабую связь между анализируемыми группами (ICC 0,47). Значения индекса Ki-67 ниже 10% и выше 35% показали достаточный уровень воспроизводимости в пределах одной лаборатории. Заключение. Считаем, что цифровая сканированная форма гистологического препарата, которую можно оценить, используя автоматические программные модули анализа, является независимым и объективным методом оценки пролиферативной активности для валидирования индекса Ki-67.
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург, Россия
Для оценки пролиферативной активности опухоли в клинической практике наиболее изученным считается митотический индекс, оцениваемый по гистологическому препарату, и индекс Ki-67 — по иммуногистохимически окрашенному препарату. Эти методы имеют определенные ограничения и если оценка митотического индекса прочно вошла в классификационные диагностические схемы, то при определении индекса Ki-67 неоднократные попытки стандартизировать методические и технологические подходы приводили всегда к выводу о необходимости валидизации методики оценки в спланированных клинических исследованиях и слабой воспроизводимости этого признака в больших исследованиях с достаточным количеством лабораторий-участниц [1].
Поскольку оценка индекса пролиферативной активности (ИПА) по Ki-67 является прогностическим и предиктивным суррогатным маркером опухолей молочной железы, для стандартизации подходов в оценке ИПА по Ki-67 в клиническом ведении пациентов с карциномой молочной железы в марте 2010 г. была создана международная рабочая группа [1]. Целью рабочей группы явилось определение общей стратегии гармонизации на преаналитическом и постаналитическом этапе диагностики и методических подходов к унифицированной оценке ИПА по Ki-67.
Внедрение количественной оценки вместо традиционно принятой полуколичественной системы оценки в баллах (например, Allred) всегда является критическим этапом в применении метода. Внедрение ИПА Ki-67 с обязательной оценкой процентного соотношения позитивно окрашенных клеток в ежедневную практику патолого-анатомического отделения связано с проблемой воспроизводимости количественной оценки ИПА. В качестве суррогатного маркера ИПА используется для разделения ER-позитивного люминального, А (прогностически благоприятного) и В (прогностически неблагоприятного) подтипа карцином молочной железы. Пороговым уровнем разделения ИПА между этими двумя группами считается 14%, где соответственно люминальный тип, А содержит менее 14% Ki-67-позитивных клеток, люминальный тип В — более 14% Ki-67-позитивных клеток [2]. Кроме того, пороговый уровень индекса Ki-67 выше 15% важен для назначения адъювантной химиотерапии при люминальном В, но не люминальном А-подтипе карцином молочной железы.
Ряд профессиональных сообществ, например Европейское общество патологов (European Society of Pathology — ESP), некоторые руководства [8] рекомендуют делать повторную оценку индекса Ki-67 c участием второго экспертного мнения или использовать цифровой анализ гистологических сканов, если ИПА находится в пределах от 10 до 35%, в так называемой серой зоне, по данным разных авторов [9]. Панель экспертов St. Galen [4] рекомендует исследователю при оценке окраски на Ki-67 ориентироваться на медиану ИПА по лаборатории с целью повышения воспроизводимости между исследователями. Следовательно, стандартизация измерения этого показателя независимо от квалификации патолога и уровня морфологической лаборатории необходима в лечебной тактике.
В связи с развитием цифровых методов визуализации в морфологии предлагаются новые методы оценки ИПА с помощью цифрового анализа изображений (ЦАИ) сканов гистологических препаратов. Предполагается, что автоматический анализ индекса Ki-67 является методом, способным заменить визуальную оценку ИПА и улучшить точность и воспроизводимость оценки.
Целью исследования являлось сравнение двух методов исследования ИПА: визуального метода оценки несколькими исследователями и цифрового анализа изображений. Мы не ставили перед собой цель проанализировать распределение ИПА Ki-67 по видам материала или сравнить виды материала между собой.
Материал и методы
Подготовка когорты пациентов
Из 3842 случаев, исследованных в лаборатории патологической анатомии НИИ онкологии им. Н.Н. Петрова в период с июля по октябрь 2016 г., в 542 (14,2%) случаях проведено стандартное исследование индекса Ki-67. Распределение по формам заболевания было следующим (рис. 1):


Фиксированный в формалине (24 ч), залитый в парафин материал резецированных карцином и трепанобиопсий молочной железы c инвазивной карциномой подвергался стандартному морфологическому исследованию с оценкой степени гистологической злокачественности. Иммуногистохимическое исследование пролиферативной активности Ki-67 (кроличьи моноклональные антитела, клон 30−9, CONFIRM, «Roche — Ventana») проведено, согласно протоколу (табл. 2)

Полученные препараты оценивали два исследователя онкопатоморфолога независимо друг от друга. Исследователи обладали различным опытом в области оценки ИПА Ki-67. Препараты отсканированы с помощью сканера гистологических препаратов Panoramic III (3D Histech, Венгрия) и получены цифровые изображения. ЦАИ проведен с помощью программного обеспечения 3D Histech QuantCenter (3D Histech, Венгрия) c разметкой 3—10 зон (рис. 2)

Статистический анализ
Статистический анализ выполнен с помощью программного обеспечения R-studio, c применением Wilcoxon signed rank test, так как распределение в выборке отличалось от нормального. Показателем согласованности между значениями двух переменных служил коэффициент непараметрической корреляции r Спирмена, где r=1 обозначает максимально сильную положительную линейную взаимосвязь. Внутриклассовый коэффициент корреляции (Intraclass Correlation — ICC) использовали для выявления связи между методами оценки.
В качестве шкалы для обнаружения согласия (табл. 3)

Результаты и обсуждение
Медиана ИПА по анализируемому материалу, согласно данным автоматического модуля анализа QC, составила 25,5% (табл. 4, рис.


Распределение ИПА во всех группах было близко к бимодальному. По степени злокачественности (G2—3) ИПА продемонстрировал высокие значения в grade 3 (табл. 5),

Медианы, полученные в границах 10—35% ИПА, находятся в интервале от 21 до 24%. Медиана серой зоны составила
24% ИПА, оцененного с помощью цифрового анализа, группа QC (табл. 6).

Уровень согласия между визуальным и цифровым методом анализа достоверно не различался (p>0,001) между группой QC и исследователями, тогда как между 1-м и 2-м исследователем выявлены значительные различия (p 
При сравнении рекомендованных границ ИПА значения коэффициентов ICC, PAC показали наличие слабой связи при визуальном методе анализа между 1-м и 2-м исследователем в границах серой зоны 10—35% ИПА по сравнению со средней и сильной связью группы QC/1-й исследователь и QC/2-й исследователь соответственно в других пределах (табл. 8).

Заключая, хотели бы сказать, что визуальная оценка индекса Ki-67 является воспроизводимым показателем вне пределов серой зоны. Статистическая обработка данных индекса Ki-67, полученного в результате визуальной оценки разными исследователями или автоматического анализа изображений, показала положительную корреляцию (r=0,89—0,92). Распределение ИПА в группе цифрового анализа выявило наличие серой зоны 10—35% ИПА, где существует недостаточная воспроизводимость между исследователями (ICC 0,47). Медиана серой зоны при оценке ИПА в карциномах молочной железы в нашем исследовании составила 24%, что коррелирует со значениями медианы зарубежных публикаций [3, 5, 8].
Значения ICC и PAC в серой зоне демонстрируют слабую связь между исследователями (см. табл. 8), что нередко приводит к диагностическим неточностям, так как порог 14—20% ИПА для разграничения люминального А- и В-подтипа карцином молочной железы находится в пределах серой зоны.
Низкие и даже отрицательные показатели ICC и PAC (см. табл. 8) в пределах от 0 до 10% связаны с большим внутригрупповым разбросом ИПА. Высокие значения коэффициента согласия (PAC) между цифровым анализом изображений и данными 2-го исследователя свидетельствуют о низком межгрупповом разбросе и характеризуют однородность выборки в интервале 0—10% ИПА. Возможно, это связано с более длительным опытом оценки ИПА 2-м исследователем.
В пределах 36—100% ИПА высокое значение PAC, коэффициента корреляции r в группах QC/1-й исследователь и QC/2-й исследователь подтверждает, что межгрупповое распределение ИПА достаточно хорошо соотносится как при визуальной оценке, так и при ЦАИ. В данном интервале полагаем, что цифровой анализ и визуальная оценка сопоставимы. Полученные данные свидетельствуют, что цифровой анализ способен служить одним из способов стандартизации исследования ИПА в предполагаемой границе до 35% и важен для внутрилабораторного контроля.
Анализ данных при помощи каппы воспроизводимости Cohen в модификации Fleiss [6] возможен только при наличии стандартизованного метода оценки ИПА, в качестве которого может выступать ЦАИ. Визуальная оценка с применением количественных методик требует выработки навыков оценки иммуногистохимических окрасок и определения границы стандарта, что считать достаточным уровнем воспроизводимости ИПА.
Мы рассматриваем возможность использования ЦАИ в качестве внешнего контроля и обучения патоморфологов для оценки ИПА. Для этого необходимо создание цифрового архива отсканированных изображений гистологических препаратов, который будет отвечать современным потребностям морфологической диагностики и клинической практики. Вне пределов серой зоны также необходимы цифровые архивы сканированных препаратов для обучения морфологов количественной оценке индекса Ki-67 в карциномах молочной железы. В пределах серой зоны рекомендуется использование ЦАИ из-за недостаточности показателей воспроизводимости и вследствие клинически обоснованной необходимости разделения на суррогатные подгруппы люминальных карцином.
Заключение
Распределение ИПА при цифровом методе анализа подтвердило границы серой зоны от 10 до 35% с медианой 24%. В данных границах наблюдалась недостаточная воспроизводимость между исследователями при визуальном методе анализа. Значения ИПА выше и ниже границы 10—35% показали достаточный уровень воспроизводимости между цифровым и визуальным методом анализа и являются сопоставимыми. На основании полученных результатов можно констатировать, что цифровой анализ изображений является одним из методов контроля воспроизводимости ИПА Ki-67 для исследователей.
Концепция и дизайн исследования: А.Г.К., В.А.Л.
Сбор и обработка материала: В.А.К., А.Г.К., Е.С.А.
Статистическая обработка: В.А.К.
Написание текста: В.А.К.
Редактирование: А.Г.К., В.А.К., Е.С.А.
Авторы заявляют об отсутствии конфликта интересов.