Пневмония и Ковидные изменения на рентгене. В чем разница?
Поражение лёгких, пневмония, вызванные коронавирусной инфекцией, отличается от других видов поражения лёгких. Принципиальное отличие основывается на довольно простых вещах.
«Обычная» пневмония возникает из-за того, что в нижних отделах дыхательных путей (чаще на фоне гриппа или острых респираторных заболеваний) накапливается воспалительная жидкость, которая в свою очередь является благотворной средой для накопления бактерий. Сама мокрота, которая скапливается в альвеолах, препятствует нормальному дыхательному процессу. В ней селятся и начинают размножаться бактерии, которые в свою очередь начинают провоцировать воспаление отдельных сегментов лёгких.
Пневмония, вызванная коронавирусной инфекцией (COVID-19 пневмония), — это отдельный тип, при котором поражение лёгких, можно назвать особым термином «пневмонит». Это означает, что при данном поражении в патологический процесс может вовлекаться как интерстициальная ткань Легких, так и альвеолярные стенки, и близлежащие сосуды. Таким образом, воспалительные изменения могут поражать все структуры легких. Это приводит к нарушению газообмена и нормальному насыщению крови кислородом.
При пневмонии, SARS-Cov-2, вызванной возбудителем COVID-19., причиной поражения является не бактериальная инфекция, а вирусная природа заболевания. Возбудитель COVID-19, попадая в организм, затрудняет дыхательную функцию лёгких, при возникновении их поражение чаще носит не локализованный характер, а распространённый. Поражение лёгких, при этом не ограничивается отдельными участками, как при бактериальной пневмонии. Воспаление распространяется, захватывая как правило оба лёгких.
Вот основные критерии отличия:
Записаться можно по телефону (391) 205−00−48 или через личный кабинет
Легочная гипертензия: взгляд детского пульмонолога
Опубликовано в журнале: «ПРАКТИКА ПЕДИАТРА»; июнь; 2016; стр. 10-15.
С.Э. Дьякова, к. м. н., в. н. с. отдела хронических воспалительных и аллергических болезней легких ОСП НИКИ педиатрии им. Ю.Е. Вельтищева
ГБОУ ВПО РНИМУ им.Н.И. Пирогова Минздрава России, г. Москва
Ключевые слова: легочная гипертензия, пульмонология, дети
Keywords: pulmonary hypertension, pulmonology, children
В практике детского пульмонолога пациенты с легочной гипертензией (ЛГ) встречаются относительно нечасто: по статистике, ЛГ имеют примерно 1,9 на 1000 рождающихся ежегодно детей, а распространенность легочной артериальной гипертензии составляет 15 случаев на 1 млн человек [5, 11, 18].
Хронические заболевания легких в 80-90% случаев являются причиной формирования хронического легочного сердца и сопровождаются развитием ЛГ у 30-50% больных. При отсутствии своевременной адекватной диагностики и лечения эта патология может быстро приводить к фатальному исходу. Установлено, что декомпенсированное хроническое легочное сердце в 30-37% случаев служит причиной смерти от недостаточности кровообращения и составляет 12,6% в структуре причин летальности от сердечно-сосудистых заболеваний. Причем многие причины ЛГ у детей значительно отличаются от таковых у взрослых пациентов [3, 5].
Известно, что малый круг кровообращения состоит из сосудистых элементов, которые находятся в анатомической и функциональной взаимосвязи. Разветвленная сеть артериовенозных анастомозов соединяет терминальные артериолы с легочными венами. В норме объем кровотока, минующего капилляры, невелик. Изменения тонуса стенки анастомозов обеспечивает расширение и сужение их просвета вплоть до полного закрытия. При повышении легочного артериального давления анастомозы, обеспечивая кровоток в обход капилляров, ограничивают этим дальнейшее повышение давления и предотвращают перегрузку давлением правого желудочка (ПЖ) [3, 6].
При этом малый круг кровообращения (МКК) осуществляет депонирование крови, обеспечение питанием респираторной ткани легких, реабсорбцию альвеолярной жидкости (дренажная функция) и нейтрализацию эмболов в венозной крови (фильтрационная функция), а также отвечает за транспортировку крови и газообмен.
В зависимости от локализации сопротивления кровотоку различают прекапиллярную, капиллярную и посткапиллярную ЛГ. Прекапиллярная ЛГ характеризуется нарастанием сопротивления в артериальном отделе МКК, что обусловлено падением парциального давления кислорода в альвеолах при обструктивных заболеваниях легких, системных васкулитах и тромбоэмболических осложнениях, а также при ограничении подвижности грудной клетки при кифосколиозе, ожирении и пневмофиброзе. Капиллярная ЛГ возникает при несоответствии объема кровотока и капиллярного русла. При заболеваниях легких эта форма гипертензии часто сочетается с прекапиллярной, поэтому условно объединяется с ней. Посткапиллярная ЛГ развивается при повышении давления в левом предсердии более 20 мм рт. ст. и наблюдается при митральных пороках и левожелудочковой недостаточности. Длительное повышение давления способствует развитию необратимых органических изменений сосудистого русла МКК, которые и становятся причиной стойкой и прогрессирующей ЛГ [3, 6].
Существующие современные международные рекомендации по диагностике и лечению ЛГ, созданные в 2009 году объединенной рабочей группой Европейского кардиологического (ESC) и Европейского респираторного обществ (ERS), одобрены различными авторитетными профессиональными врачебными Ассоциациями и дополнены в 2015 году экспертами Американской кардиологической ассоциации (AHA) и Американского общества специалистов в области торакальной медицины [1, 5, 11, 18, 20].
ЛГ представляет собой патофизиологическое явление, к которому может приводить целый ряд клинических состояний, в частности, она может осложнять большинство сердечно-сосудистых заболеваний и болезней дыхательной системы. Согласно классификации ЛГ 2008 года, выделяют пять основных типов ЛГ:
1. Легочная артериальная гипертензия (включающая два подтипа: веноокклюзивная болезнь легких и/или легочный капиллярный гемангиоматоз и персистирующая ЛГ у новорожденных).
2. ЛГ вследствие патологии левых отделов сердца.
3. ЛГ вследствие болезней легких и/или гипоксии.
4. Хроническая тромбоэмболическая ЛГ и прочие варианты обструкции легочной артерии.
5. ЛГ с неясными и/или многофакторными механизмами.
У детей наиболее часто встречается легочная артериальная гипертензия и ЛГ, ассоциированная с патологией дыхательной системы и/или гипоксией [1, 5].
Среди причин ЛГ, ассоциированной с патологией дыхательной системы и/или гипоксией, основными являются хронические обструктивные заболевания легких; к более редким этиологическим факторам ЛГ этого типа в детском возрасте относятся пороки развития бронхолегочной системы, интерстициальные заболевания легких, легочная патология со смешанными обструктивно-рестриктивными нарушениями, нарушения дыхания во время сна, альвеолярная гиповентиляция, высокогорная легочная гипертензия, легочная гипертензия вследствие хронических тромботических и/или эмболических заболеваний, а также системные заболевания с поражением легких (саркоидоз, гистиоцитоз легочных клеток Лангерганса, лимфангиоматоз, васкулиты).
Принципиально в развитии ЛГ можно выделить три стадии. На первой стадии увеличенное легочное давление является единственной гемодинамической аномалией: больные не имеют отчетливых симптомов заболевания, но может отмечаться одышка при физической нагрузке. На второй стадии при уменьшении сердечного выброса появляется развернутая клиническая симптоматика в виде гипоксемии, одышки, синкопальных состояний, при этом давление в ЛА сохраняется на стабильно высоком уровне. С появлением правожелудочковой недостаточности наступает третья стадия заболевания: несмотря на стабильно высокие значения легочного давления, резко падает сердечный выброс, появляются венозный застой и периферические отеки. Продолжительность каждой стадии может быть различной; течение ЛГ может быть острым и хроническим; быстро, умеренно и медленно прогрессирующим; крайне редко встречаются случаи спонтанного регресса заболевания.
Начальные признаки ЛГ при заболеваниях легких обычно маскируются проявлениями основного заболевания (приступный период бронхиальной астмы, спонтанный пневмоторакс, выраженный плевральный выпот и т. д.). Иначе протекает ЛГ при хронических обструктивных болезнях легких: ЛГ и вызванная ею патология сердца и недостаточность кровообращения занимают первое место среди осложнений этих заболеваний, определяют жизненный прогноз пациентов и эффективность их лечения.
Основной жалобой у детей с ЛГ бывает одышка. Именно поэтому нередко первым специалистом, к кому могут обращаться пациенты с ЛГ, является пульмонолог. В дебюте заболевания одышка возникает только при физической нагрузке, по мере прогрессирования заболевания одышка появляется в покое, иногда сопровождается приступами удушья. Чем выше давление в легочной артерии, тем ярче выражена одышка.
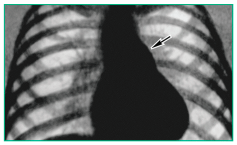
При рентгенографии органов грудной клетки у детей с ЛГ могут быть не только диагностированы заболевания легких, при которых характерна ЛГ (эмфизема легких, пневмосклероз, туберкулез, саркоидоз, пороки легких и т. д.), но и выявлены патогномоничные признаки ЛГ, такие как расширение корней легких, усиление легочного рисунка, общее или неравномерное повышение прозрачности легочных полей, интерстициальный отек, выбухание дуги ЛА по левому контуру, увеличение коэффициента Мура (процентное отношение поперечника дуги ЛА к половине диаметра грудной клетки на уровне диафрагмы (норма до 30%)), расширение нисходящей ветви правой ЛА (рис.). При этом индекс Мура и ширина правой ЛА коррелируют с высотой давления в ЛА и могут быть использованы в качестве критериев наличия и выраженности ЛГ. На ранних стадиях ЛГ до развития дилатации ПЖ размеры сердца могут не изменяться; по мере нарастания ЛГ и увеличения ПЖ на рентгенограмме грудной клетки в боковой проекции ретростернальное пространство выполняется тенью ПЖ. Еще большей информационной ценностью для верификации диагноза обладает компьютерная томография легких [1, 4, 6].
Рисунок
Повышение прозрачности легочной ткани, усиление легочного рисунка и выбухание дуги легочной артерии у ребенка 12 лет с ЛГ
При электрокардиографии ЛГ можно заподозрить по наличию признаков перегрузки и гипертрофии правых отделов сердца: отклонение электрической оси сердца вправо, перегрузка правого предсердия и правого желудочка, отрицательный зубец Т в грудных отведениях, транзиторная блокада правой ножки пучка Гиса [1, 3, 6].
Тем не менее, электрокардиография и рентгенография дают возможность лишь косвенно судить о наличии ЛГ. В течение длительного времени единственным методом исследования, позволявшим оценивать состояние правых отделов сердца, получать характеристики внутрисердечного кровотока и определять давление в правых отделах сердца и ЛА, была катетеризация правых отделов сердца и ЛА, которая на сегодняшний день продолжает использоваться для исключения кардиальных причин ЛГ (врожденные пороки сердца), определения основных параметров легочной и центральной гемодинамики, а также для подбора эффективных вазодилататоров. Однако, в силу инвазивности и высоких рисков осложнений, эта методика не может быть рекомендована для динамического наблюдения детей с ЛГ [11, 18].
Достоверно установлено, что показатели легочной гемодинамики при проведении ЭхоКГ сопоставимы с данными, полученными при катетеризации ЛА. В связи с этим всем младенцам с бронхолегочной дисплазией в анамнезе рекомендовано проведение эхокардиографического скрининга для исключения формирования ЛГ. При обследовании детей с ЛГ с помощью ЭхоКГ рекомендуется проведение теста с физической нагрузкой, который позволяет уточнять степень функциональных нарушений.
Немаловажным для дифференциальной диагностики ЛГ является определение газового состава крови, в частности, определение насыщения ее кислородом: снижение этого показателя наблюдается при сбросе крови справа налево, а также при ЛГ, сочетающейся с дыхательной недостаточностью (хронические обструктивные заболевания легких, массивная тромбоэмболия легочной артерии и т. д.) [1, 5, 11].
Исследование функции легких позволяет выявить вид и степень выраженности вентиляционных нарушений (обструктивные, рестриктивные смешанные). В целях дифференциальной диагностики, наряду со спирометрией, целесообразно проведение бодиплетизмографии и оценки диффузионной способности легких. У детей старше 6 лет для контроля переносимости нагрузок должна использоваться проба с 6-минутной ходьбой. Если ребенок относится к группе риска нарушений дыхания во сне, то в план его обследования должна включаться полисомнография.
Для верификации диагноза ЛГ в детской практике редко прибегают к открытой биопсии легких с последующим морфометрическим исследованием мелких сосудов, поскольку она сопряжена со значительными рисками и не обладает высокой информативностью в связи с неравномерным поражением сосудов легких.
Таким образом, диагностика ЛГ у детей предполагает проведение комплексного обследования с целью установления диагноза, оценки клинического класса и типа ЛГ, уровня давления в ЛА и оценки функционального и гемодинамического статуса пациентов с определением стадии заболевания.
У детей с хроническими бронхолегочными заболеваниями необходимо регулярное проведение комплексного кардиологического обследования (ЭКГ, ЭхоКГ) с целью диагностики патологии легочной гемодинамики и предупреждения формирования легочного сердца. Раннее выявление ЛГ позволяет начать своевременное лечение и предупредить развитие сердечной декомпенсации.
Основные подходы к лечению детей с ЛГ включают в себя ежедневные физические нагрузки по переносимости, что способствует улучшению качества жизни и уменьшению клинической симптоматики [16], а также профилактику инфекционных заболеваний (вакцинирование от гриппа и пневмококковой инфекции), исключение активного и пассивного курения. Наибольшее внимание должно быть уделено лечению основного заболевания, ликвидации гипоксии, снижению давления в малом круге кровообращения, профилактике дистрофической гипоксии миокарда и лечению правожелудочковой недостаточности [7].
Хотя гипоксия не является единственным этиологическим фактором ЛГ, однако развивающаяся гипоксемия у больных с хронической бронхолегочной патологией обусловливает необходимость применения кислорода в качестве терапевтического средства [21].
Тем не менее, специфической терапии ЛГ при хронической бронхолегочной патологии не разработано. В любом случае решение о назначении специфической терапии ЛГ у детей должно приниматься коллегиально, с учетом возрастных особенностей, тяжести течения и быстроты прогрессирования заболевания. В лечении больных с бронхиальной обструкцией, осложненной ЛГ, применение адреналина, норадреналина, эфедрина требует особой осторожности, так как они, помимо бронходилатирующего действия, вызывают гипертензивные реакции в малом круге кровообращения.
При неэффективности медикаментозного лечения проводится трансплантация легкого; в большинстве случаев для снижения давления в легочной артерии достаточно пересадки одного легкого. Двухлетняя выживаемость при трансплантации легкого составляет 60%, однако в отдаленные сроки у 50% больных развивается облитерирующий бронхиолит (проявление хронической реакции отторжения). На конечных стадиях высокой легочной гипертензии, особенно при сочетании с врожденными пороками сердца или кардиомиопатией, показана легочно-сердечная трансплантация; на начальных стадиях заболевания даже успешно выполненная операция не увеличивает продолжительность жизни таких больных [7].
Наибольшая эффективность лечения ЛГ у детей достигается в случае, если оно начато в ранний период болезни с применением средств, повышающих реактивность организма (лечебная физкультура, массаж, использование климатических факторов, иммуномодуляторов).
Комплексное лечение детей с ЛГ проводится непрерывно с соблюдением преемственности между стационаром, поликлиникой и санаторием-профилакторием; важность этого принципа вытекает из особенностей течения хронических бронхолегочных заболеваний, для которых и в фазе ремиссии необходима постоянная поддерживающая терапия.
Медицинские интернет-конференции
Языки
Первичная легочная гипертензия (клинический случай)
Таинкин А.А., Ирлык К. И., Круглова М. П., Бецуков И. О., Лобачёва Д. Н., Мартынова И. Р., Капьёва А. А.
Резюме
В статье представлен клинический случай первичной легочной гипертензии у молодого мужчины.
Ключевые слова
Статья
Проблема легочной гипертензии в настоящее время стала очень популярной. Если гипертоническая болезнь сейчас относительно хорошо контролируется, в ведении больных с легочной гипертензией существуют проблемы. Среди пациентов с данным заболеванием есть когорта больных с первичной легочной гипертензией. Этиология ее не известна. Актуальность проблемы высока в связи с малой продолжительностью жизни пациентов при отсутствии своевременно назначенной специфической терапии. Цель нашей работы – на примере клинического случая рассказать о принципах и сложностях ведения больных с первичной легочной гипертензией.
Клинический случай
Больной А., 39 лет поступил в кардиологическое отделение 25.02.2019 с жалобами: на одышку с затрудненным вдохом, головокружение, слабость при подъеме на один лестничный пролет, головные боли при повышении артериального давления, периодически перебои в работе сердца, учащенное сердцебиение.
С 2012 г. повышается артериальное давление максимально до 160 и 90 мм рт ст. Обращался в поликлинику по месту жительства, принимал антигипертензивные препараты. С 2014 г. беспокоит одышка при привычных физических нагрузках, проходил обследование в кардиологическом отделении и был направлен в кардиохирургический стационар с подозрением на врожденный порок сердца, куда обратился в 2017 г. в связи с усилением ордышки. Выполнено зондирование полостей сердца (25.09.2017): давление в легочной артерии 81 и 50 мм рт ст (среднее 61 мм рт ст), в правом желудочке 76 и 24 мм рт ст (44 мм рт ст), в правом предсердии 21 и 15 мм рт ст (среднее 18 мм рт ст). При мультиспиральной компьютерной томографии сердца 22.09.2017 (рис. 1) КТ-признаки изолированной артериальной легочной гипертензии. Расширение правых отделов сердца, гипертрофия миокарда правого предсердия и правого желудочка, расширение ствола и крупных ветвей легочной артерии. Данных за врожденный порок сердца не получено. Выписан с диагнозом «первичная легочная гипертензия. Рекомендовано наблюдение кардиолога по месту жительства, прием лекарственных препаратов: тромбо Асс 100 мг в сутки, периндоприл 2,5 мг 1 раз в сутки, беталок зок 50 мг 1 раз в сутки, амлодипин 5 мг 1 раз в сутки, торасемид 10 мг 1 раз в сутки. Был запланирован контроль допплерэхокардиографии через 3 месяца с последующей консультацией главного внештатного кардиолога. На фоне приема данных препаратов отмечал улучшение самочувствия, наблюдался в поликлинике по месту жительства. С ноября 2018 г. признан инвалидом 2 группы. Ухудшение состояния около двух месяцев, когда снизилась толерантность к физической нагрузке, появилась одышка при подъеме на один лестничный пролет, головокружение, слабость при выполнении физических нагрузок на работе. Госпитализирован для обследования, подбора специфической терапии легочной артериальной гипертензии.
Из анамнеза жизни известно, что пациент в течение 6 лет служил в армии: обслуживал самолеты. Работал на заводе по производству стеклопластика. В настоящее время работает слесарем: ремонтирует автомобили. Курит.
При осмотре отеков не было. При пальпации определялся сердечный толчок, эпигастральная пульсация, усиливающаяся на вдохе. При перкуссии левая граница относительной сердечной тупости располагалась по левой среднеключичной линии. При аускультации тоны сердца были ритмичными, частота сердечных сокращений составляла 60 в минуту, на верхушке сердца первый тон был ослаблен. Над легочной артерией определялся акцент второго тона. При аускультации легких выслушивалось везикулярное дыхание. Частота дыхательных движений составляла 20 в минуту. Живот при пальпации был мягким, безболезненным. Печень имела нормальные размеры.
В общем анализе крови обращал на себя внимание эритроцитоз 6,19 млн в 1 мкл, повышение уровня гемоглобина до 187 г/л.
При электрокардиографии 25.02.2019 (рис. 2) регистрировалось отклонение электрической оси сердца вправо, неполная блокада правой ножки пучка Гиса, признаки гипертрофии правого предсердия и правого желудочка.
При холтеровском мониторировании ЭКГ 27.02.2019 в течение всего периода мониторинга ритм синусовый, средняя частота сердечных сокращений составила 80 в минуту. За сутки было зарегистрировано 35 одиночных желудочковых экстрасистол и 3 одиночных наджелудочковых экстрасистолы. Сердечный ритм пациента включал 11 минут 45 секунд синусовой тахикардии с максимальной частотой сердечных сокращений 120 в минуту.
При рентгенографии органов грудной клетки 26.02.2019 (рис. 3) выявлялись признаки артериальной легочной гипертензии, признаки увеличения правых камер сердца, расширения легочной артерии.
Легочные поля были прозрачными. Отмечалось усиление легочного рисунка за счет сосудистого компонента в прикорневых отделах. Корни легких были структурны, расширены: нисходящая ветвь правой легочной артерии 28 мм (норма менее 16 мм), левая легочная артерия 34 мм (норма менее 24 мм). На тени сердца в прямой проекции выявлялось увеличение второй и четвертой дуги по левому контуру. Аорта была уплотнена. В первой (правой косой) проекции по переднему контуру выявлялось увеличение пульмонального конуса и дуги левого желудочка. Во второй (левой косой) проекции отмечалось незначительное увеличение дуг правого предсердия и дуги правого желудочка.
Пациенту был выставлен диагноз:
Первичная легочная гипертензия. Артериальная гипертензия 3 стадии риск 4.
Осложнение: Хроническая сердечная недостаточность 2 А стадии, функциональный класс 3.
Помимо аспирина (ацекардол 100 мг в 20:00), ингибиторов АПФ (престариум 2,5 мг в 8:00), бета-блокаторов (бисопролол 5 мг в 8:00), антагонистов кальция (лотонел 10 мг в 8:00), антагонистов минералокортикоидных рецепторов (верошпирон 100 мг в 14:00) к лечению были добавлены препараты для специфической терапии легочной артериальной гипертензии: силденафил кардио по 20 мг 2 раза в день и бозенекс 125 мг по ½ таблетки 2 раза в день с последующим увеличением дозировки до 125 мг 2 раза в сутки.
25% спорадических случаев первичной лёгочной гипертензии ассоциируется с мутацией гена BMPR2, обусловливающей нарушениеангиогенеза, сосудистой дифференциации, органогенеза легких и почек [1].
В патогенезе заболевания важное значение имеет эндотелиальная дисфункция. Она проявляется снижением образования оксида азота и простациклина – веществ, обладающих антипролиферативным и вазодилатирующим действием, и увеличением продукции тромбоксана А2 и эндотелина 1, обладающих вазоконстрикторным и пролиферативным действием [3]. Значительную роль играет редукция легочного сосудистого русла, снижение эластичности, облитерация легочных сосудов вследствие пролиферации гладкомышечных клеток, тромбоза in situ [1]: генетические изменения обусловливают усиление тенденции к тромбообразованию [2]. Все это приводит к повышению легочного сосудистого сопротивления, и, следовательно, увеличению нагрузки на правый желудочек [1], его гипертрофии, дилатации, развитию правожелудочковой сердечной недостаточности.
Симптомы первичной легочной гипертензии неспецифичны [2, 4]. Нашего пациента больше всего беспокоила инспираторная одышка при физической нагрузке. По данным литературы в начале заболевания эта жалоба является наиболее частой [1, 4]. Реже встречаются обмороки; давящие, ноющие, колющие боли в грудной клетке, длящиеся от нескольких минут до суток, усиливающиеся при физической нагрузке, не купирующиеся приемом нитратов [4]; перебои в работе сердца; кашель; кровохарканье [1].
При объективном исследовании больных обычно выявляют сердечный толчок, эпигастральную пульсацию, обусловленные гипертрофией или дилатацией правого желудочка, акцент второго тона над легочной артерией. Может выслушиваться систолический шум у основания мечевидного отростка грудины, обусловленный недостаточностью трехстворчатого клапана, диастолический шум над легочной артерией, связанный с регургитацией через клапан легочной артерии [1, 2]. При развитии правожелудочковой сердечной недостаточности появляются отеки, акроцианоз, набухание яремных вен, асцит [1, 2]. У больного А признаков правожелудочковой недостаточности не было, что свидетельствует о недавнем начале заболевания и своевременном назначении лечения.
Эритроцитоз и увеличение уровня гемоглобина, имевшие место у нашего пациента, объясняются компенсаторной реакцией на гипоксемию [1].
Для исключения других форм легочной гипертензии в план обследования помимо общего, биохимического анализов крови включают определение уровня гормонов щитовидной железы, серологические исследования для исключения системных заболеваний соедтинительной ткани, ВИЧ-инфекции, гепатита [5].
Перечень необходимых инструментальных методов исследования включает в себя ЭКГ, рентгенографию органов грудной клетки, эхокардиографию, катетеризацию правых камер сердца, которая выполняется для подтверждения диагноза, оценки тяжести гемодинамических изменений и проведения теста на вазореактивность сосудов легких [5].
При установлении диагноза первичной легочной гипертензии необходимо немедленное назначение специфической медикаментозной терапии. Для лечения легочной гипертензии применяются: антагонисты рецепторов эндотелина (амбризентан, бозентан); аналоги простациклина (илопрост, эпопростенол), агонисты его рецепторов (селексипаг); оксид азота, ингибиторы фосфодиэстеразы 5-го типа (силденафил), стимуляторы гуанилатциклазы (риоцигуат). Антагонисты кальция эффективны при положительном остром тесте на вазореактивность [5].
При тяжелой легочной гипертензии, неэффективности медикаментозной терапии выполняется балонная предсердная септостомия, билатеральная трансплантация легких или трансплантация комплекса сердце-легкие.
Прогноз у больных с первичной легочной гипертензией неблагоприятный. Выживаемость без специфической медикаментозной терапии в течение 1 года составляет 68%, 3 лет – 48%, 5 лет – 34% [4], а на фоне лечения выживаемость существенно выше: 90%, 75% и 65% соответственно [3].
Заключение
Первичная легочная гипертензия – редкое тяжелое заболевание с неблагоприятным прогнозом. Симптомы его неспецифичны, поэтому диагноз часто ставится не сразу. Своевременная диагностика и назначение специфической медикаментозной терапии позволяют значительно улучшить выживаемость больных.
Литература
1. Анализ случаев идиопатической лёгочной гипертензии по данным амурской областной клинической больницы / О. Н. Сивякова, В. В. Войцеховский, Е. С. Скрипкина [и др.] / Бюллетень физиологии и патологии дыхания. 2017. Вып. 64. С. 88 – 93
3. Клинический случай 10-летнего успешного применения амбризентана у пациентки с идиопатической легочной гипертензией / Т. В. Мартынюк [и др.] // Евразийский кардиологический журнал. 2015. № 4. С. 48 – 55
4. Стентирование межпредсердной перегородки при идиопатической лёгочной гипертензии / Б. Г. Алекян, С. В. Горбачевский, М. Г. Пурсанов [и др.]// Грудная и сердечно-сосудистая хирургия. 2015. № 5. С. 26 – 33
5. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension / Nazzareno Galiè [et al.] // European Heart Journal. 2016. Vol. 37, № 1. P. 67 – 119