Нейроэндокринные опухоли
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Что такое нейроэндокринные опухоли (НЭО)?
Основные локализации нейроэндокринных клеток:
щитовидная и паращитовидные железы, надпочечники.
Нейроэндокринные опухоли встречаются сравнительно редко и могут быть как злокачественными, так и доброкачественными. Чаще всего НЭО (устаревшее название – карциноиды) встречаются в следующих органах:
тонкая кишка, прямая кишка и аппендикс,
Нейроэндокринные опухоли делятся по следующим признакам:
Факторы риска появления НЭО
Чаще всего эти опухоли возникают спорадически – то есть случайно. Но есть и наследственные мутации, при наличии которых риск возникновения НЭО возрастает. Описаны несколько наследственных опухолевых синдромов, при которых повышен риск появления НЭО:
MEN 1 типа (multiple endocrine neoplasia – синдром множественных эндокринных неоплазий первого типа),
болезнь фон Гиппеля-Линдау,
Симптомы НЭО
Не всегда у пациентов с НЭО есть какие-либо симптомы. Кроме того, симптомы часто не специфичны – то есть встречаются и при других заболеваниях. На основе наличия или отсутствия симптомов НЭО принято разделять на функциональные (симптомные) и нефункциональные (бессимптомные). Функциональные опухоли усиленно вырабатывают гормоны, которые и становятся причиной появления симптомов.
Наиболее распространенные симптомы НЭО:
покраснение кожи лица и шеи,
повышенное артериальное давление,
Стадирование опухолевого процесса
Определение стадии играет ключевое значение, так как полностью определяет дальнейшее лечение. Как и при большинстве других опухолей, при НЭО принято выделять 4 стадии – от I до IV. При этом, кроме стадии, диагноз включает специальную кодировку – TNM, где:
T (tumor, опухоль) – описывает первичную опухоль,
N (nodes, лимфоузлы) – описывает распространение опухоли в лимфоузлы,
M (metastasis, метастазы) – описывает наличие или отсутствие метастазов.
Еще один параметр, описывающий нейроэндокринную опухоль – Grade. Он используется для описания способности опухоли к быстрому росту и распространению по организму и бывает 3 степеней:
G1 (low grade) – низкий темп роста и распространения,
G2 (intermediate grade) – промежуточный,
G3 (high grade) – высокий темп роста и распространения.
Обследование при подозрении НЭО
Сбор жалоб и анамнеза (истории болезни),
Анализ крови и мочи для выявления биохимических маркеров нейроэндокринной опухоли,
ПЭТ-КТ с галием (68Ga-DOTATATE и 68Ga-DOTANOC),
ПЭТ-КТ с глюкозой (ФДГ)
Сцинтиграфия с 111 In-Octreotide,
Особое место в диагностике занимает биопсия – забор фрагмента опухоли для точного определения ее типа. Биопсию возможно выполнить различными методами, например, при ФКС или ФГС. После биопсии фрагмент опухоли отправляется на гистологическое и иммуногистохимическое исследование (под микроскопом) для определения типа и агрессивности опухоли.
Какие из обследований будут использованы в Вашей ситуации будет определяться Вашим лечащим врачом. Часто при обследовании и планировании лечения необходимо получить консультацию у смежного специалиста, например, у кардиолога.
Лечение нейроэндокринных опухолей
Учитывая редкость НЭО и сложность постановки диагноза, перед началом лечения каждый пациент обсуждается мультидисциплинарной командой. В ее состав входят:
специалист лучевой диагностики,
при необходимости – дополнительные специалисты: кардиолог, анестезиолог и т.д.
В ходе разбора клинической ситуации каждого конкретного пациента вырабатывается коллегиальный индивидуальный план лечения, а при необходимости – дополнительного обследования.
Возможности лечения при НЭО:
терапия аналогами Соматостатина,
эмболизация при наличии метастазов в печени.
Часто лечение складывается из комбинации нескольких методов для достижения наиболее хорошего результата. Кроме того, бывают ситуации, когда одному пациенту подходят два варианта лечения с одинаковой эффективностью. Наилучший для Вас вариант лечения Вам расскажет лечащий врач по итогам работы мультидисциплинарной команды.
Лечение нейроэндокринных опухолей в Израиле
Содержание
Что такое нейроэндокринные опухоли
Нейроэндокринные опухоли — это злокачественные новообразования, первичный очаг которых базируется в органах эндокринной системы. Речь идет о железах, вырабатывающих гормоны — вещества, регулирующие деятельность организма.
Злокачественные нейроэндокринные опухоли выявляются приблизительно у 2% онкологических больных в Израиле. В стране ежегодно регистрируется около 350 новых случаев. Статистика заболеваний данной группы у мужчин и женщин одинаковая. Подобные опухоли могут развиться в любом возрасте.
По каким признакам классифицируются нейроэндокринные опухоли?
Нейроэндокринные опухоли характеризуются по двум главным признакам; они же и определяют тактику лечения. Первый фактор — орган, в котором образовалась опухоль; второй — показатель скорости деления клеток, так называемый KI 67.
Большинство нейроэндокринных опухолей берут свое начало в желудочно-кишечном тракте. Данные новообразования подразделяются на два типа, в зависимости от источника опухолевого процесса — в кишечнике или в поджелудочной железе. У немногих пациентов развитие заболевания ассоциируется с генными мутациями, такими как MEN1 и MEN2.
С чем связана проблематичность диагностики?
Раньше считалось, что речь идет о редком виде рака. Сейчас, ввиду совершенствования методов диагностики, число выявляемых ежегодно случаев нейроэндокринные опухолей возрастает. Симптомы болезни неспецифичны — это составляет определенную сложность для диагностики на ранней стадии. В этой связи часто диагноз ставится лишь тогда, когда уже идет активный процесс метастазирования, и полное излечение невозможно. Среди возможных проявлений — румянец, свистящие хрипы, кожная сыпь, понос, боли в животе и др.
Новые методы лечения нейроэндокринных опухолей
Основной метод лечения данного заболевания — хирургический.
В случае неоперабельной опухоли мы предлагаем другие варианты лечения, в том числе
Нейроэндокринные клетки, равно как и клетки нейроэндокринных опухолей, имеют рецепторы к соматостатину — гормону, в норме синтезирующемуся в организме и подавляющему выделение различных других гормонов.
В настоящее время существуют лекарства, являющиеся аналогами соматостатина. Речь идет о препаратах под названием Somatuline и Sandostatin. Данная медикаментозная терапия показана пациентам, которые не могут быть излечены путем операции и у которых показатель KI67 достаточно низкий. Терапия аналогами соматостатина показана приблизительно 70% пациентов с нейроэндокринными опухолями. Этим больным, у которых выявлена экспрессия рецепторов к соматостатину, в качестве первой линии может быть назначена терапия радиоактивным изотопом.
До последних лет основной целью терапии аналогами соматостатина считалось облегчение симптомов заболевания, обусловленных повышенной продукцией гомонов опухолями. Исследование PROMID было первым, которое продемонстрировало преимущество терапии аналогами соматостатина (Sandostatin).
Исследование CLARINET, материалы которого были представлены на конференции Американской ассоциации по изучению нейроэндокринных опухолей (ENET), показало следующее: терапия препаратом Somatuline тормозит дальнейшее развитие опухоли и, тем самым, дает пациентам дополнительный срок жизни без прогрессирования заболевания. Исследование проводилось в 14 медицинских центрах в разных странах в течение двух лет; в нем приняли участие 200 испытуемых с нейроэндокринными опухолями в ЖКТ и поджелудочной железе. По прошествии двух лет, более чем у половины испытуемых, получавших Somatuline, прогрессирования заболевания не было. Что же касается контрольной группы, получавшей плацебо, у половины испытуемых по прошествии 18 месяцев опухолевый процесс прогрессировал. Результаты исследования весьма обнадеживают: они доказывают, что сравнительно легкое лечение позволяет надолго отсрочить прогрессирование заболевания у пациентов с нейроэндокринными опухолями системы пищеварения.
Что означают результаты этих исследований?
Результаты исследований подтверждают информацию, которой мы располагаем, а именно, что на сегодняшний день благодаря существующим препаратам больные с нейроэндокринными опухолями могут рассчитывать на многие годы полноценной жизни. Огромное значение имеет ранняя диагностика и немедленное предоставление адекватного лечения, учитывающего общее состояние больного и специфические параметры опухоли. Своевременно принятые меры помогут сохранить приемлемое качество жизни на годы, превратить скоротечный недуг в хроническое вялотекущее заболевание.
Обратиться в отдел медицинского туризма больницы Ихилов можно несколькими способами: отправив заявку на почту medtour@tlvmc.gov.il или оставить заявку на официальном сайте больницы Ихилов. После получения заявки врачи больницы проведут ревизию результатов диагностических исследований, проведенных на родине, и в течении 24, максимум 48 часов, дадут ответ, можем ли мы помочь пациенту в условиях пандемии и предоставят предварительный прайс-лист, чтобы заранее понимать стоимость обследования/лечения.
Это позволяет избежать ненужных проверок по приезде, а также существенно экономит время и деньги пациента, прибывшего на лечение.
Особенности диагностики нейроэндокринных опухолей
Нейроэндокринные опухоли (НЭО) — это гетерогенная группа новообразований, развивающихся из нейроэндокринных клеток. Такие клетки расположены в различных органах и секретируют биологически активные вещества, эффекты которых обуславливают многообразие клинической картины и трудности диагностики. Прежде чем попасть на прием к онкологу, пациентам зачастую бывают проведены консультации различных специалистов, обращение к которым вызвано симптоматикой новообразования. Ранняя диагностика НЭО в значительной мере зависит от онконастороженности непрофильных клиницистов и, конечно же, от морфологической верификации диагноза — «золотого правила» в онкологии, своеобразной точки отсчета онкологической истории.
Локализация НЭО крайне разнообразна, но чаще всего они обнаруживаются в органах пищеварительной системы (более 50 %): прямая (17,2 %) и тонкая кишка (13,4 %), желудок (6,0 %), поджелудочная железа (6–7 %). НЭО занимают второе место в общей структуре онкологической патологии ЖКТ, уступая лидерские позиции лишь колоректальному раку. Около 27 % случаев НЭО возникают в легких (согласно базе данных Surveillance, Epidemiology, and End Results (SEER) 1975-2016) [1].
Еще недавно обсуждались вопросы включения НЭО в список орфанных заболеваний. Но в настоящее время отмечается увеличение частоты встречаемости этой патологии, в том числе из-за улучшения диагностических возможностей (в частности, распространение гастроскопии, колоноскопии, капсульной эндоскопии).
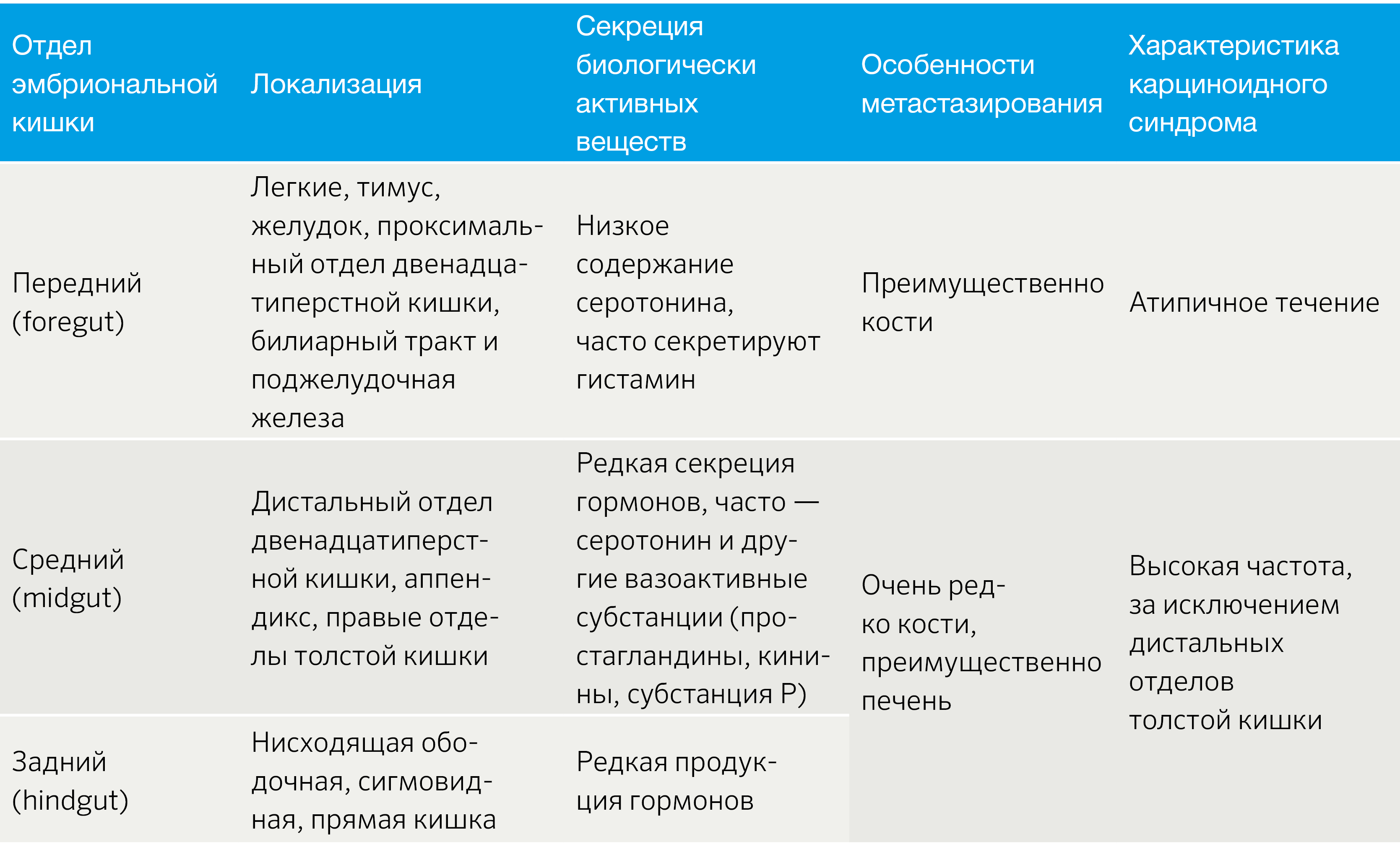
НЭО классифицируют в зависимости от отдела эмбриональной кишечной трубки: из передней, средней и задней кишки (табл. 1) [2].
Табл.1 | Классификация НЭО по эмбриогенезу [2].
Карциноидный синдром — важный клинический признак. В основном, он обусловлен эффектами серотонина, а также брадикинина, гистамина, дофамина и в меньшей степени других биологически активных веществ (БАВ).
Клинические проявления карциноидного синдрома разнообразны. Наиболее часто у пациентов отмечается гиперемия кожи лица, приливы, диарея, боль в животе. У 60 % пациентов отмечают формирование карциноидной болезни сердца, с нарушением работы преимущественно клапанного аппарата правых отделов (стеноз и/или недостаточность легочного и трехстворчатого клапанов). Серьезным осложнением является декомпенсация нарастающей сердечной недостаточности. Морфологическим субстратом служит выраженный диффузный фиброэластоз эндокарда. Возможны появления телеангиоэктазий, одышки, пеллагры, бронхоспазма. Усиливается продукция соединительнотканных компонентов, в частности, коллагена. Это ведет к фиброзированию и стенозу брыжеечных артерий, фиброзирующему стенозу уретры. Ввиду склонности к развитию спаечного процесса в брюшной полости нарастает риск формирования кишечной непроходимости.
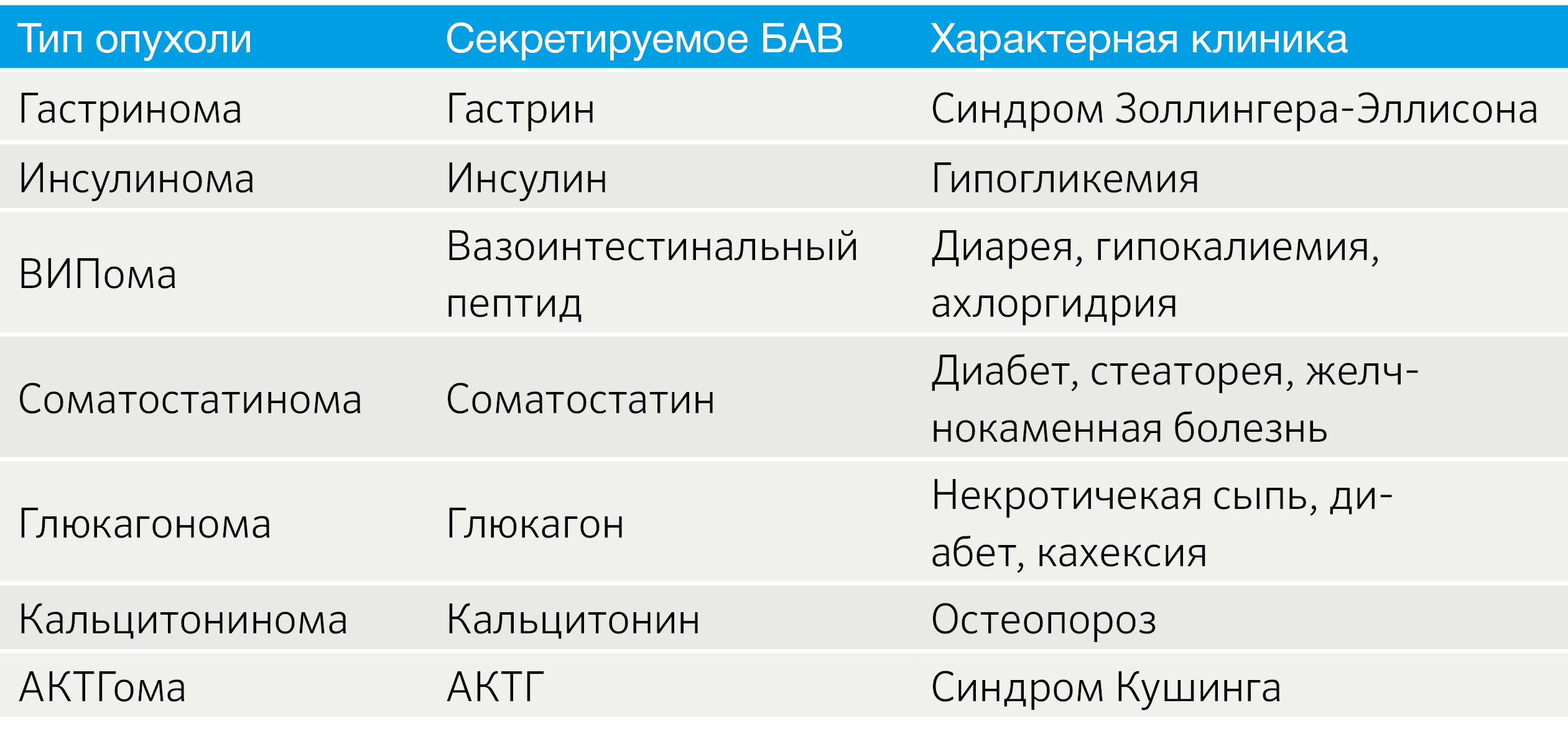
Важным аспектом является функциональный статус опухоли. В зависимости от наличия продукции БАВ выделяют функционирующие (табл. 2) и нефункционирующие новообразования [3].
Табл.2 | Функционирующие НЭО [3].
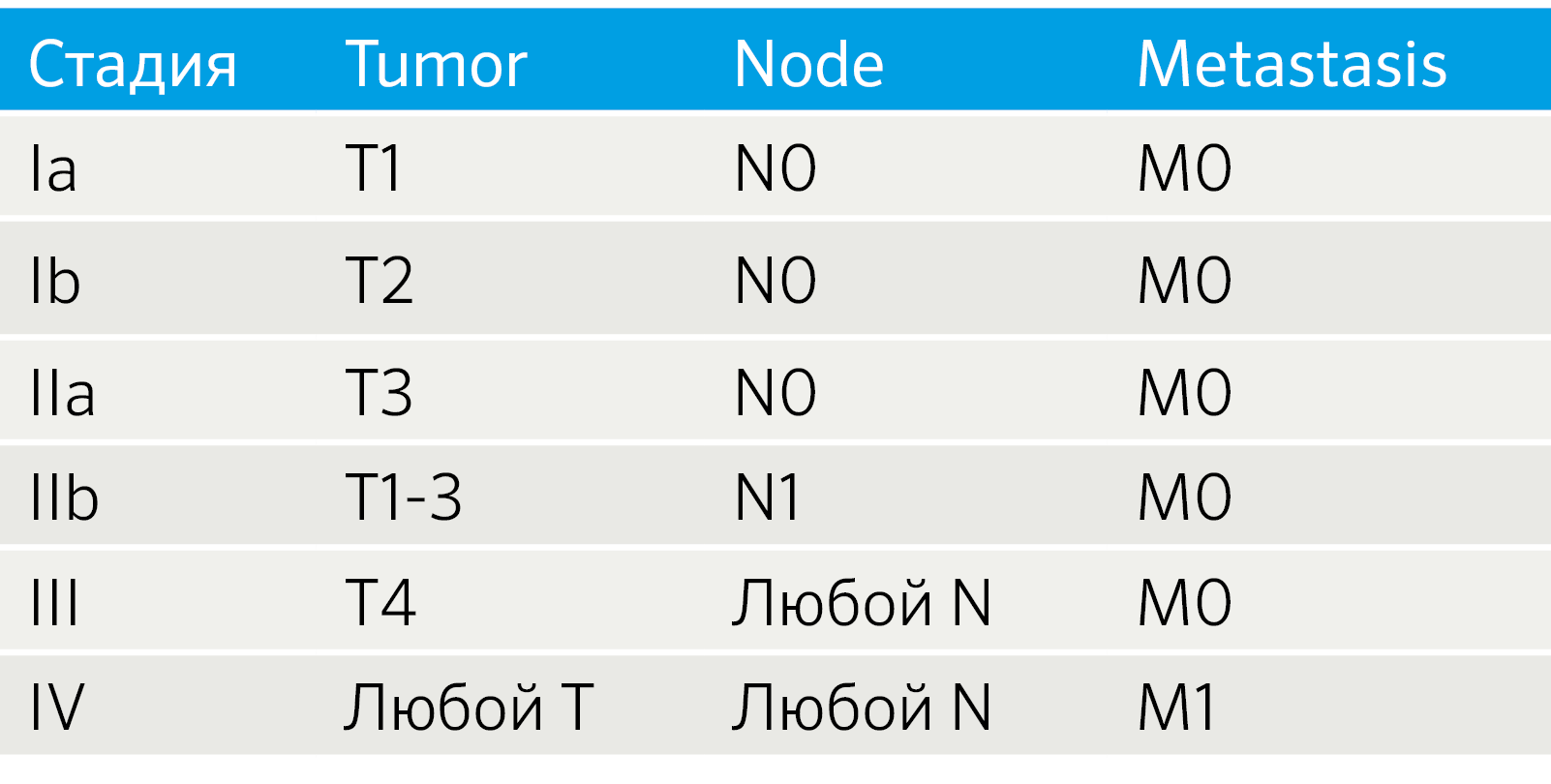
Особенности TNM-классификации определяются локализацией НЭО. НЭО легких стадируются как немелкоклеточный рак легких, для НЭО ЖКТ и поджелудочной железы разработаны рекомендации Европейского общества по изучению НЭО (ENETS) [4]. Также установление стадии TNM для всех анатомических локализаций регламентируется руководством, созданным Американским объединенным комитетом по раковым заболеваниям (the American Joint Committee on Cancer, AJCC) [5, 6]. Так как эти системы не идентичны, возникают вопросы унификации подходов к стадированию. Например, была создана модифицированная система ENETS (mENETS), для диагностики НЭО поджелудочной железы (pNET) (табл. 3) [7].
Табл.3 | Стадирование НЭО поджелудочной железы согласно модифицированной системе ENETS (mENETS) [7].
И вот мы подходим к той черепахе, на которой стоят киты онкологической диагностики. Это, несомненно, гистологическая верификация диагноза. Как и многие опухолевые заболевания, морфологические градации НЭО подвергались различным модификациям, уточнениям, дополнениям. Дискуссии в этой области в итоге привели к созданию 4-ой редакции классификации ВОЗ (2017 год) [8]. Именно она является актуальной на настоящий момент и заключение при проведении патологоанатомическом исследовании должно отвечать введенным в ней понятиям и требованиям.
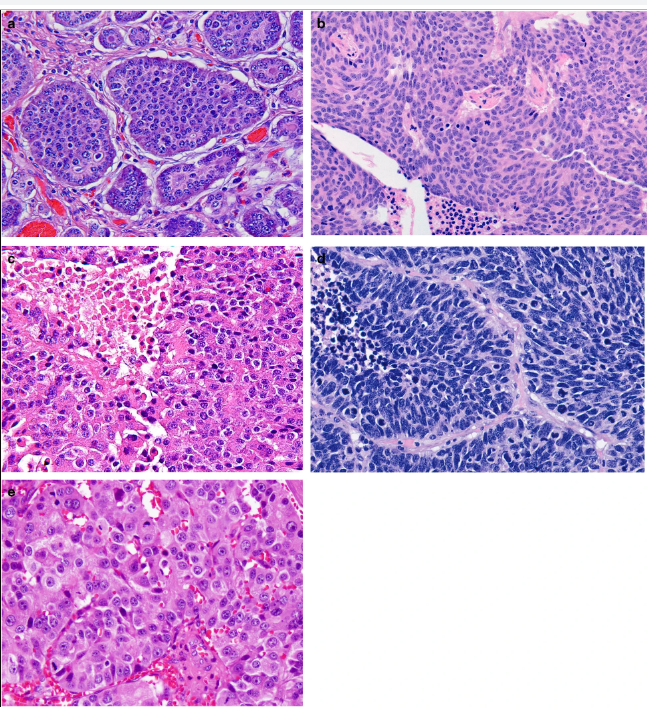
Параметрами морфологической оценки нейроэндокринных новообразований являются: гистологическое строение опухоли, определение сосудистой и периневральной инвазии, митотический индекс. Несмотря на многообразия источников НЭО, морфологическая картина является сходной (рис. 1) [9].
Нейроэндокринное происхождение атипичных клеток доказывает положительная экспрессия так называемых общих нейроэндокринных маркеров. Основные из них это хромогранин А, окрашивающий компоненты нейросекреторных гранул, и пептид синаптофизин, накапливающийся в мелких синаптических везикулах. Также применяется дополнительно установление экспрессии рецепторов соматостатина 2 и 5 типов (SSTR2 и SSTR5). В этом случае возможно определить чувствительность опухолевых клеток к аналогам соматостатина.
Степень злокачественности НЭО определяют на основании двух основных критериев: уровня дифференцированности опухолевых клеток и их пролиферативной активности. Традиционно выделяют три степени злокачественности (grade): G1, G2, G3. Для НЭО ЖКТ и поджелудочной железы введены понятия высокодифференцированных и низкодифференцированных новообразований (или нейроэндокринного рака (карциномы), НЭР). Высокодифференцированные НЭО объединяют G1 (менее 2 митозов на 10 репрезентативных полей зрения (РПЗ) при большом увеличении микроскопа (х400) и индекс Ki-67 ≤ 2%), G2 (2–20 митозов на 10 РПЗ и индекс Ki-67 3–20 %), G3 (> 20 митозов на 10 РПЗ и индекс Ki-67 > 20 %). Grade 3 опухоли разделяют на мелко- и крупноклеточный рак. Опухоли мелкоклеточного типа построены из однотипных клеток округлой, овальной или вытянутой формы, мелкого размера, со скудной цитоплазмой и нечеткими границами. Ядра имеют характерный вид за счет нежного хроматина и невизуализирующихся ядрышек. Определяются массивные некрозы. Крупноклеточные НЭР образованы, соответственно, клетками крупного или среднего размера, с низким ядерно-цитоплазматическим соотношением, выраженной атипией ядер, содержащих гранулярный хроматин и четкие ядрышки. В опухолевой ткани выявляются мультифокальные некрозы, значительное число митозов [8, 9].
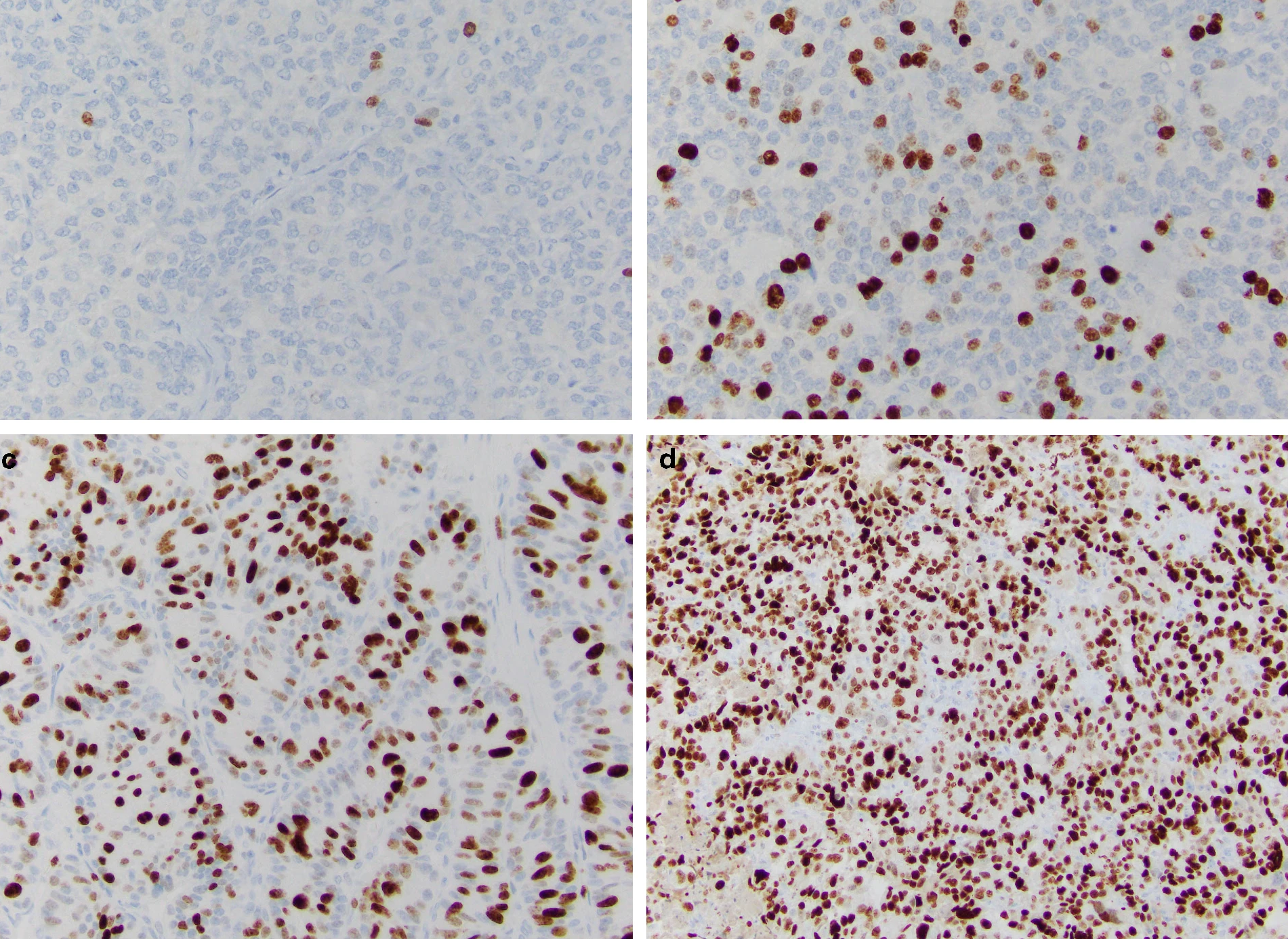
Индекс Ki-67 определяют как средний процент окрашенных ядер при учете 500–2000 злокачественно трансформированных клеток (рис. 2) [9].
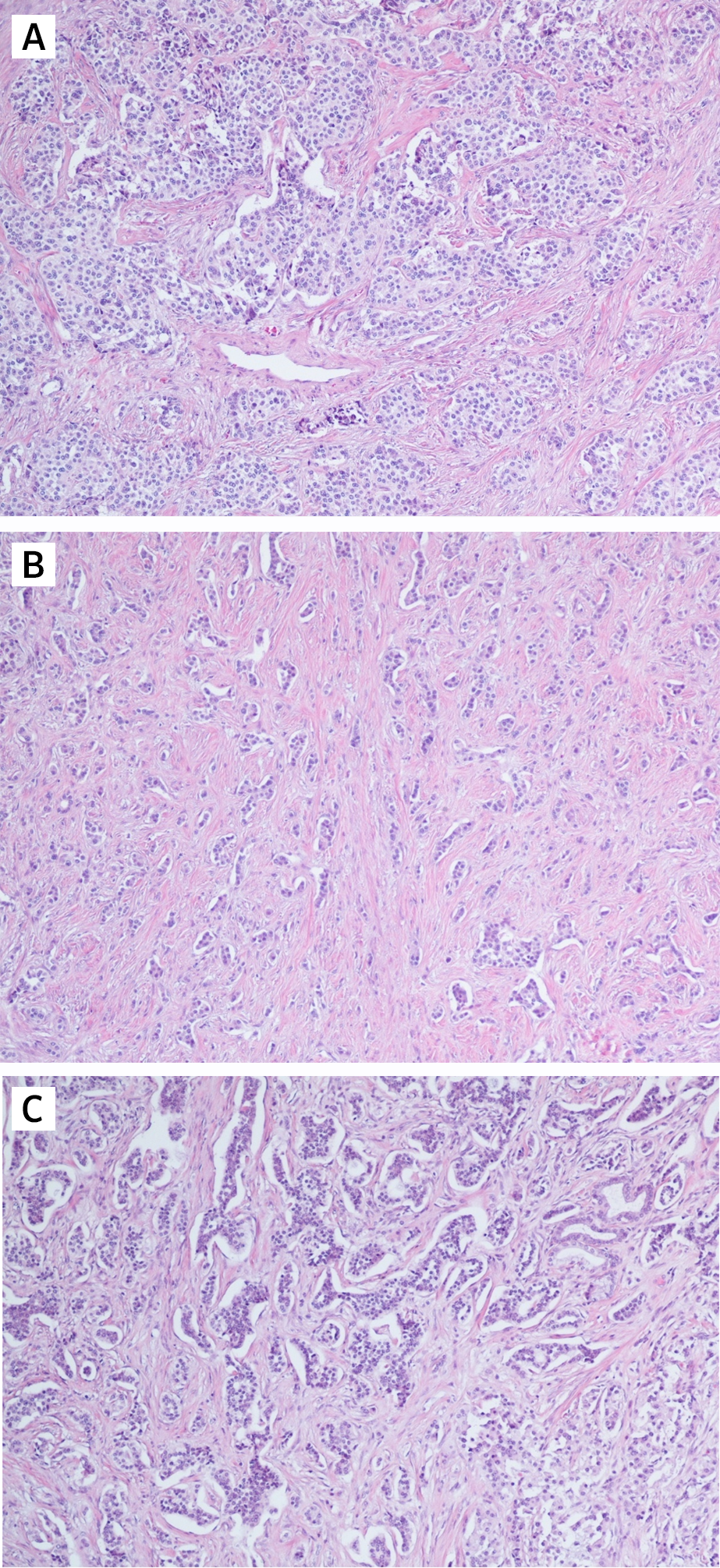
Рассмотрим различия понятий НЭО G3 и НЭР при локализации в поджелудочной железе. Несмотря на высокую степень злокачественности НЭО G3 гистологически имеют органоидную модель строения (рис. 3), отсутствие некрозов [10]. При иммуногистохимическом исследовании опухолевая ткань сохраняет экспрессию общих маркеров нейроэндокринной дифференцировки (диффузно и интенсивно определяется экспрессия синаптофизина, зачастую хромогранина А), а также панкреатические экзокринные или эктопические гормоны. Кроме того, в них отсутствует выраженная экспрессия p53 и утрата экспрессии RB (также определяются иммуногистохимически).
НЭР поджелудочной железы — это опухоли низкой степени дифференцировки и соответственно высокой степени злокачественности. Экспрессия общих маркеров нейроэндокринной дифференцировки атипичными клетками снижается: синаптофизин определяется слабо или диффузно, хромогранин А также слабо или фокально. Экзокринные гормоны отрицательны в таких опухолях [9]. Часто определяется экспрессия р53, белков ремоделирования хроматина DAXX (death-associated protein 6) и ATRX (АТФ-зависимая хеликаза), потеря экспрессии RB (белок ретинобластомы) и ISL1 (энхансер гена инсулина 1) [11].
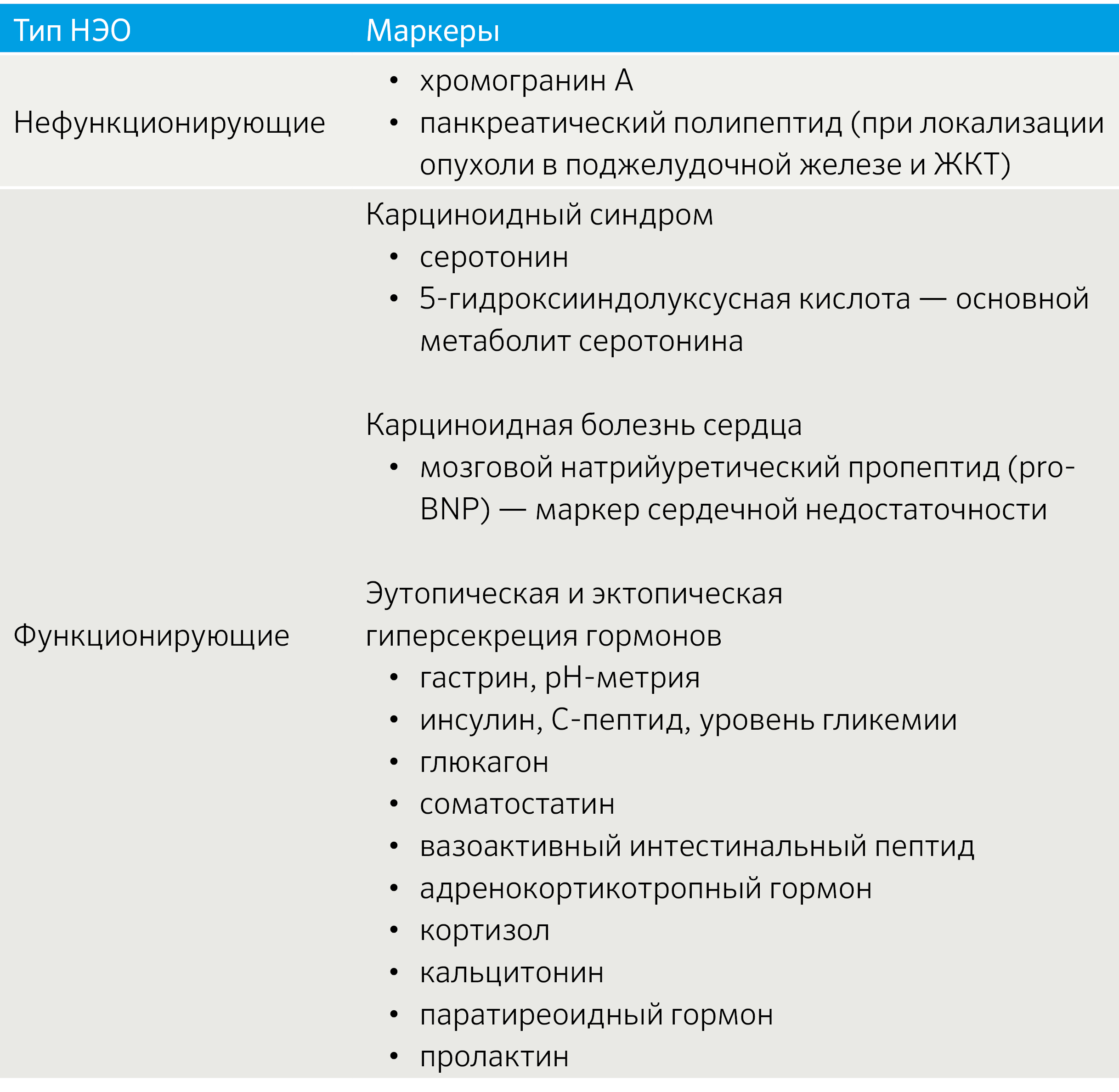
Ввиду многообразия секретирующего профиля НЭО биохимическая диагностика включает различные маркеры, комбинируемые с учетом клинической картины (табл. 4).
Табл. 4 | Спектр биохимических маркеров НЭО [2].
Методы лучевой диагностики включают «классические» КТ и МРТ с контрастированием. Для оценки метастатического поражения печени возможно проведение УЗИ органов брюшной полости.
Радионуклидная диагностика играет важную роль в топической характеристике НЭО. Она включает методы специфической метаболической визуализации ( 123 I-MIBG), рецепторной визуализации ( 111 In-октреотид, 68 Ga-DOTA-TOС/DOTA-NOC/DOTA-TATE) и неспецифической метаболической визуализации ( 18 F-FDG, 18 F-DOPA).
123 I-метайодбензилгуанидин (MIBG) является аналогом норадреналина (норэпинефрина). Он накапливается в адренергических тканях и опухолях, происходящих из них. Сцинтиграфия с 123 I-MIBG используется для диагностики нейробластомы, феохромоцитомы, параганглиомы, карциноидов бронха и тонкой кишки [12].
Для рецепторной визуализации применяют 111 In (индий)-октеотид. Он выявляет высокодифференцированные нейроэндокринные опухоли, опухоли из клеток островкового аппарата поджелудочной железы (гастринома, глюкагонома, инсулинома). Также для верификации НЭО ЖКТ применяется соматостатин-рецепторная сцинтиграфия, так как большинство из них имеют рецепторы к соматостатину (SSTR) на поверхности опухолевых клеток (чаще 2 и 5 типа).
Выбор радионуклидного метода связан со степенью дифференцировки опухолевых клеток. Первичная диагностика НЭО Grade 1 и 2 проводится путем ПЭТ/КТ с радиофармпрепаратами (РФП), мечеными галлием 68 (является ПЭТ-радионуклидом). Сродство (аффинитет) РФП к конкретному подтипу трансмембранных рецепторов соматостатина определяет выбор диагностического индикатора (ПЭТ-лиганда, представленного различными модификациями DOTA). Например, для визуализации НЭО, экспрессирующих рецепторы подтипов SSTR2a и SSTR2b, применяют 68 Ga-DOTA-TATE (DOTA-Tyr3-октреотад). 68 Ga-DOTA-NOC (DOTA-1-Nal3-октреотид) выявляет подтипы SSTR3 и SSTR5, 68 Ga-DOTA-ТOC (DOTA-Tyr3-октреотид) — рецепторы SSTR5 [13].
При отсутствии возможности проведения данного исследования следует выполнить однофотонную эмиссионную компьютерную томографию (ОФЭКТ)/КТ (гибридный метод визуализации) с соматостатин-рецепторным радиофармпрепаратом.
Для недифференцированных НЭО Grade 3 и НЭР при отрицательных результатах соматостатин-рецепторной сцинтиграфии рекомендуется ПЭТ неспецифическая метаболическая визуализация с использованием других РФП. В частности, ПЭТ/КТ c 18F-фтордезоксиглюкозой (18F-ФДГ), которая неэффективна при высокодифференцированных НЭО [14]. Также рассматривают применение 18F-L–DOPA (дигидроксифенил-аланин) — меченого предшественника допамина, который эффективен для обнаружения медуллярного рака щитовидной железы, НЭО, параганглиомы и феохромоцитомы [15].
Современные классификации НЭО в значительной мере основаны на общей морфологии, которую эти новообразования демонстрируют в различных анатомических участках. Закономерно предположить, что такая структурная схожесть является результатом общей «нейроэндокринной» мультигенной программы, стимулирующей дифференцировку нейроэндокринных клеток. Но схожесть не означает идентичность, и несомненно существующая тканеспецифичность нейроэндокринных клеток диктует характерною индивидуальную гормональную продукцию. Профиль экспрессии БАВ атипичными клетками определяет клиническую картину и прогноз заболевания. Поэтому важно иметь возможность точно определяет источник опухоли. С использованием все расширяющихся диагностических возможностей такой подход становится реальным, формируя персонализацию терапевтических стратегий в нейроэндокринной онкологии.
Терапия нейроэндокринных опухолей
ЗАБОЛЕВАЕМОСТЬ
Клинико-патогенетическая характеристика основных НЭО
| Тип опухоли | Секретируемые гормоны или амины | Клиническая симптоматика |
| Карциноид | Серотонин | Карциноидный синдром: приливы, диарея, бронхоспазм, гипертензия, поражение сердца. |
| Гастринома | Гастрин | Синдром Золлингера-Эллисона, тяжелые пептические язвы |
| ВИПома | Вазоинтестинальный полипептид | Тяжелая диарея («панкреатическая холера», синдром Вернера-Моррисона) |
| Инсулинома | Инсулин | Гипогликемия |
| Глюкагонома | Глюкагон | Диабет, мигрирующая некротическая эритема, раздражение и покраснение языка |
| Соматостатинома | Соматостатин | Дисфункция желчного пузыря, ЖКБ, нарушенная толерантность к глюкозе |
КАРЦИНОИД
Одна из наиболее часто встречающихся опухолей диффузной нейроэндокринной системы!
Опухоль секретирует:
Это приводит к развитию карциноидного синдрома.
КАРЦИНОИДНЫЙ СИНДРОМ
Проявления:
Синдром обусловлен развитием фиброзных изменений в эндо- и миокарде правых отделов сердца с поражением клапанов.
Характерны стеноз и недостаточность трехстворчатого клапана и клапана легочной артерии.
КАРЦИНОИДНЫЙ КРИЗ
КЛАССИФИКАЦИЯ НЭО (ВОЗ, 2002 г.)
Характеристика высокодифференцированных НЭО
К ним относятся различные карциноиды передней, средней и задней кишки, феохромоцитома, медуллярный рак щитовидной железы.
Характеристика низкодифференцированных НЭО
К ним относится мелкоклеточный рак легкого и других органов.
Характеристика смешанных экзокринных и эндокринных карцином
КЛАССИФИКАЦИЯ КАРЦИНОИДНЫХ ОПУХОЛЕЙ (ВИЛЬЯМС И САНДЛЕР, 1963)
Классификация в зависимости от наличия или отсутствия карциноидного синдрома
ЛАБОРАТОРНАЯ ДИАГНОСТИКА
ИНСТРУМЕНТАЛЬНАЯ ДИАГНОСТИКА
Рентгенологические методы
Эндоскопические методы
Ультразвуковые методы
Спиральная КТ с контрастным усилением и МРТ
РАДИОИЗОТОПНАЯ ДИАГНОСТИКА
НЭО на поверхности клеток имеют рецепторы, обладающие высоким сродством к гормону соматостатину. В 87% случаев они присутствуют как в первичной опухоли, так и в метастазах. В связи с этим в последние годы для определения локализации опухоли и метастазов используется радиоизотопный метод с меченным 111 In Октреотидом. Введенный внутривенно Октреотид, 111 In через 24-48 ч. определяется на соматостатиновых рецепторах и позволяет визуализировать соматостатинпозитивную опухоль, а также определить возможность применения аналогов соматостатина для лечения.
Метод с применением Октреотида, 111 In обладает чувствительностью 87%, специфичностью 75% и частотой совпадения диагнозов 87%.
Лечение
Хирургическое лечение
Основной метод лечения НЭО – хирургический. Возможные варианты оперативного вмешательства определяют по локализации опухоли, наличию или отсутствию метастазов и осложнений опухолевого процесса. Однако контроль симптомов при хирургическом лечении достигается не всегда!
Немедикаментозное лечение
Контроль за проявлениями карциноидного синдрома: исключение стрессов, алкоголя, соблюдение диеты.
Медикаментозное лечение
Биотерапия:
Химиотерапия:
Комбинированная химиотерапия:
Симптоматическая терапия:
Механизм действия ОКТРЕОТИДА-ДЕПО
При карциноидных опухолях применение Октреотида-депо может приводить к уменьшению выраженности симптомов заболевания, в первую очередь, таких как приливы и диарея. Во многих случаях клиническое улучшение сопровождается снижением концентрации серотонина в плазме и экскреции 5-гидроксииндолуксусной кислоты с мочой.
При опухолях, характеризующихся гиперпродукцией вазоактивного интестинального пептида (ВИПомы), применение Октреотида-депо приводит у большинства больных к уменьшению тяжелой секреторной диареи, которая характерна для данного состояния, что, в свою очередь, приводит к улучшению качества жизни больного. Одновременно происходит уменьшение сопутствующих нарушений электролитного баланса, например, гипокалиемии, что позволяет отменить энтеральное и парентеральное введение жидкости и электролитов. По данным компьютерной томографии у некоторых больных происходит замедление или остановка прогрессирования опухоли, и даже уменьшение ее размеров, особенно метастазов в печень. Клиническое улучшение обычно сопровождается уменьшением (вплоть до нормальных значений) концентрации вазоактивного интестинального пептида (ВИП) в плазме.
При глюкагономах применение Октреотида-депо в большинстве случаев приводит к заметному уменьшению некротизирующей мигрирующей сыпи, которая характерна для данного состояния. У больных, страдающих диареей, Октреотид-депо вызывает ее уменьшение, что сопровождается повышением массы тела. При применении Октреотида-депо часто отмечается быстрое снижение концентрации глюкагона в плазме, однако при длительном лечении этот эффект не сохраняется. В то же время симптоматическое улучшение остается стабильным длительное время.
При гастриномах/синдроме Золлингера-Эллисона Октреотид-депо, применяемый в качестве монотерапии или в комбинации с блокаторами H2-рецепторов и ингибиторами протонного насоса, может снизить образование соляной кислоты в желудке и привести к клиническому улучшению, в т.ч. и в отношении диареи. Возможно также уменьшение выраженности и других симптомов, вероятно связанных с синтезом пептидов опухолью, в т.ч. приливов. В некоторых случаях отмечается снижение концентрации гастрина в плазме.
У больных с инсулиномами Октреотид-депо уменьшает уровень иммунореактивного инсулина в крови. У больных с операбельными опухолями Октреотид-депо может обеспечить восстановление и поддержание нормогликемии в предоперационном периоде. У больных с неоперабельными доброкачественными и злокачественными опухолями контроль гликемии может улучшаться и без одновременного продолжительного снижения уровня инсулина в крови.
У больных с редко встречающимися опухолями, гиперпродуцирующими рилизинг-фактор гормона роста (соматолибериномами), Октреотид-депо уменьшает выраженность симптомов акромегалии. Это, по-видимому, связано с подавлением секреции рилизинг-фактора гормона роста и самого гормона роста. В дальнейшем возможно уменьшение размеров гипофиза, которые до начала лечения были увеличены.
Обнаружено, что применение Октреотида-депо в дозах 30 мг и выше оказывает антипролиферативный эффект, связанный с прямым цитотоксическим действием препарата на опухоль при взаимодействии с соматостатиновыми рецепторами, а также с угнетением образования сосудов, питающих опухоль.
Режим дозирования
При эндокринных опухолях ЖКТ и поджелудочной железы для больных, у которых подкожное введение Октреотида обеспечивает адекватный контроль проявлений заболевания, рекомендуемая начальная доза Октреотида-депо составляет 20 мг каждые 4 недели.
Подкожное введение Октреотида следует продолжать еще в течение 2 недель после первого введения Октреотида-депо.
Для больных, не получавших ранее Октреотид подкожно, рекомендуется начинать лечение именно с подкожного введения Октреотида в дозе 0.1 мг 3 раза/сут. в течение относительно короткого периода времени (примерно 2 недели) с целью оценки его эффективности и общей переносимости. Только после этого назначают Октреотид-депо по вышеприведенной схеме.
В случае, когда терапия Октреотидом-депо в течение 3 мес. обеспечивает адекватный контроль клинических проявлений и биологических маркеров заболевания, возможно снизить дозу Октреотида-депо до 10 мг, назначаемых каждые 4 недели.
В тех случаях, когда после 3 мес. лечения Октреотидом-депо удалось достичь лишь частичного улучшения, дозу препарата можно увеличить до 30 мг каждые 4 недели.
На фоне лечения Октреотидом-депо в отдельные дни возможно усиление клинических проявлений, характерных для эндокринных опухолей ЖКТ и поджелудочной железы. В этих случаях рекомендуется дополнительное подкожное введение Октреотида в дозе, применявшейся до начала лечения Октреотидом-депо. Это может происходить, главным образом, в первые 2 мес. лечения.
Октреотид-депо – препарат первой линии для монотерапии или комбинированной терапии высокодифференцированных нейроэндокринных опухолей ЖКТ и поджелудочной железы, эффективно купирующий гормональные синдромы за счет подавления гиперсекреции гормонов этими опухолями, повышая качество жизни и выживаемость больных.