Питание при химиотерапии
10.11.21 Время на чтение: 20 минут
Содержание статьи
Современная медицина развивается с огромной скоростью, постоянно совершенствуя методы борьбы с онкологическими заболеваниями. Так, в 2018 году в США было одобрено рекордное количество препаратов против рака – 59. А Нобелевская премия того же года была вручена за новую модальность иммуноонкологии.
В России на борьбу с онкологическими заболеваниями направлена Национальная программа «Онкология», в рамках которой большое внимание уделяется ранней диагностике рака и повышению качества жизни онкопациентов, что существенно облегчает борьбу с недугом.
Важным элементом лечения онкологических пациентов является нутритивная терапия: проблемы с питанием являются одной из самых распространённых трудностей, сопровождающих возникновение и лечение раковых заболеваний, а также восстановление после них. По данным Европейского общества парентерального и энтерального питания, частота недостаточности питания у онкологических больных колеблется от 46 до 88%. Нутритивная (белково-энергетическая) недостаточность может стать даже причиной смерти.
Одним из ведущих методов борьбы с онкологическими заболеваниями является химиотерапия. Этот системный метод лечения основывается на введении в организм сильнодействующих токсических препаратов, которые уничтожают злокачественные опухоли или останавливают их развитие. К сожалению, такое лечение отражается и на здоровых клетках, например, пациент может временно лишиться волос или испытывать проблемы с пищеварением.
Химиотерапия сложно переносится организмом и может вызывать тяжёлые последствия. Так, она меняет вкус и обоняние: привычная, даже любимая еда, может вызвать у пациента отвращение, а её запах – рвотные позывы. Повреждённые слизистые делают очень сложным процесс пережёвывания и проглатывания пищи. Становятся часты запоры. К тому же часть препаратов, которое принимает больной, может подавлять чувство голода. Из-за всего этого человек начинает мало есть, и у него может возникнуть анорексия. В этом случае нутритивная терапия становится одним из методов лечения: она обеспечивает организм необходимыми питательными веществами, помогая сохранить силы и жизнеспособность даже в самых тяжёлых состояниях.
Это важно!
Нутритивная поддержка для онкологических больных важна, потому что она:
Нутритивная поддержка онкологических пациентов
Описываются проблемы нарушения питания, их причины и классификация у онкологических пациентов. Нутритивная недостаточность является фактором повышенного риска в период лечения онкологических больных. Рассматриваются способы коррекции нутритивного статуса,
Problems of nutrition disorders, their reasons and classification in oncologic patients are described. Nutritive insufficiency is an increased risk factor during oncologic patients treatment. Ways of nutritive status correction are considered, in particular, use of special nutrition.
Кроме современных методов диагностики и лечения онкологический больной нуждается в специальной организации лечебного питания. Опухоль-индуцированная потеря веса имеется у 30–70% больных. Она снижает эффективность лечения, увеличивает токсичность противоопухолевой терапии, удлиняет время пребывания пациента в больнице и снижает его выживаемость, существенно влияет на его качество жизни и физическую активность. Лечением опухоль-индуцированной потери веса врачи часто пренебрегают, при этом не каждый пациент может скорректировать свою диету. Серьезной проблемой при развитии онкологических заболеваний является тот факт, что и сама болезнь, и используемые для ее лечения методы вызывают анорексию. Кроме того, и наличие опухоли, и проводимое противоопухолевое лечение могут приводить к нарушению усвоения ряда питательных веществ [1–3].
Причины опухолевой кахексии:
Развившаяся кахексия приводит к белково-энергетической недостаточности. Происходит потеря массы тела, истощение соматических и висцеральных белковых запасов с повреждением ферментативных и структурных функций. Дефицит белка снижает гуморальный и клеточный иммунитет, что способствует увеличению частоты осложнений, развитию вторичных инфекций. Увеличивается смертность пациентов. Наличие кахексии ограничивает возможности химиотерапии.
Нутритивный статус можно оценивать по уровню сывороточного альбумина, уровень его менее 2,2 г/дл отражает тяжелое нарушение питания [4]. В клинической практике критериями значимой белково-энергетической недостаточности у онкологических пациентов можно считать потерю веса более чем на 10%, снижение альбумина менее 35 г/л и трансферрина менее 1,9 г/л.
При наличии двух из трех критериев больному необходима активная нутритивная поддержка.
Принципиально важным вопросом является выбор метода питания.
Способы энтерального питания:
В случае неэффективности энтерального питания или при наличии противопоказаний показано полное парентеральное питание.
Для сохранения положительного азотистого баланса и жировых запасов небелковые калории должны на 130% превышать уровень основного обмена. Согласно рекомендациям ESPEN суточные потребности пациента в белке составляют 1–1,5 г/кг, а энергии — 20–25 ккал/кг для пациентов, находящихся на постельном режиме, и 30–35 ккал/кг для пациентов, проходящих амбулаторное лечение.
Специализированное питание обладает определенными преимуществами перед обычной диетой.
При выборе специализированного лечебного питания необходимо ориентироваться не только на потребности пациента в белке и энергии, но и на проводимое противоопухолевое лечение и состояние ЖКТ (например, наличие мукозита или нарушений стула).
Пациенту, который готовится к операции, особенно по поводу опухоли желудочно-кишечного тракта, например опухоли толстой кишки, необходимо специализированное питание с повышенным содержанием белка. Одним из примеров специализированного питания является Нутридринк Компакт Протеин, который содержит самое большое количество белка в малом объеме (18 г белка в бутылочке 125 мл)*, что важно для пациентов с потерей веса и сил, с отеками, тех, кому трудно выпить большой объем жидкости. Нутридринк Компакт Протеин может быть рекомендован для питания пациентов в послеоперационном периоде, например, при операциях по поводу опухолей головы и шеи или желудочно-кишечного тракта, а также с период реабилитации после операции.
Особенности состава продукта Фортикер (соотношение омега-6 и омега-3 жирных кислот) могут снизить выраженность такого неприятного явления, как мукозиты, т. к. полиненасыщенные жирные кислоты группы омега-3 обеспечивают противовоспалительный и иммуномодулирующий эффект. Кроме того, продукт Фортикер является предпочтительным при диарее и запорах, т. к. содержит комплекс пищевых волокон, способных уменьшить выраженность этих явлений [5].
Какое бы специализированное питание не было назначено, важно следовать условиям его употребления.
Таким образом, использование специализированного питания может быть рекомендовано как в период лечения, так и после выписки пациента из стационара. Преемственность рационального лечебного питания на этапах стационарного и амбулаторного лечения, сбалансированного по пищевой и энергетической ценности, в соответствии со стадией и активностью заболевания, является важным компонентом процесса лечебных мероприятий. Ежедневное использование специализированного питания позволит минимизировать, а во многих случаях и предупредить развитие нежелательных явлений на фоне проводимой противоопухолевой терапии.
Литература
ГБОУ ВПО КемГМА МЗ РФ, Кемерово
* Среди линейки продукции «Нутриция Эдванс».
Ключевые принципы и технологии нутритивной поддержки в паллиативной медицине
Клиническое питание в паллиативной помощи – это особая концепция нутритивной поддержки, учитывающая гидробаланс, энергобаланс, корректные показания и противопоказания и качество жизни пациента. Лечебное питание назначается пациентам для поддержания гидро- и электробаланса, увеличения мышечной массы. Исследования доказывают, что правильно подобранный режим нутритивной поддержки способен увеличить продолжительность жизни пациента.
По данным ВОЗ дефицит массы тела более 30% может рассматриваться как причина летального исхода. Однако на практике в истории болезни врачи редко указывают кахексию, потому что это вызывает вопросы – «как больной получал лечение, что у него появилась кахексия?».
Нужно помнить, что кахексия входит в Международную классификацию болезней 10 издания (МКБ-10), и врачи обязаны указывать ее в истории болезни. Другими показаниями определения голодания как причины смерти может быть потеря жировых запасов (70%), потеря мышечной массы (более 30%), низкий индекс массы тела (11-13).
Оценка нутритивного статуса
Кому необходимо проводить нутритивную поддержку? Какие могут быть показания? Разработано множество различных инструментов (ESMO 2008, MUST и т.д.). Скрининговая шкала NRS-2002 используется среди больных инсультом. Она проста в использовании, ее заполнение занимает около двух минут. Если больной набирает три балла по этой шкале, необходимо ставить вопрос о проведении нутритивной поддержки. Если больной не набирает необходимое число баллов – его можно кормить теми способами, что и ранее. При этом нужно проводит скрининг каждую неделю.
Чтобы оценить нутритивный статус, в первую очередь необходимо взять у больного общий анализ крови и узнать точный индекс массы тела. Общий анализ крови позволяет любому врачу увидеть количество лимфоцитов, общий белок, альбумин.
Обратите внимание, что у онкологических больных фактическая масса тела зачастую ни о чем не говорит – имеет значение вес, который человек потерял за последние несколько месяцев. И если пациент говорит вам, что при росте 180 см он весит 85 килограммов, это еще не значит, что у него нет питательной недостаточности. Особенно если он похудел на 10-12 килограммов за три месяца – это высокий темп потери массы тела. Также всегда нужно учитывать функцию желудочно-кишечного тракта пациента.
Критерии питательной недостаточности:
Энтеральное питание – ключевая технология
Энтеральное питание – это ключевая технология, которую должны использовать врачи. На практике применяется три варианта организации такого питания: методика обогащения энтеральными диетами обычных продуктов, сиппинг, зондовое питание. Сиппинг – технология перорального приема энтеральных смесей, которое позволяет для больного избежать зондирования, что является значимым шагом в улучшении качества жизни. Разумеется, сейчас используются разные зонды, и некоторые из них могут стоять даже по 30 суток без замены. Разработаны и тонкие зонды, которые не вызывают раздражения у пациента в отличие от зондов старого поколения.
Начинать энтеральное питание рекомендуется с обогащения диеты. Пациенты принимают обычную пищу, сочетая ее с питательными смесями в небольших количествах. То есть мы понимаем, что пациент принимает недостаточное количество белка, но ему сложно съедать килограмм мяса каждый день. Поэтому каши, йогурты, творог, картофельное пюре обогащаются смесями. Технология обогащения питания удобна и абсолютно реализуема практически. Я рекомендую изучить книгу «Рецептура обогащения» о том, как наполнить белком и энергией не только сладкие продукты, но и суп, гарниры и разного рода блюда.
При назначении энтеральных смесей пациентам нужно учесть несколько важных нюансов. Все эти бутылочки со смесями только выглядят красиво.
Первое, что нужно сказать пациенту при назначении «дринков», – это невкусно. Если врач об этом не говорит, на четвертые сутки треть больных от них отказываются. Только написано, что они имеют клубничный или банановый вкус, а на самом деле вкус у них очень специфический, лекарственный.
И это, в общем-то, закон жизни: полезное – невкусное. Но если вы предупреждаете об этом пациента, он будет относиться к «дринкам» как к микстуре от кашля – «да, невкусно, но надо, потому что это помогает».
Другой очень важный момент, о котором нужно сказать пациентам, – нельзя выпивать эти бутылочки со смесями залпом, как мы привыкли пить сок или чай. Иначе естественная реакция – это тошнота, чувство переполнения. В 200м л очень плотной смеси содержится очень много белка, энергии и электролитов, поэтому 1-2 бутылочки нужно постепенно выпивать в течение дня.
Другой важный совет, который может дать врач пациенту: если вы чувствуете снижение аппетита, запивайте таблетки 2-3 глотками питательной смеси, чтобы повысить общий объем потребления. А также у пациента должны быть рекомендации для потребления продуктов в граммах с разъяснением того, сколько именно этого продукта нужно съесть. Вроде бы сказать это пациенту несложно, но, как показывает практика, это очень удобно для больного. Длительность курса приема энтеральных смесей составляет от 7 дней до 21 дня.
У паллиативных пациентов, как правило, энтеральное питание начинается с установления зонда. Однако необходимо помнить, что чем дольше стоит зонд у пациента, тем больше со временем у него появится проблем, связанных не только с ухудшением качеством жизни, но и с осложнениями от зонда. Во-первых, у пациента с установленным зондом возрастает риск развития синусита из-за высокой частоты контаминации околоносовых пазух. Синусит возникает из-за отсутствия естественной аэрации носоглотки при наличии интубационной или трахеостомической трубки, затрудненной эвакуации секрета из пазух и по причине преимущественно горизонтального положения тела.
Помимо синусита, нужно помнить о риске возникновения пролежней, язв и пищеводных свищей, поэтому специалистам нужно вовремя поставить вопрос о гастроскопии, особенно если у больного зонд стоит больше четырех недель.
Сегодня гастростомия стала более доступна, потому что появились технологии чрескожных эндоскопических гастростом (еюностомия). Устанавливает гастростому хирург-эндоскопист при местной анестезии в процедурном кабинете или в палате интенсивной терапии. Установка занимает от пяти до семи минут, и больного можно кормить через нее уже на следующие сутки. Такая чрескожная эндоскопическая гастростома может стоять у пациента несколько лет. С ней меньше риска развития мацерации кожи, а также подтекания содержимого из трубки.
Однако для установления чрескожной гастростомической трубки имеются противопоказания: перитонит, сепсис, язвенная болезнь желудка и ДПК, выраженная кровоточивость, выраженный асцит, анатомические дефекты после предшествующей операции или воспаления.
Удобна гастростомическая трубка еще и тем, что она быстро приживается: за неделю у пациента формируется чрескожный канал. Никаких специальных перевязок не требуется. Уход осуществляется обычным жидким мылом или специальным лосьоном. Ни в коем случае нельзя использовать в уходе за гастростомой и кожей вокруг нее йод, зеленку, вазелин, детские крема. Акцентируйте на этом внимание родственников и всегда выдавайте им памятку о том, как за ней ухаживать, как промывать, как вводить пищу и каким образом трубку проворачивать.
Уход за пациентом после установления гастростомы:
Важно помнить, что пациента нельзя кормить продуктами неясного происхождения и качества. Медперсонал и осуществляющие уход за пациентом люди должны понимать, сколько человек потребляет белка, сколько в питании витаминов, микроэлементов, какая у него калорийность. Я рекомендую кормить пациентов специальными смесями с высоким содержанием пищевых волокон, поскольку они уменьшают риск возникновения диареи различного генеза.
Вводя пребиотики, вы удерживаете нормальный баланс флоры в толстой кишке. Это имеет значение для паллиативных больных, для онкобольных, которые проходят курс радио- или химиотерапии, для неврологических больных, у которых в организме нет запаса пребиотиков.
Парентеральное питание – вспомогательная технология
Парентеральное питание используется только в тех случаях, когда у пациента не работает желудочно-кишечный тракт, и его нутритивный статус и гидробаланс невозможно поддерживать с помощью различных методов энтерального питания.
На качество жизни пациента, которому показан такой тип питания, влияют очень разные нюансы, в том числе тип проведенной операции. К примеру, радикальная хирургия иногда заканчивается жесточайшим демпинг-синдромом, когда после любого приема пищи больной покрывается холодным липким потом, и через месяц у него формируется стереотип, что прием пищи вызывает у него проблемы – тошноту, тахикардию, что сопровождается потерей массы тела. Хотя у человека радикально убрана опухоль, и причина симптоматики именно в этом.
Инкурабельным пациентам нередко показано домашнее парентеральное питание. Этой технологии я учился в Праге, где, несмотря на скромное состояние экономики, программы домашнего парентерального питания полностью оплачиваются государством и подписываются государственным советом по медицине. Реализация этой программы для Чехии крайне важна: паллиативные пациенты получают возможность находиться дома рядом со своими близкими, кроме того, парентеральное питание снижает риск смерти пациента от голодания, что обычно происходит при невозможности адекватного энтерального питания.
Исследования, проведенные у инкурабельных больных с обструктивной опухолью, показывают, что выживаемость без парентерального питания составляет около 19 суток при нахождении больного дома. При нахождении в стационаре выживаемость достигает 90 суток, что соответствует сроку жизни (2,5 месяца) здорового человека при полном голодании.
Выживаемость больных на домашнем парентеральном питании с опухолевой обструкцией колеблется от 90 до 180 суток. Это абсолютно реальные цифры, которые озвучены международными медицинскими сообществами.
Критерии включения в программу домашнего парентерального питания могут быть следующие:
Противопоказаниями считаются Индекс Карновского ≤ 50 и ECOG ≥ 3.
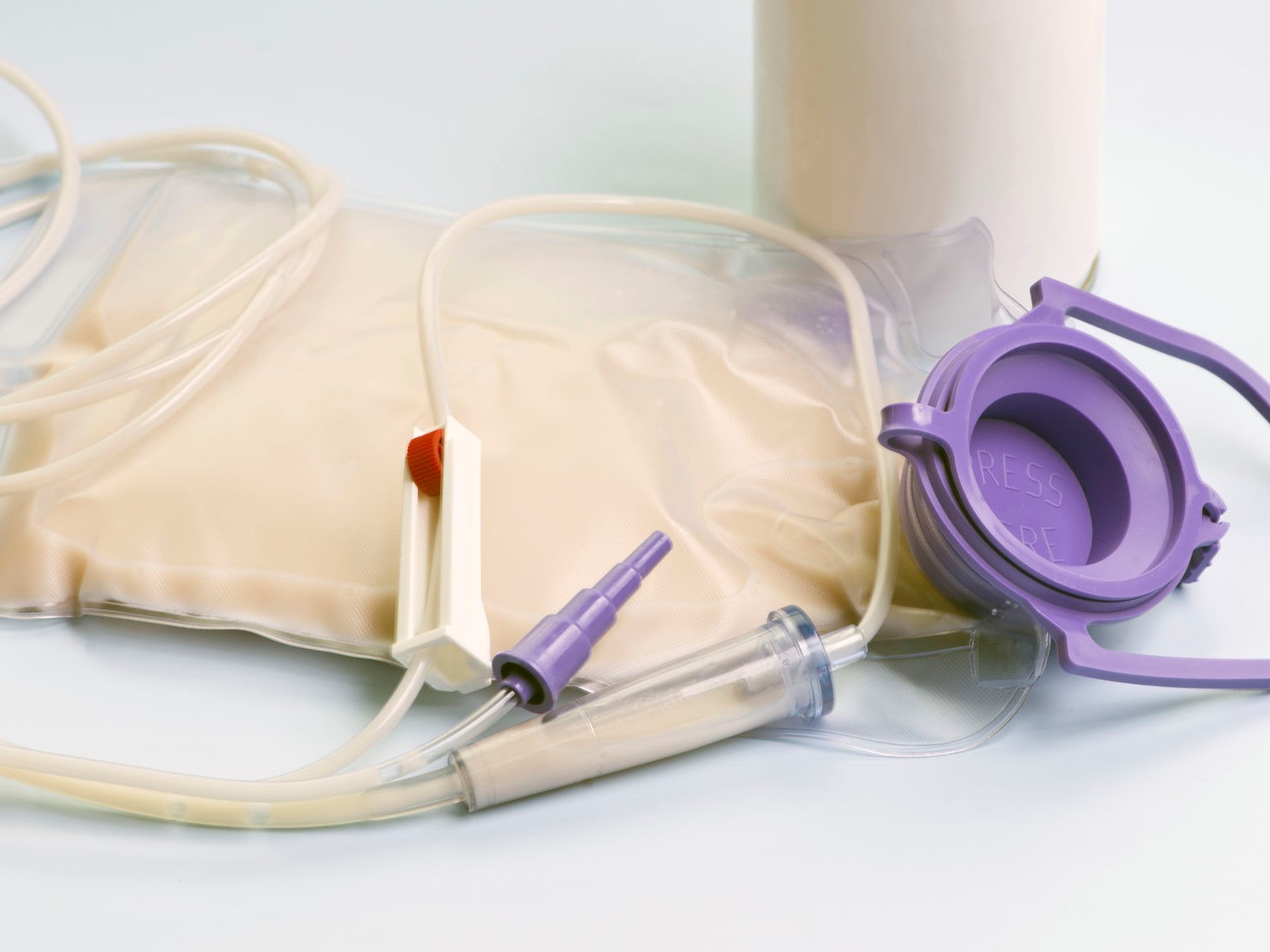
С 2005 года для домашнего парентерального питания используются специальные мешки, с помощью которых пациент и ухаживающие за ним люди могут отслеживать, сколько жидкости в систему ввели, какой калорийности питание, сколько в нем белка и электролитов. В отличие бутылочных систем, которые применялись ранее, мешки сохраняют свою стерильность не сутки, а двое суток. Однако нужно внимательно следить за стерильностью не только мешка, но и всей системы парентерального питания, поэтому в укладку обязательно должны входить антисептики и салфетки для ухода за венозным доступом.
С такой системой питания пациенту и его близким удобно осуществлять уход – катетер выходит из подкожного тоннеля в области большой грудной мышцы. Кроме того, это позволяет человеку без особых усилий принимать душ. Почему это важно? Потому что паллиативная помощь – это не только об эффективном контроле за болевым синдромом, снятии тяжелых симптомов и качественной нутритивной поддержке, но и о поддержании качества жизни пациента, поэтому крайне важно использовать наиболее удобные для пациента технологии.
Материал подготовлен по итогам выступления И.Н. Лейдермана на Конференции с международным участием « Развитие паллиативной помощи детям и взрослым ».
Нутритивная поддержка онкологических пациентов
Значимость питания в жизни пациента
Питание важно для здорового функционирования организма человека. И в особенности для онкологических пациентов.
На любом этапе комплексного лечения онкологических заболеваний – от диагностики заболевания до этапа реабилитации – необходимо уделять должное внимание тому, чем и как питается пациент. Питание – это важный показатель качества жизни пациента.
Качество жизни пациента – это интегральная характеристика. Она включает в себя его физическое, психологическое и социальное функционирование.
Цель врача не просто вылечить человека, но и сохранить социальную адаптацию и психологическое благополучие, чтобы пациент мог себя максимально комфортно чувствовать в период лечения и после него.
Нутритивная недостаточность и риск ее возникновения
Важно, чтобы пациент и врач понимали, о чем они говорят друг другу. Поэтому ознакомимся с некоторыми терминами.
Нутритивный статус – комплекс клинических, антропометрических и лабораторных показателей, характеризующих количественное соотношение мышечной и жировой массы человека.
Также важным понятием является нутритивная или питательная недостаточность. Это состояние, которое обусловлено несоответствием между поступлением питательных веществ в организм и их расходом, что приводит к снижению массы тела и изменению компонентного состава организма.
Риск развития нутритивной недостаточности у онкологических пациентов высок. Он зависит от локализации опухоли и стадии процесса.
Причины нутритивной недостаточности
1. Снижение потребления пищи.
Оно может быть связано как с проявлениями самого заболевания (затруднения при проглатывании пищи, тошнота, рвота), так и с осознанным ограничением потребления пищи пациентом.
2. Нарушение усвоения питательных веществ.
Часто это связано с органическими и структурными изменениями органов ЖКТ.
3. Потеря питательных веществ.
Это может происходить на фоне рвоты или диареи в связи с основным заболеванием или в результате лечения.
4. Нарушения метаболизма (обмена веществ).
Нарушение метаболизма на фоне онкологического заболевания может быть связано с недостатком определенных питательных веществ, например, витаминов. Они участвуют во многих биологических реакциях организма. Если происходит нарушение всасывания или поступления витаминов в организм, нарушается обмен веществ в целом.
5. Психологический стресс.
Во-первых, на фоне стресса может снижаться аппетит, и, как следствие, снижаться количество потребляемой пищи. Замыкается порочный круг. Во-вторых, в организме могут запускаться механизмы, которые ускоряют распад питательных веществ.
Медицинский скрининг нутритивной недостаточности
Специалистам в контроле динамики и состояния нутритивного статуса пациента помогают следующие методы:
1. Контроль массы тела.
Контроль массы тела – задача не только врача, но и самого пациента. Необходимо следить за своим весом, питанием и обращать внимание на происходящие изменения.
2. Клинический и биохимический анализы крови.
По данным анализа крови (например, по уровню белка, альбумина в крови, по количеству лимфоцитов) врачи могут отслеживать и фиксировать наличие и динамику нутритивной недостаточности у пациента.
3. Биоимпедансметрия.
Это один из инструментальных методов в арсенале врачей. Он основан на изучении количественного соотношения мышечной и жировой массы тела, оценке их соотношения в динамике. В его основе лежат физические законы различной электропроводимости тканей организма.
4. Компьютерная томография.
Используется также для оценки количества мышечной и жировой массы тела. Она выполняется каждому пациенту на этапе постановки диагноза и при дальнейшем лечении.
Скрининг нутритивной недостаточности: самостоятельный тест
Пациент может самостоятельно осуществить скрининг нутритивной недостаточности.
Для этого нужно ответить на три простых вопроса:
Если за 3 вопроса в сумме набралось более 2х баллов, то пациенту необходимо проведение нутриционной поддержки.
Необходимо своевременно выявлять пациентов из группы риска нарушения питательного статуса. Это позволяет защитить их от прогрессирующей потери массы тела и развития связанных с этим осложнений.
Скрининг и мониторинг недостаточности питания должны проводиться на протяжении всего лечения, что важно для оценки динамики нутритивного статуса онкологических пациентов.
Профилактика саркопении
Саркопения – понятие, которое тесно связано с нарушением питательного статуса.
Саркопения – изменение скелетной мускулатуры, приводящее к постепенной потере мышечной массы тела и снижению функции мышц. Обычно такое состояние обусловлено возвратными изменениями метаболических процессов, нарушением питания и усиленным мышечным катаболизмом (расщеплением питательных веществ).
Помочь в профилактике саркопениии могут следующие методы:
Если говорить о конкретных показателях, то можно обратить внимание на следующие элементы и придерживаться указанных значений:
Синдром анорексии-кахексии
Следующее важное понятие – синдром анорексии-кахексии. Это многофакторный синдром, характеризующийся потерей массы тела, анорексией (в том числе снижением или отсутствием аппетита) и различными метаболическими нарушениями (усиленный распад питательных веществ, распад белков в мышцах, синдром хронического воспаления).
Выделяют 3 степени этого синдрома: прекахексия, кахексия и рефрактерная кахексия.
Синдром анорексии-кахексии тесно связан с общим самочувствием пациента. При нарастании явлений синдрома анорексии-кахексии ухудшается общее самочувствие пациента, что влечет за собой невозможность продолжения специализированного противоопухолевого лечения.
В широком смысле кахексия не равняется потере массы тела. Потеря массы тела – это только часть, одно из звеньев, которое приводит к ее развитию.
Раковая кахексия — это:
Нутритивная поддержка как вид сопроводительной терапии
Нутритивная поддержка – это лечебное питание, цель которого обеспечить организм всеми необходимыми питательными веществами с помощью питательных смесей. Это оптимизирует процессы метаболизма, а также увеличивает резервы организма.
Цели и задачи нутритивной поддержки:
Методы нутритивной поддержки:
Сипинговое питание
Энтеральное питание (сипинг) — питание, физиологичное для организма. Применяется обычно в дополнение к обычному рациону пациента. Это пероральный прием питательной смеси через трубочку маленькими глотками.
Следует соблюдать простые правила относительно сипинга: пить необходимо строго через трубочку (чтобы глоток был небольшим) и пить медленно (примерно в течение 30 минут). При этом предпочтительно использовать специализированные смеси, содержащие максимальное количество питательных веществ в минимальном объеме.
Особое внимание следует обращать на количество в смеси белка – строительного материала для восстановления организма, повышения его сопротивляемости. При развитии нутритивной недостаточности в первую очередь усиливается распад именно белков, нарушается их синтез в организме.
Смеси для сипинга имеют различные вкусовые особенности, и часто пациенты могут индивидуально выбирать тот вкус, который им нравится.
Зондовое питание
Еще один из методов нутритивной поддержки – зондовое питание. Оно представляет собой энтеральное питание. Такое питание осуществляется посредством постановки зонда в желудок или тонкий кишечник.
При невозможности постановки зонда необходимо формирование гастро- или энтеростомы, при которых питание поступает непосредственно в соответствующий орган.
Данный подход применим в трех случаях: когда пациенты не могут, не хотят или не должны получать питание перорально (через рот).
Парентеральное питание
Парентеральное питание предполагает использование смесей, которые специально разработаны для их введения в периферические или центральные вены.
Показания к применению такого метода:
Кому нужна нутритивная поддержка?
К принципам нутритивной поддержки принято относить следующие:
Важно, чтобы этапы оценки нутритивного статуса пациента, разработка плана питательной поддержки пациента совпадали с диагностикой и лечением основного заболевания. Тем самым можно добиться увеличения эффективности обоих методов.
Абсолютными показаниями к назначению активной нутритивной поддержки являются:
Начало и продолжительность нутритивной поддежки
Период, когда назначается нутритивная поддержка:
Продолжительность проведения нутритивной поддержки:
Критерии продолжительности нутритивной поддержки или показатели того, что она может быть завершена:
Лишний вес и нутритивная поддержка
Очень важным вопросом является оценка того, нуждаются ли пациенты с повышенной массой тела в нутритивной поддержке.
Нормальная или повышенная масса тела не означает того, что у пациента не имеется признаков саркопении (снижения объема мышечной массы).
При нарастающей потере массы тела в первую очередь уменьшается не жировая ткань, а теряется именно мышечная ткань. Это ведет к потере белка и развитию различных осложнений. Данный процесс не зависит от исходной массы тела человека.
Кроме того, во многих исследованиях доказано, что наличие саркопенического ожирения (сочетание уменьшения мышечной массы тела с повышенной жировой массой) также неблагоприятно сказывается на прогнозе заболевания, т.к. ухудшает переносимость противоопухолевого лечения.
Развитие опухоли и нутритивная поддержка
Еще один часто задаваемый вопрос от пациентов: влияет ли проведение нутритивной поддержки на рост и распространение опухоли?
В настоящее время данных, подтвержденных какими-либо научными исследованиями, которые говорили бы о воздействии нутритивного («искусственного») питания на рост опухоли у пациентов, нет.
Нормальные неизмененные клетки организма (точно также, как и злокачественные) нуждаются в питательных веществах, чтобы лучше функционировать, чтобы иметь возможность сопротивляться активному противоопухолевому лечению.
Жесткое ограничение в питательных веществах и каких-либо продуктах не только не поможет в лечении, но и может нанести вред.
Рекомендации нутритивной поддержки от russco
Рекомендации по проведению нутритивной поддержки являются неотъемлемой частью многих руководств по лечению различных заболеваний, в том числе и онкологических.
Так, в руководстве российского общества клинической онкологии RUSSCO даны четкие указания по поводу проведения нутритивной поддержки:
Что нужно знать о нутритивной поддержке?
Подходит ли спортивное питание для пациентов?
Некоторые пациенты интересуются возможностью использования питания для спортсменов, поскольку оно содержит много питательных веществ.
Спортивное питание рассчитано на спортсменов, которые получают повышенную физическую нагрузку. В таком питании очень высоки дозы всех питательных веществ, не только витаминов. Это питание создано из расчета на то, что человек будет испытывать большую физическую нагрузку.
Пациенты, как правило, в период лечения в спортивный зал не ходят, поэтому все-таки лучше обратиться к медицинскому питанию. Оно более сбалансировано и рассчитано на потребности именно пациентов, которые на данный момент получают лечение.
Рекомендации по лечебному питанию должен давать онколог. Также есть и другие специалисты – диетологи и нутрициологи, которые могут помочь с подбором питания. Кроме того, можно также проконсультироваться с гастроэнтерологом, который учтет имеющиеся гастроэнтерологические проблемы, связанные с нарушением питания.
Лечебное голодание и лечение опухоли
Бытует мнение, что при онкологических заболеваниях полезно лечебное голодание, чтобы не «кормить» опухоль.
Специалисты с этим категорически не согласны. Опухоль, которая имеется в организме, получает только часть питательных веществ, которые поступают в организм. При голодании организму не хватает сил, строительного материала для быстрого и успешного восстановления после химиотерапии, лучевой терапии или хирургического лечения. Поэтому ограничений в рационе быть не должно.
Конечно, этот вопрос должен решаться индивидуально: многие пациенты имеют сопутствующую патологию. В этом случае врач должен подобрать определенную диету. Но целенаправленно ограничивать себя в употреблении белка, рыбы, молочных и других продуктов и не стоит. Весь организм, кроме злокачественной опухоли, настроен на борьбу с заболеванием и нуждается в питательных веществах.
В организме ежесекундно образуются опухолевые клетки – клетки, над которыми организм теряет контроль – у кого-то они эффективно уничтожаются, у кого-то активно делятся. Наивно думать, что ограничение употребления белка приведет к гибели опухоли. При голодании организм запускает альтернативный синтез и начинает «брать» белок из здоровых тканей. В таком случае в теле человека происходят необратимые процессы, что приводит к ограничению использования современных методов противоопухолевого лечения.
Можно ли оценить недостаточность питания только по индексу массы тела?
Недостаточность питания также оценивается по ИМТ. Индекс массы тела – это соотношение веса к росту в квадрате. Но у онкологических больных ИМТ не является однозначным показателем для оценки нутритивного статуса.
Для оценки состояния нутритивного гомеостаза у пациента нужно оценивать все в комплексе: и клинические данные, и жалобы пациента на потерю массы тела, и показатели клинического и биохимического анализов крови, а также рассчитывать соотношение мышечной и жировой массы тела по компьютерной томографии и биоимпедансметрии.
Следует обращать большое внимание на стабильность массы тела. О любом снижении массы тела пациент должен сообщить лечащему врачу. Очень важно учитывать за какой период и сколько килограммов было потеряно.
Когда нет необходимости в нутритивной поддержке?
Нутритивная поддержка нужна не всем пациентам.
Питание должно быть полноценным и в процессе лечения, и в период реабилитации, и на протяжении всей жизни. Рацион должен стать гармоничным.
Витаминные комплексы и нутритивную поддержку (лечебное, специальное питание) должен назначать только лечащий врач. Существует целая линейка такого питания, и специалист выбирает именно то, что необходимо для поддержки и лечения конкретному пациенту.
Роль обычных продуктов питания при лечении онкологических заболеваний
Не существует каких-либо общих рекомендаций по рациону онкологических пациентов.
На основании исследований, в том числе зарубежных, врачи приходят к выводу, что «ненужных» продуктов как таковых не существует. Например, нет обоснованных запретов относительно употребления сахара.
Что касается белка, то он должен присутствовать в рационе – как растительный, так и животный. Некоторое отклонение в вегетарианство на фоне достаточно тяжелого и сложного лечения врачами не очень приветствуется, так как этим резко ограничивается разнообразие рациона пациентов.
В лечении онкологического заболевания важна стабильность. В том числе и в питании. Не стоит резко переходить на другой тип питания (например, вегетарианство, если вы всегда если мясо), или садиться на любую другую диету. Это ‒ стресс для организма.