Нарушения циркадного ритма
Нарушения циркадного ритма — один из вариантов инсомнии, при котором происходит рассогласование между внутренним циклом сон-бодрствование и внешним циклом день-ночь. Состояние развивается при смене часовых поясов (джетлаг), посменном и вахтовом графике работы, неврологических заболеваниях. Расстройства суточных ритмов вызывают психоэмоциональные нарушения, снижают работоспособность, повышают риск эндокринных и кардиологических проблем. Диагностика включает детальный сбор анамнеза, полисомнографию, нейровизуализацию. Для лечения применяются препараты (мелатонин, снотворные средства), немедикаментозная коррекция режима отдыха.
МКБ-10
Общие сведения
Сбои физиологических циркадных ритмов — одна из наиболее распространенных проблем в современной неврологии, с различными проявлениями которой периодически сталкивается каждый человек. Состояние имеет большую актуальность ввиду отсутствия эффективных медикаментозных методов коррекции, выраженного негативного влияния на самочувствие и соматическое здоровье больных. Несмотря на усовершенствование тактики лечения, многие люди продолжают страдать от сомнологических циркадных расстройств.
Причины
Изменения циклов сна могут иметь физиологические предпосылки: в подростковом возрасте обычно наблюдается более позднее засыпание, которое не совпадает с предписанными нормами, а в старческом возрасте, наоборот, люди ложатся спать слишком рано, а затем просыпаются среди ночи и больше не могут уснуть. К патологическим причинам расстройств циркадных биоритмов относят следующие:
Патогенез
Регуляция внутренних циркадных ритмов человека подчинена сложному молекулярному механизму, включающему 9 основных «часовых» генов-регуляторов. Они способствуют выработке транскрипционных факторов, активации казеинкиназ, белков криптохромов, отвечающих за улавливание уровня освещенности. Важную роль играют гены, стимулирующие выработку мелатонина и способствующие реализации эффектов гормона.
В норме все вещества работают сообща, поддерживая циркадный цикл, который регулируется с помощью обратной связи. Но при резком изменении внешних суточных ритмов (часовых поясов), постоянном воздействии освещения в ночное время (работа по сменам, несоблюдение гигиены сна), происходит десинхронизация естественных циркадных ритмов. В головном мозге снижается продукция мелатонина, возникают функциональные патологии ЦНС.
Симптомы
Нарушения циркадных ритмов имеют сходные клинические признаки: бессонница ночью, патологическая сонливость днем, нарушения работоспособности и концентрации внимания, связанные с депривацией сна. Как правило, наблюдаются головные боли, беспричинные перепады настроения, многих больных беспокоят необъяснимая тревожность, нервозность. Иногда бывают нарушения пищеварения, перебои в работе сердца.
Джетлаг (jet lag)
Наиболее ярко симптомокомплекс проявляется при джетлаге (резкой перемене часовых поясов). Нарушения циркадных ритмов беспокоят человека от 2-3 дней до нескольких недель. Чем больше разница во времени между исходной точкой и местом текущего пребывания, тем сильнее выражены признаки. Тяжелее переносятся поездки на восток с переносом засыпания на более раннее время, тогда как к путешествиям на запад организм адаптируется довольно быстро.
Инсомния при посменной работе
В этом случае интенсивность симптомов нарушения биоритмов зависит от количества рабочих смен за месяц, их продолжительности, графика ротации. Самые тяжелые проявления отмечаются при нефиксированной работе с хаотичным чередованием смен и ротации «против часовой стрелки». К тому же часто пациенты сознательно меньше спят, чтобы проводить время с семьей, участвовать в общественной жизни.
Синдром нарушения фаз сна
Такой тип нарушений характеризуется нормальным качеством ночного отдыха в сочетании с несоответствием между физиологическим графиком и желаемым режимом дня. У молодых людей в основном встречается отстроченное наступление фазы сна, из-за чего они ложатся поздно ночью, а потом с трудом просыпаются утром на учебу или работу. Пожилые, наоборот, страдают от опережающей фазы, слишком ранних пробуждений.
Обычно трудностей с засыпанием в «своем ритме» не возникает, что отличает состояние от типичной бессонницы. Основная проблема нарушений фаз сна заключается в необходимости подстраиваться под общепринятый распорядок, вследствие чего больные испытывают постоянную нехватку отдыха, в рабочее время они страдают проблемами с мышлением, памятью, концентрацией внимания.
Осложнения
При длительном нарушении суточных ритмов на 7-10% снижается содержание лептина (гормона сытости), возрастает показатель грелина (гормона голода). Это чревато перееданием, ожирением, к чему более подвержены женщины вследствие особенностей обмена веществ. Хронический недосып снижает иммунную защиту организма, увеличивает риск развития сахарного диабета, сердечно-сосудистых заболеваний.
Еще одна опасность циркадных нарушений в том, что люди с этой проблемой часто не обращаются за медицинской помощью, пытаясь справиться с ситуацией самостоятельно. Пациенты прибегают к алкоголю, снотворным и седативным препаратам для облегчения засыпания, а для повышения работоспособности днем принимают психостимуляторы. В результате патология усугубляется зависимостью от психоактивных веществ.
Диагностика
Главным этапом в постановке диагноза десинхронизации биоритмов является детальный расспрос страдающего инсомнией: сбор жалоб, информации о профессиональной деятельности, частоте путешествий. К обследованию зачастую привлекается несколько врачей — неврологи, психиатры, сомнологи, профильные специалисты по соматическим заболеваниям. В план диагностики включаются:
Лечение нарушений циркадного ритма
Терапия нарушений суточных ритмов представляет собой сложную задачу. Наилучший вариант борьбы с проблемой — устранить провоцирующий фактор, если это возможно (перейти на должность со стандартным рабочим днем, ограничить дальние перелеты). Однако в большинстве случаев больным не подходят радикальные меры, либо триггер невозможно полностью исключить. В такой ситуации используется несколько направлений лечения:
По показаниям могут назначать другие медикаментозные средства (снотворные, психостимуляторы, адаптогены). В каждом конкретном случае подбирается персонализированная схема применения препаратов, чтобы устранить негативную симптоматику и при этом не усугубить циркадные расстройства. Дозировки и график приема лекарств тщательно контролируются неврологом.
Прогноз и профилактика
Циркадные нарушения довольно сложно поддаются лечению, однако при комплексном подходе, комбинации препаратов и немедикаментозных способов удается синхронизировать биоритмы. Менее благоприятный прогноз для пациентов с нейродегенеративными патологиями, которые не подлежат коррекции. Профилактика включает соблюдение гигиены отдыха, правильную организацию трудового процесса, регулярные профосмотры людей, занятых на посменной/вахтовой работе.
Сон и старение I: «Часы в мозге» и влияние генов на ритм жизни
Сон и старение I: «Часы в мозге» и влияние генов на ритм жизни
Эпифиз вырабатывает «гормон сна» мелатонин ночью, а солнечный свет тормозит его образование. Мелатонин — главный регулятор циркадных ритмов, управляющих распорядком дня человека.
Автор
Редакторы
Новая неделя, новый день, новый год. Время жизни разбито на отрывки разной длительности, и все эти отрывки повторяются. Каждые несколько часов нам хочется есть. Каждый вечер мы ложимся спать. Каждые четыре недели организм женщины вырабатывает яйцеклетку. Большинство процессов, происходящих с нашим телом, циклично, и одни циклы завязаны на другие. И хотя старение организма периодическим процессом не назовёшь (ведь никто не молодеет!), его ход напрямую зависит от биоритмов человека, в частности, от цикла сна и бодрствования. Доказательства этому находятся и на уровне поведения, и на уровне отдельных органов, клеток и генов.
Старение и долголетие
Цикл статей, задуманных в рамках спецпроекта «биомолекулы» для фонда «Наука за продление жизни».
В этом цикле рассмотрим общие проблемы старения клеток и организмов, научные подходы к долголетию и продлению здоровой жизни, связь сна и старения, питания и продолжительности жизни (обратимся к нутригеномике), расскажем про организмы с пренебрежимым старением, осветим темы (эпи)генетики старения и анабиоза.
Конечно, феномен старения настолько сложен, что пока рано говорить о радикальных успехах в борьбе с ним и даже о четком понимании его причин и механизмов. Но мы постараемся подобрать наиболее интересную и серьёзную информацию о нащупанных связях, модельных объектах, разрабатываемых и уже доступных технологиях коррекции возрастзависимых нарушений.
Краткое содержание спецпроекта освещено в видеоролике «Стареть или не стареть? // Всё как у зверей». Подробности же узнаете из наших статей.
Следите за обновлениями!
Часы в мозге
Как показывает практика, механизмы смены сна и бодрствования можно объяснить даже детям — «„Проснись!“ — „Усни. “ — „Проснись!“ — „Усни. “ — „Проснись!“» [1]. — Ред.
У дрозофил нашли подобие «гена сна», что описано в статье «Бессонные ночи дрозофилы» [2]. Чисто теоретически это может привести к тому, что потребностью во сне можно будет управлять, но вряд ли мы это когда-то увидим. — Ред.
Есть предположение, что изначально (много миллионов лет назад) циркадные ритмы помогали организмам не умирать от кислорода, которого в тот момент в атмосфере стало аномально много для тогдашних обитателей планеты — «Прообраз биологических часов» [3]. — Ред.
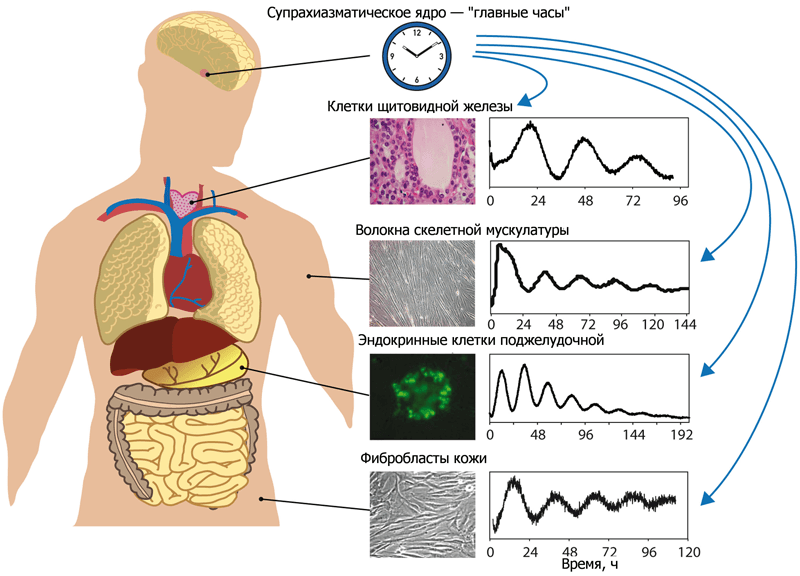
Рисунок 1. Влияние супрахиазматического ядра гипоталамуса на работу различных клеток организма. Функционирование клеток всех типов тканей подчиняется центральному ритму, который задаёт супрахиазматическое ядро гипоталамуса. Оно «следит» за тем, чтобы сигналы от нервной и эндокринной систем приходили к клеткам в одно и то же время — фактически, синхронизирует их. Кстати, то же можно сделать и вне организма: выращивая в культурах несколько образцов различных тканей человека, можно эти культуры синхронизировать, если имитировать сигналы SCN. Такая синхронизация активности культур различных типов клеток одного и того же человека представлена на графиках.
В ходе исследований посмертных срезов мозга здоровых пожилых людей выяснилось, что с возрастом нейроны SCN дегенерируют. Изменяется и структура LC. Кроме того, активность лобных долей коры значительно падает с возрастом (и степень снижения этой активности напрямую отражается на интеллекте), что показано в исследованиях фМРТ [4]. Всё это приводит к тому, что со временем у людей исчезают острые пики активности при бодрствовании. То есть пожилые, конечно, бодрствуют, но внимательность и скорость мышления у них не так хороши, как раньше. Вероятно, причина этого — постепенное ухудшение работы мозговых регуляторов сна и бодрствования.
У пожилых по сравнению с молодыми эффективность сна снижена. С этим может быть связана старческая сонливость, возникающая даже тогда, когда человек определённо выспался. Судя по всему, возрастное падение качества сна не вызвано какими-то конкретными патологиями, это просто часть обычного процесса старения. Впрочем, так ли неизбежно само старение, вопрос.
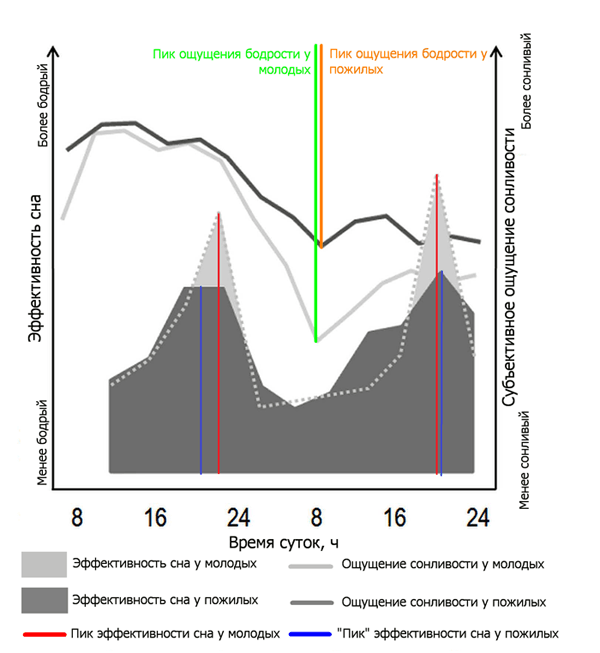
Кроме того, старые хуже переносят вынужденный пропуск сна. Это показали эксперименты, в ходе которых 12 мужчин возрастом 21–31 год и 11 мужчин возрастом 61–70 лет не спали 40 часов (рис. 2). У пожилых субъективное ощущение сонливости было сильнее, чем у молодых, да и внимание из-за недосыпа падало заметнее [5].
Другой эксперимент с такой же длительностью провели в 2005 году [6]. Его результаты тоже представлены на рисунке 2 (закрашенные серым области). В нём двум группам участников-мужчин (опять пожилым и молодым) нужно было в течение 40 часов то спать по 75 минут, то бодрствовать по 150 минут, притом делать это по расписанию. Такой искусственный режим должен был выявить, насколько сон у людей одной возрастной группы более эффективен, чем у испытуемых из другой группы. Нетрудно догадаться, что молодые во время эксперимента и после него чувствовали себя лучше, чем пожилые, потому что лучше высыпались.
Рисунок 2. Субъективное восприятие качества сна и бодрствования у молодых и пожилых мужчин во время 40-часового эксперимента по лишению сна [5], а также эффективность сна во время эксперимента с множеством эпизодов сна [6]. Пожилые раньше начинают чувствовать сонливость, и субъективно она проявляется сильнее (тёмно-серая линия). Молодые более устойчивы к депривации сна (светло-серая линия). Кроме того, субъективно сон молодых (светло-серые закрашенные области) более эффективен, чем сон пожилых (тёмно-серые закрашенные области).
«Гены циркадных ритмов» и старение
Работа любого органа — это, в конечном счёте, работа его генов. Наши «внутренние часы» — не исключение. В супрахиазматическом ядре экспрессируется ряд генов, малоактивных в других частях мозга и тела вообще. Среди таких генов BMAL1 (он же MOP3 и ARNT3), CLOCK и NPAS2 [7], [8]. Эти гены были выявлены в исследованиях с помощью нокаутных мышей — таких, которым методами генной инженерии нарушили работу одного или нескольких генов.
Как правило, продолжительность жизни у грызунов с одним или несколькими выключенными «генами периодичности» снижена. В частности, мыши с неработающим BMAL1 живут меньше своих собратьев. Под конец жизни у них проявляются все характерные признаки старения: их органы уменьшаются в размерах, теряется мышечная масса и подкожный жир, развивается старческая катаракта, повышается содержание активных форм кислорода в тканях [9]. При постоянной нехватке белков BMAL1 и CLOCK ухудшается память, снижается интеллект: животные хуже обучаются и быстрее забывают новую информацию [10].
BMAL1 и CLOCK действуют по-разному: если «выключить» работу гена CLOCK, не затрагивая BMAL1, жизнь мышей претерпевает менее глобальные изменения. Средний срок жизни грызунов без CLOCK на 15% короче, чем у животных дикого типа, а преждевременное старение проявляется у них только в изменении структуры кожи и развитии катаракты [11].
Вот один из примеров связи циркадных ритмов с обменом веществ в целом: «Найдена связь между обменом веществ и циркадным ритмом» [12].
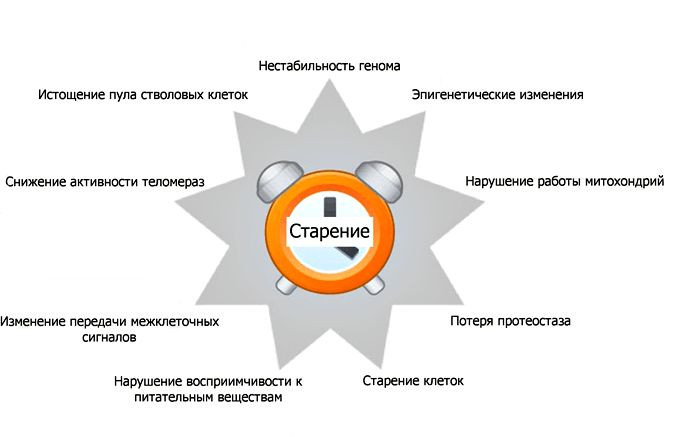
Рисунок 3. Примеры проявлений старения на клеточном уровне. Подробное объяснение этих проявлений дано ниже в тексте в виде нумерованного списка.
Исследования обычно проводятся на больших группах животных, и данные по этим животным усредняются. Но мы-то помним, что каждый организм имеет свой уникальный геном, и от того, как гены в его составе взаимодействуют между собой, зависит очень многое. У двух мышей может быть нарушена работа одного и того же CLOCK, но на уровне отдельных органов и организма в целом это нарушение проявится у них совершенно по-разному. Да даже если с вариантами генов всё в порядке, два организма не будут стариться одинаково. Дело в том, что роль в силе и характере изменений сна с возрастом играет и генотип конкретного организма. Это было подтверждено исследованиями на мышах [23], [24], в которых качество сна грызунов оценивали по элетроэнцефалограммам, а также смотрели, как с возрастом у этих грызунов ухудшается зрение.
У грызунов линии C57BL/6 чаще других с возрастом развивается катаракта, а значит, почти пропадает зрение. Видимо, поэтому под старость (в возрасте примерно год) эти сумеречные животные всё более активны в светлое время суток и всё менее активны в темноте. Кроме того, пожилые C57BL/6 бодрствуют дольше остальных, а AKR/J дольше всех спят. Больше всего времени в стадии REM-сна проводят мыши линии DBA/2J, а меньше всего — AKR/J. Если годовалым мышам этих трёх линий некоторое время мешать спать, а потом дать им возможность выспаться, то быстрее всех к своему обычному режиму возвращаются грызуны C57BL/6.
Сон и метаболизм
Мы выяснили, как нарушение работы «генов циркадных ритмов» влияет на состояние отдельных клеток. А как на них действует нарушения сна, столь частые в преклонном возрасте?
Хотя сон считается временем покоя, во время сна очищение нейронов от «отработанных» продуктов обмена веществ происходит быстрее, чем при бодрствовании [26]. Кстати, ночью очищается не только нервная система. Во время сна также усиливается или ослабевает экспрессия ряда генов. В тканях лёгких экспрессия 3% генов различается во сне и при бодрствовании. В тканях сердца таких «сон-зависимых» генов 6%. Во время сна содержание маркеров клеточного стресса в тканях лёгких, сердца и мозга снижено [27].
Возможно, одна из функций сна — избавление организма от отработанных метаболитов и общее восстановление клеток после стресса. Если это предположение окажется верным, оно сможет объяснить некоторые факты. Например, известно, что независимо от национальности у женщин 46–57 лет, имеющих частые жалобы на качество сна, особенно высок риск метаболического синдрома [28]. Впрочем, последнее может быть связано с тем, что в дополнительные часы бодрствования эти женщины едят [29]. А значит, они потребляют больше калорий в сутки, чем женщины без проблем со сном. В пользу этой гипотезы свидетельствует то, что экспериментальное нарушение сна не вызывало у крыс метаболического синдрома [30].
По данным эпидемиологических исследований, депривация (ограничение времени) сна повышает вероятность дислипидемии, диабета 2 типа и нетолерантности к глюкозе (таб. 1).
| Первый автор статьи, ссылка | Год | Число участников | Продолжительность исследования | Результаты |
|---|---|---|---|---|
| Chaput et al. [32] | 2007 | 740 | 3 года | Регулярный сон длительностью менее 6 часов вызывает нарушение толерантности к глюкозе. |
| Mallon et al. [33] | 2005 | 2663 | 12 лет | У мужчин частые пробуждения и короткий сон связаны с повышенной вероятностью диабета. |
| Nilsson et al. [34] | 2004 | 6599 | 14,8 ± 2,4 года | Нарушения сна повышают риск развития диабета. |
| Tuomilehto et al. [35] | 2008 | 2800 | 2 года | Слишком короткий (≤6 ч) или слишком длинный (≥8ч) сон повышают вероятность развития диабета 2 типа у женщин среднего возраста. У мужчин аналогичного эффекта не нашли. |
| Meisinger et al. [36] | 2005 | 8300 | 11 лет | У людей обоих полов сложности с поддержанием сна (частые просыпания и т.п.) повышают риск развития диабета 2 типа. |
| Hayashino et al. [37] | 2007 | 6509 | 6 лет | У взрослых без серьёзных проблем со здоровьем нарушения засыпания связаны с повышенным риском диабета. |
| Kawakami et al. [38] | 2004 | 2649 | 8 лет | Нарушения сна связаны с повышением риска диабета в 2-3 раза. |
| Choi et al. [39] | 2008 | 4222 | 1 год | И слишком короткий, и слишком длинный сон ассоциируются с повышенным риском метаболического синдрома. |
| Gangwisch et al. [40] | 2007 | 8992 | 10 лет | Кратковременный сон может быть важным фактором риска диабета. |
| Xu et al. [41] | 2010 | 10143 | 10 лет | Короткий ночной сон и частый дневной сон связаны с проявлением диабета. |
| Rafalson et al. [42] | 2010 | 1455 | 6 лет | Короткий ночной сон связан с нарушением содержания глюкозы в крови натощак, вызванным резистентностью к инсулину. |
| Yaggi et al. [43] | 2006 | 1709 | 18 лет | И слишком короткий, и слишком длинный сон повышают риск развития диабета. |
| Hall et al. [44] | 2008 | 1214 | Одномоментное исследование | Продолжительность сна связана со степенью риска метаболического синдрома. |
| Facco et al. [45] | 2010 | 189 | В течение беременности | Малая продолжительность сна связана с нарушением толерантности к глюкозе во время беременности. |
| Qui et al. [46] | 2010 | 1290 | В течение беременности | Гестационный диабет (диабет беременных) и нарушение толерантности к глюкозе чаще развиваются у тех, кто мало спит. |
Помимо нарушений метаболизма, ошибок репликации и повышенным по сравнению с нормой процентом гибнущих клеток [30], депривация сна может повлечь за собой негативные последствия для иммунной системы. У пациентов с постоянным недосыпом днём в крови повышается содержание маркеров воспаления — фактора некроза опухолей (TNF), интерлейкинов 1 и 6, а также кортизола [31], [47]. А ведь воспаление идёт рука об руку с повышенным риском множества заболеваний, начиная от инсульта и заканчивая болезнью Альцгеймера. Например, при последней клетки микроглии (это макрофаги в мозге) выделяют заметные количества интерлейкинов 12 и 23 — одних из важнейших сигналов воспаления. В норме этого, разумеется, не происходит, ведь ни болезни Альцгеймера, ни воспаления нет. Судя по всему, команду микроглии вырабатывать факторы воспаления даёт сам бета-амилоид. Далее, при болезни Альцгеймера астроциты (разновидность глиальных клеток, питают и поддерживают нейроны, направляют их рост у зародышей) становятся восприимчивыми к IL-12 и IL-23 (опять же, в норме такого не наблюдается.) Отложения бета-амилоида увеличиваются в размерах, клеток астроглии становится всё больше, а нейронов рядом с ними — всё меньше [48]. Если снизить выработку IL-12 и IL-23 в клетках глии, патология замедлит своё развитие.
Во взаимосвязях воспаления, выделения интерлейкинов и работы астроцитов при болезни Альцгеймера ещё предстоит разобраться, но уже сейчас ясно, что такие взаимосвязи существуют. На самом деле, подобных корреляций выявили уже немало. А о связи нарушений сна и различных заболеваний (нервных, и не только) будет отдельная статья.
Уменьшение светового дня: как меняются биоритмы человека?
Биоритмы или циркадные ритмы – циклические колебания биологических процессов, которые протекают в организме и связаны со сменой дня и ночи. Это важный механизм приспособления, который помогает адаптироваться в окружающей среде. Но как работают биоритмы человека и как они меняются в зависимости от времени года?
Что нужно знать о циркадных ритмах?
Основная задача биоритмов – помощь в реализации своей генетической программы: поиск пищи в наиболее подходящих условиях, своевременное восстановление сил, подготовка к изменениям погоды и времен года.
Организм человека подчиняется биоритмам, причем некоторые из них короткие по периодичности: дыхание, сердечные сокращения. Существуют и долгосрочные, например, подготовка к спячке, перелет птиц, а у человека — менструальный цикл у женщин и др.
Циркадные ритмы связаны с вращением Земли, сменой дня, и они отвечают за многие аспекты жизни. Например, в некоторые дневные часы отмечается лучшая работоспособность, в другие — легче справляться с физической нагрузкой и она даст лучший результат.
Для примера, самая низкая точка концентрации внимания достигается ранним утром, поэтому так много ДТП в промежуток между 3-5 часами утра, причем это не зависит от уровня бодрости водителей и других показателей. Кстати, умственная работоспособность также практически на нуле, поэтому нет смысла засиживаться за работой или учебной до раннего утра.
Главный дирижер биоритмов
Существует так называемые молекулярные часы, совпадающие с природными сутками, но и есть и главный дирижер, который контролирует все процессы. Если естественный период молекулярных часов не совпадает с природными сутками, то именно супрахиазматическое ядро под влиянием световых сигналов извне дает общие команды и синхронизирует эту работу.
Центральные «часы» – это скопление тысяч нейронов и замкнутая система, на выходе которой получаются электрические импульсы. Полученные сигналы из сетчатки глаза о световом дне усиливают эти импульсы или же, наоборот, ослабевают.
Но у незрячих людей эти часы также работают, но четкого периода дня и ночи не возникает.
Импульсы, которые вырабатывают центральные части (ядро, находящееся в гипоталамусе), отправляет сигнал в другие отделы нервной системы, в том числе, и в спинной мозг. Оттуда этот сигнал передается в периферические органы.
Эпифиз или шишковидная железа под действием этого сигнала вырабатывает гормон – мелатонин, являющийся стабилизатором суточных ритмов, и способствующий сну. Поэтому его назначают как снотворное, а также средство, которое поможет смягчить или избавиться от джетлага – сдвига циркадных ритмов, возникающего при резкой перемене часовых поясов, когда разница составляет более 4-8 часов.
Мелатонин и серотонин
Мелатонин вырабатывается из серотонина в темное время суток. Это продуманная система, ведь когда нужно спать, нервное возбуждение излишне, и не поможет полноценному отдыху. Но если человек постоянно засиживается на свету за полночь, то организм лишается положенного мелатонина. Отсюда и формируются соответствующие проблемы.
Но есть и обратная сторона, если мы большую часть времени проводим в темноте, то гормон счастья вырабатывается в меньших количествах, и это лишает положительных эмоций, снижает активность мозга в целом. Нередко развиваются депрессия и ей подобные состояния. Лучший пример – осенняя хандра, ранее этому состоянию не уделяли внимания, но последние исследования изменили ситуацию.
Относительно недавно в медицинском мире появился термин – сезонная депрессия, обоснованная снижением продолжительности светового дня. Большой интерес к проблеме обоснован тем, что в странах, где длительность светового дня не совпадает с активным периодом человека, среди населения высокая распространенность депрессивных состояний с суицидальными наклонностями.
Уменьшение светового дня и биоритмы
На цикл сна и бодрствования воздействует 2 фактора: солнечный свет и выработка мелатонина. Поэтому, чем выше интенсивность солнечного света, тем активнее ведут себя наши внутренние часы. Человек ощущает себя бодрым, полным сил и готовым на любые свершения.
В пасмурный день многие ощущают сонливость, даже говорят «сонная погода». Но даже через тучи пробивается солнечный свет, и его достаточно, чтобы воздействовать на центры сна и бодрствования.
Мелатонин вырабатывается между 21-22 часами, когда на улице уже темно, и сигнализирует организму о том, что наступает ночь и нужно ложиться спать. Так мозг переключается на ночной режим, замедляется работа организма и обменных процессов. Но, с возрастом, а также при наличии других факторов, выработка мелатонина снижается.
Влияет на этот фактор, во-первых, возраст, поэтому некоторые люди начинают испытывать проблемы со сном. Во-вторых, действуют другие факторы: использование гаджетов в постели, наличие в спальне источников света, которые вмешиваются в эти процессы. В третьих, на эти слаженные процессы влияет и время года, погодные условия, и особенности региона проживания, например, белые ночи и др.
С наступлением зимы у большинства людей биологические ритмы смещаются – вслед за восходом солнца. Активное время для продуктивного дня смещается в первую его половину, а когда наступают сумерки, активность снижается. Появляется сонливость и снижение работоспособности. Однако, этого достаточно, чтобы продолжать заниматься делами.
При уменьшении светового дня и формировании депрессии, в крови увеличивается концентрация кортизола – гормона, который вырабатывается надпочечниками, и способен угнетать работу иммунной системы. А это неминуемо ведет к повышенной восприимчивости к инфекционным и другим заболеваниям. Поэтому существует мнение, что короткий световой день – причина вспышек респираторных инфекций в зимнее время года.
Такие изменения объясняются физиологическими изменениями, хоть и предрасполагают к болезням. Однако контролировать этот процесс можно, да и противостоять ОРВИ и гриппу не так сложно, как кажется: активный образ жизни, витаминотерапия, полноценное питание – факторы, которые помогут поддерживать нормальный режим дня и предотвратить болезни.
Будьте здоровы! Питайтесь полноценно и занимайтесь спортом!