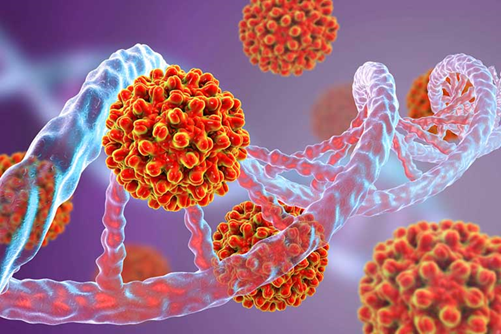
Экспресс-тест на выявление антигена SARS-CoV-2
Экспресс-тест на выявление антигена SARS-CoV-2 – быстрый способ диагностики COVID-19 на ранних стадиях заболевания методом иммунохроматографического анализа.
О тестировании
Иммунохроматографический анализ (ИХА) – качественный анализ, основанный на реакции между антигеном (вещество, определяемое организмом как чужеродное) и соответствующим ему антителом в биологическом материале человека.
Другими словами, исследование методом ИХА выявляет белки вируса, распознаваемые иммунной системой человека.
Чувствительность теста: 84.38%
Экспресс-тест на выявление антигена SARS-CoV-2 относится к основным этиологическим методам лабораторной диагностики новой коронавирусной инфекции, официально одобрен Минздравом РФ и соответствует Временным методическим рекомендациям «Профилактика и лечение новой коронавирусной инфекции (COVID-19)» версия 9 от 26.10.2020 г. и СП 3.1.3597-20 «Профилактика новой коронавирусной инфекции (COVID-19)» с изменениями от 16.11.2020.
Для чего проводится?
Результат экспресс-тестирования на выявление антигена SARS-CoV-2 приравнивается к ПЦР в соответствии с СП 3.1.3597-20 «Профилактика новой коронавирусной инфекции (COVID-19)» с изменениями от 16.11.2020.
Результаты экспресс-теста на выявление антигена SARS-CoV-2 не будут приняты для выписки/закрытия больничного, по возвращении из-за границы. Уточните заранее в организации, куда вы планируете предоставлять результат, подходит ли он или требуется результат ПЦР-диагностики.
Чем отличается от ПЦР-диагностики?
Как и ПЦР, экспресс-тест на антиген позволяет определить наличие в организме новой коронавирусной инфекции на ранних стадиях заболевания, только гораздо быстрее – всего за 15-30 минут.
Преимущества:
Необходимый биоматериал
Мазок из носоглотки и ротоглотки.
Подготовка к анализу
До взятия мазков запрещается:
Как проводится тестирование?
Забор биоматериала проводится двумя стерильными зондами. Мазки берутся со слизистой нижнего носового хода и из ротоглотки. Взятый биоматериал помещается в раствор на несколько минут, после чего 3 капли выделенного образца наносятся на специальную тестовую кассету. Результат оценивается в течение 15-30 минут.
Где проводится:
Результат анализа
Выявляет инфицирование или отсутствие инфицирования непосредственно на момент проведения тестирования:
Стоимость
Экспресс-тест на выявление антигена SARS-CoV-2 в клинике
Экспресс-тест на выявление антигена SARS-CoV-2 на дому
*Цена включает стоимость исследования и забора мазков в амбулатории.
**Цена включает стоимость исследования и забора мазков на дому. Стоимость выезда рассчитывается в зависимости от адреса, дня недели (будний/выходной) и времени (утро/день/вечер) выезда. Окончательную стоимость услуги по вашей заявке уточняйте при записи.
Научная электронная библиотека
Морозова В. С., Габрильянц О. А., Мягкова М. А.,
Глава 4. МЕТОД ИММУНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ НАРКОТИЧЕСКИХ ВЕЩЕСТВ И ИХ МЕТАБОЛИТОВ В РОТОВОЙ ЖИДКОСТИ «ОРАНАРК»
В последние годы на мировом рынке появилось большое количество иммунохроматографических тестов для выявления наркотических веществ в слюне. Это связано с тем, что развитые страны начали активно использовать такие тесты, замещая ими наиболее распространенные ранее ИХА-тесты по моче. Выявление наркотических веществ в слюне незаменимо в случаях, когда необходимо установить состояние наркотического опьянения. Например, в настоящее время в Европе тесты по слюне являются единственно приемлемыми для тестирования на дорогах [1]. Это связано, во-первых, с удобством их использования (неинвазивный метод, исключающий вмешательство в личную жизнь, в отличие от тестов по моче). Во-вторых, тестирование по слюне практически исключает возможность фальсификации результатов анализа или подмены образца (что очень распространено при тестировании по моче). И самое главное, в крови и слюне наркотики появляются сразу после употребления, и остаются там только в течение нескольких часов. В моче же наркотики появляются спустя несколько часов после употребления, и сохраняются до 3-х суток, когда человек уже не находится в состоянии опьянения. Результаты тестов по слюне показывают текущее состояние, когда человек находится непосредственно под воздействием наркотиков и неадекватен в поведении, что неминуемо отражается на способности управлять автомобилем (а также другими видами транспорта, сложными устройствами на производствах и т.п.).
В Европе соблюдение прав человека, в том числе права на использование рекреационных ПАВ во время отдыха, толерантность к людям, потребляющим ПАВ, являются очень важным в обществе. Поэтому здесь переход от тестирования по моче к тестированию по слюне явился основополагающим при проверке водителей на дорогах и в других ситуациях, связанных с определением непосредственного состояния опьянения.
Другие биологические образцы (моча, волосы) также считаются перспективными для различных целей: моча – для определения недавнего факта употребления ПАВ, волосы – для выявления истории наркопотребления данного человека [2].
Как уже было описано в главе 3, разработка иммунохроматографических тестов является сложной высокотехнологичной задачей. Лабораторией иммунохимии ИФАВ РАН совместно с МНПЦ наркологии разработаны экспрессные тест-системы ИХА наркотических соединений в слюне человека «Оранарк» для одновременного определения 4-х классов наркотических веществ и «Дианарк-Ора» – 6 классов наркотических веществ. Диагностические тесты характеризуются методической простотой анализа, высокой производительностью и специфичностью.
Основными иммунореагентами, полученными в ходе разработки иммунохроматографических тест-систем являлись:
1. Растворимые моноклональные антитела к исследуемому антигену, конъюгированные («сшитые») с коллоидным золотом – красителем, который можно легко идентифицировать даже в самых малых концентрациях. Такие антитела нанесены вблизи участка погружения тест-полоски в физиологическую жидкость.
2. Конъюгированные антигены исследуемых веществ с белком-носителем, жестко иммобилизованные в тестовой зоне тест-полоски.
3. Вторичные антитела к моноклональным антителам, жестко иммобилизованные в контрольной зоне тест-полоски.
Иммунореагенты были синтезированы, протестированы, подобраны их оптимальные концентрации.
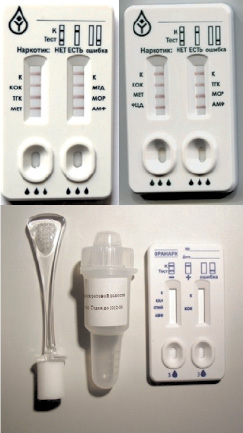
Для создания иммунохроматографической тест-полоски подобраны все необходимые материалы, их размеры и конструкция конечного иммунохроматографического теста. Слюна относится к биообъектам, которые можно собрать в ограниченном небольшом количестве; конструкция такой тест-системы должна позволять использование минимального объема образца. С этой целью используются пластиковые тест-кассеты со встронными в них тест-полосками (рис. 29).
Рис. 29. Тест-системы «Дианарк-Ора» и «Оранарк»
В отличие от тестов для мочи, к тест-системам для анализа слюны предъявляются намного более высокие требования. Моча является жидкой средой, в то время как слюна – вязкой. Поэтому тесты для анализа слюны должны обладать отличными от тестов по моче характеристиками: материал составных частей тест-полоски должен давать большую скорость потока для возможности прохождения по полоске вязкой жидкости. В прокладке для образца сорбируют специальные реагенты, снижающие вязкость образца.
Также следует помнить, что кислотность слюны отличается от кислотности мочи, поэтому при производстве тест-полосок для мочи и для слюны используют различные реагенты для создания оптимальных условий иммунохимической реакции.
При использовании в качестве биообъекта слюны процедура отбора и подготовки пробы к анализу имеют принципиальное значение для успешности всего аналитического процесса. Первоначально необходимо обеспечить идентичность объекта исследования, чтобы результаты анализа отражали истинное содержание аналита в исследуемом объекте и состояние организма как источника этого объекта. В противном случае результат исследования не только теряет рациональное значение, но и может вызвать негативные последствия: врачебные ошибки, неправомерные последствия, и т.п.
Конструкция пробоотборника для слюны и материал, из которого сделана адсорбирущая часть пробоотборника, значительно влияют на конечный результат анализа. Для исключения этого нежелательного влияния необходимо выбирать материалы и конструкцию пробоотборника, руководствуюсь следующими характеристиками:
1. Способность пористого материала пробоотборника не адсорбировать определяемые вещества. В противном случае часть анализируемого вещества остается в материале пробоотборника, что отрицательно влияет на чувствительность определения.
2. Конструкция пробоотборника, позволяющая собрать и нанести на тест-кассету количество слюны, достаточное для удачного проведения теста.
Часто в качестве пробоотборника предлагается пластиковая пипетка либо стаканчик для сбора слюны. Это наиболее экономичный вариант, однако такой пробоотборник, как правило, не позволяет собрать достаточное количество слюны. Кроме того, процедура сбора слюны является неудобной для обследуемого.
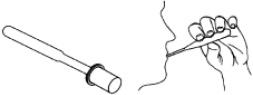
Наиболее удобным для использования и позволяющим получить достаточное количество биоматериала является пробоотборник в виде губки, прикрепленной на пластиковую ручку и отдельный флакон для отжима и хранения образца (рис. 30). Адсорбирующая губка помещается в рот, отбор слюны происходит в течение 1–2 минут до полного впитывания губки. Затем губка помещается во флакон, жидкость отжимается и наносится на тест-кассету.
Рис. 30. Внешний вид пробоотборника и процедура сбора слюны
В результате, иммуногроматографические тест-системы «Оранарк» и «Дианарк-Ора» состоят из 3-х частей:
● пробоотборника: губка цилиндрической формы из адсорбирубщего материала с прикрепленной к ней пластиковой ручкой,
● ёмкости для сбора и хранения образца – ёмкость из бесцветного пластика, состоящая из отделения для хранения образца, перегородки для отжима жидкости ротовой полости и закручивающейся крышки,
● тестового планшета: планшет прямоугольной формы из пластика с двумя тестовыми полосками. В средней части планшета имеется две тестовых зоны прямоугольной формы с маркировками по бокам: К (контроль) и наименованием анализируемых веществ. В нижней части планшета должно находиться два отверстия овальной формы для внесения анализируемого образца (рис. 30).
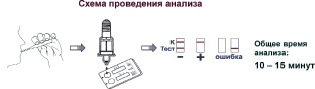
Схема проведения тестирования показана на рис. 31. Она является простой и не требующей лабораторных условий и квалифицированного персонала. Отбор слюны происходит в течение 1–3 минут, а проведение самого теста занимает не более 10 минут. В итоге, вся процедура тестирования занимает 10–15 минут.
Применение иммунохроматографических экспресс-тестов для выявления наркотических веществ в слюне является единственно возможным методом обследования при освиделельствовании на состояние наркотического опьянения, например, при тестировании водителей на дорогах на постах ГИБДД (по аналогии с освидетельствованием на состояние алкогольного опьянения). Используемые иногда ИХА тесты по моче в этом случае неэффективны, т.к. показывают факт употребления наркотиков, который мог иметь место несколько суток назад.
Рис. 31. Схема проведения анализа слюны
с помощью тест-систем «Оранарк» и «Дианарк-Ора»
Преимущества тест-систем «Оранарк» и «Дианарк-Ора» заключаются в следующем:
● Экспресс-тесты по слюне удобны: это неинвазивный метод, исключающий вмешательство в личную жизнь, в отличие от тестов по моче.
● Анализ слюны практически исключает возможность фальсификации результатов анализа или подмены образца, что очень распространено при использовании в качестве биопробы мочи.
● Результаты тестов по слюне показывают текущее состояние наркотического опьянения. В то же время выявление ПАВ в моче дает положительный результат в течение нескольких дней после приема наркотиков.
Предел обнаружения тестов определяется как минимальная концентрацию аналита, при которой он может быть достоверно обнаружен. Для качественных иммунохроматографических тестов процедура определения предела обнаружениязаключается в следующем. Для каждого аналита готовили растворы определяемого вещества различных концентраций, близких к предполагаемому значению предела обнаружения. Каждый полученный стандартный раствор исследовали с помощью разработанного ИХА 30 раз. Для каждой концентрации определяли количество положительных и отрицательных результатов теста. Предел обнаружения определяли как концентрацию аналита, при которой процент положительных результатов теста равен или более 50 %. Полученные результаты определения предела обнаружения представлены в табл. 7.
Чувствительность иммунохроматографических тестов
«Оранарк» и «Дианарк-Ора»
Как работает экспресс-тест на коронавирус
Тестирование на COVID-19 не только помогает получать информацию о распространенности вируса, но также дает представление о том, как вирус распространился и накопил ли он потенциально значимые мутации. Многие методы тестирования основаны на анализе нуклеиновых кислот. Хотя эти подходы бесценны и позволяют определить активную инфекцию, они не дают полной картины. Как мы можем узнать, заразился ли кажущийся здоровым пациент вирусом? Что, если бы у этого человека не было симптомов носительства, и его обследовали после того, как инфекция прошла? Ответы на эти вопросы может помочь получить экспресс-тест на антитела к коронавирусу.
Что такое экспресс-тест на коронавирус и в чем его отличие от ПЦР
В рамках борьбы с патогенами ваша иммунная система вырабатывает антитела к патогену. Даже после того, как вирус был уничтожен, ваше тело продолжает вырабатывать эти антитела как своего рода иммунную «память», которая дает нам записи о прошлой инфекции. Диагностика с помощью экспресс-теста основана на выявлении этих антител. На данный момент используется иммуноферментный анализ (ИФА), который проводится только в условиях лаборатории, и иммунохроматографический анализ (ИХА), представляющий собой тест-полоску или кассету, на которую наносится капля крови.
Молекулярное тестирование, включая тестирование с помощью полимеразной цепной реакции (ПЦР), выявляет генетический материал вируса и, таким образом, может определить, инфицирован ли человек SARS-CoV-2 в настоящее время. Серологический анализ, к которым относятся экспресс-тесты, выявляет антитела к вирусу, измеряя количество антител, вырабатываемых после инфицирования, тем самым выявляя, был ли человек ранее инфицирован SARS-CoV-2. Серологические тесты не следует использовать для диагностики острой инфекции SARS-CoV-2, поскольку антитела вырабатываются через несколько недель после заражения.
Что такое IgA, IgG, IgM
Серологические тесты, к которым относится экспресс-тест, — это тесты на основе крови, которые можно использовать для определения того, подвергались ли люди воздействию определенного патогена, по их иммунному ответу. Напротив, тесты ПЦР, которые в настоящее время используются во всем мире для диагностики случаев COVID-19, могут указывать только на присутствие вирусного материала во время инфекции и не указывают, был ли человек инфицирован и впоследствии выздоровел. Эти тесты могут дать более подробную информацию о распространенности заболевания в популяции путем выявления людей, у которых выработались Ig к вирусу.
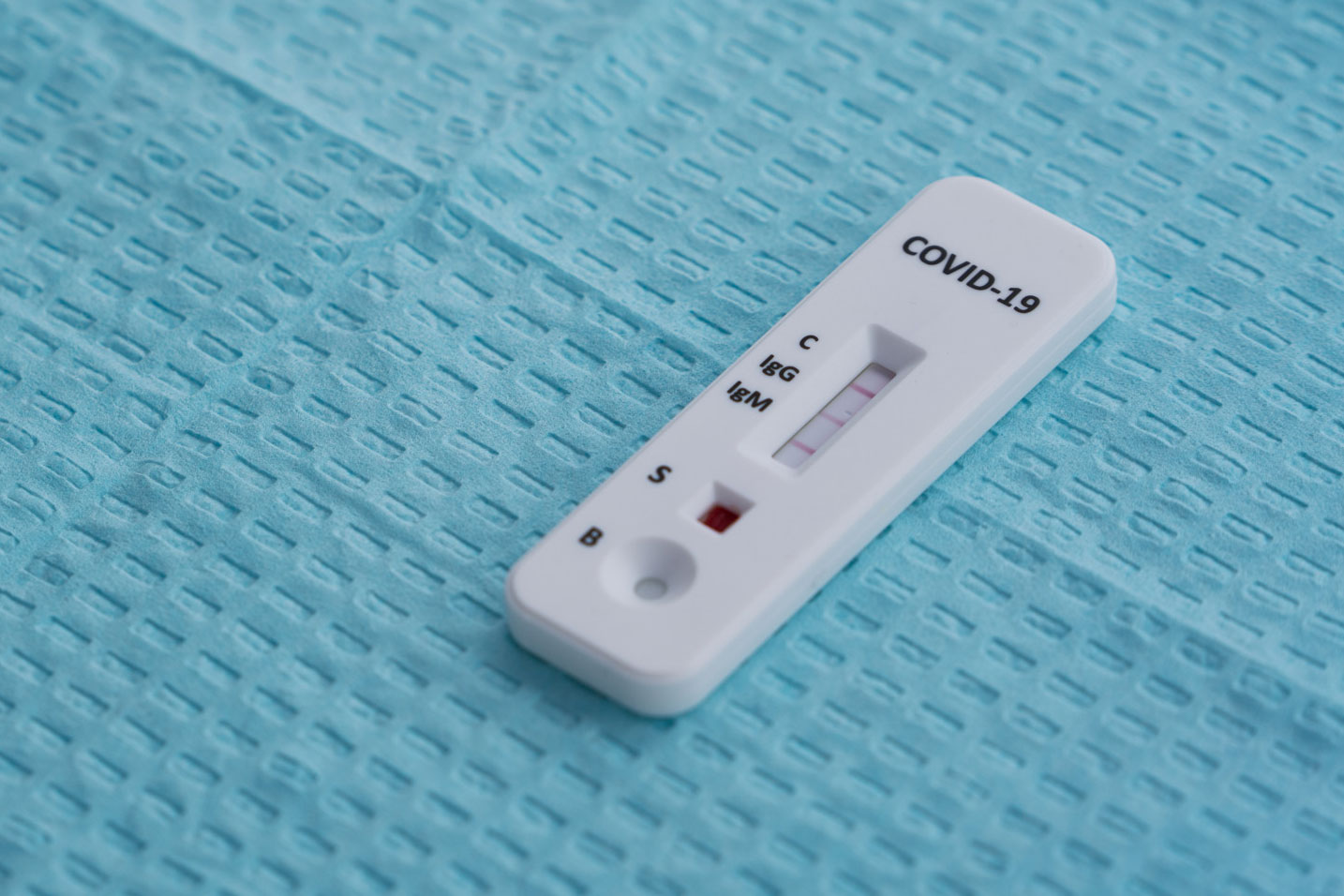
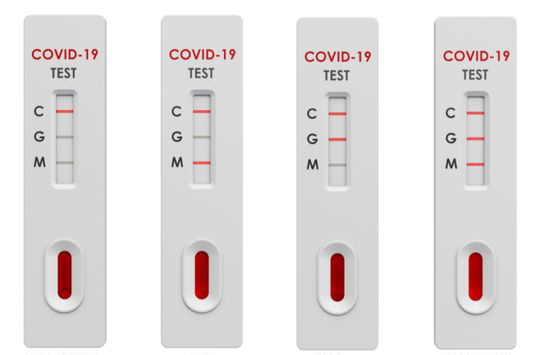
Экспресс-тесты используется для выявления следующих антител:
Тестирование на все три Ig улучшило информативность результатов по сравнению с любым тестом на одно антитело. Этот тип теста на COVID-19 подтверждает, были ли вы ранее инфицированы SARS-CoV-2. Это исследование не подтверждает, что вы полностью невосприимчивы к COVID-19, поскольку в настоящее время нет доказательств того, что люди не могут заразиться коронавирусом более одного раза. Кроме того, тест на Ig к COVID-19 не показывает, инфицированы ли вы в настоящее время коронавирусом. Если вы хотите узнать, инфицированы ли вы в настоящее время COVID-19, вам нужно пройти диагностику методом ПЦР.
Как интерпретировать результаты экспресс-теста?
Проведение экспресс-тестирования — возможность получить достоверные результаты о наличии циркулирующих антител в крови. Есть 4 возможных результата диагностики:
Можно ли делать экспресс-тестирование на ковид дома?
Проведение диагностики с использованием иммунохроматографического анализа возможно и в домашних условиях. Для этого не требуются специальные знания, поскольку к каждому диагностическому набору прилагается краткая инструкция, в которой указано всего несколько действий, позволяющих получить быстрый результат. В большинстве комплектов содержится полоска, пипетка, буферный раствор и скарификатор для прокола кожи. Как правило, исследуемому нужно нанести на полоску каплю крови, а после — несколько капель буфера и подождать, пока уровень жидкости достигнет индикаторов для получения ответа.
С чем связана недостоверность результатов
Негативный результат ИХА экспресс-тестов не всегда отражает реальную картину, поскольку их чувствительность значительно ниже, нежели у ИФА.
Отрицательный результат может означать, что вы:
Кому стоит сделать тест на антитела к коронавирусной инфекции
Экспресс-тест на антитела к коронавирусу — простой метод диагностики, который отличается:
Проведение этого вида диагностики рекомендовано людям, у которых более 5 дней назад наблюдались симптомы ОРВИ, и тем, кто был в контакте в зараженными коронавирусом, но в течение 14 дней симптомы инфекционного заболевания так и не проявили себя.
Что делать, если результат теста положительный
Позитивный результат означает, что на момент тестирования в вашем организме циркулируют антитела, которые образовались в ответ на заражение коронавирусом. Для получения подробных данных о состоянии иммунной системы рекомендуется дополнительно пройти ИФА диагностику для количественного определения антител острой фазы воспаления. Желательно воспользоваться проведением исследования на дому.
Для получения дополнительной информации о том, что нужно делать вам, всем, с кем вы живете, и всем, кто находится в вашем кругу общения, обратитесь за помощью к вашему врачу и после консультации выполните все инструкции, которые он вам предоставил.
Научная электронная библиотека
Морозова В. С., Габрильянц О. А., Мягкова М. А.,
3.2.4. Иммунохроматографический анализ
К иммунохимическим методам относится также метод иммунохроматографического анализа (ИХА, экспресс-тесты) – качественный скрининговый предварительный метод, позволяющий быстро, в течение нескольких минут, провести анализ в любых условиях, в т.ч. «полевых» [17]. Этот метод заслуживает наиболее пристального внимания, т.к. является самым распространенным при выявлении ПАВ и не требует оборудования и специалистов для проведения. Экспресс-тесты используют в химико-токсикологических лабораториях для скрининга, при прохождении медосмотров при устройстве на работу, при тестировании абитуриентов и студентов вузов. Метод может использоваться для тестирования водителей на дорогах, в домашних условиях родителями для контроля детей. Объектами исследования в данном случае являются моча, жидкость ротовой полости, потожировые выделения (редко).
К преимуществам ИХА следует отнести:
● быстроту и легкость в использовании;
● малые объемы образца, отсутствие пробоподготовки;
● дешевизну для производителя и потребителя;
● возможность производства тестов в больших объемах;
● простоту чтения и интерпретации результата;
● высокую чувствительность и вопроизводимость;
● возможность количественного определения;
● возможность использования портативных ридеров, совместимых с компьютером;
В связи с большим количеством преимуществ по сравнению с другими скрининговыми методами, ИХА получил широкое применение
и находится на первом месте на мировом рынке диагностики. ИХА применяется в различных областях медицины и народного хозяйства:
● банки крови и плазмы;
● промышленность (контроль качества, безопасности, идентификация продукта, эко-контроль);
● сельское хозяйство, агрономия;
Тест-полоски для ИХА являются чрезвычайно удобными и простыми в использовании, однако они имеют сложное строение и процесс разработки каждого вида ИХА является чрезвычайно трудоемким и высокотехнологичным.
ИХА-тест (иммунохроматографическия полоска) состоит из следующих основных элементов: пластиковой подложки, на которую наклеены все остальные компоненты теста, фильтра (прокладки для образца), прокладки или мембраны с конъюгатом, хроматографической мембраны, содержащей одну или несколько зон захвата иммунных комплексов и контрольную зону захвата, мембраны абсорбции (впитывающая прокладка) (рис. 13). Тест-полоска может быть помещена в пластиковый корпус, в котором имеется приемное и тестовые «окна».
Рис. 13. Схематическое изображение иммунохроматографической тест-полоски
Метод ИХА, так же как и ИФА, имеет несколько форматов. Наиболее распространены 2 схемы: прямой (сэндвичный) и непрямой конкурентный метод.
В схеме прямого (сэндвичного) ИХА используется конъюгат специфических антител с красящей меткой (в случае визуальной оценки результата), нанесенный на мембрану для конъюгата. На тестовой линии иммобилизованы антитела, специфические к данному аналиту, а на контрольной линии – антивидовые антитела, специфические к первичным антителам. При нанесении образца, содержащего анализируемое вещество, на мембране с конъюгатом происходит связывание аналита с конъюгатом Ат-метка. Затем иммунный комплекс попадает в тестовую зону, где он связывается со специфическими антителами, образуя «сэндвич» Ат-Аг-Ат-метка. избыток несвязавшегося конъюгата связывается с антивидовыми антителами на контрольной линии. Таким образом, выявление 2-х линий на тест-полоске является положительным результатом теста. При отсутствии аналита в образце конъюгат связывается с антивидовыми антителами только на контрольной линии, образуя одну линию на тест-полоске (рис. 14).
Рис. 14. Схема прямого (сэндвичного) ИХА
Метод прямого ИХА используется для выявления высокомолекулярных соединений – вирусов, в т.ч. ВИЧ; различных гормонов (например, в тестах на беременность), возбудителей инфекционных заболеваний.
Схема сэндвичного ИХА не подходит для определения низкомолекулярных веществ, т.к. для образования сэндвича Ат-Аг-Ат антиген должен иметь по крайней мере две антигенные детерминанты (т.е. центра связывания с антителами). Кроме того, из-за стерических затруднений образование такого двойного комплекса с низкомолекулярным антигеном маловероятно. Поэтому для анализа небольших молекул, в том числе наркотических веществ, используется другая схема – непрямой конкурентный ИХА.
Метод конкурентого ИХА основан на конкуренции аналита и иммобилизованного конъгата аналит:белок-носитель за ограниченное количество центров связывания специфических антител, содержащихся в конъюгате Ат-метка. При нанесении образца, содержащего аналит, он связывается с конъюгатом Ат-метка на мембране с конъюгатом (рис. 15). Далее иммунокомплекс проходит через тестовую зону, где на иммобилизован конъгат аналит:белок-носитель. Иммунокомплекс не может связаться с этим конъюгатом из-за стерических затруднений: низкомолекулярные соединения обычно имеют одну антигенную детерминанту и, соответственно, антитела имеют один центр связывания с антигеном, который уже является занятым аналитом. Далее иммунный комплекс связывают антивидовые антитела, находящиеся на контрольной линии. В результате, отсутствие окрашенной полосы в контрольной зоне свидетельствует о том, что концентрация определяемого вещества в исследуемом образце превышает его пороговое значение для данного теста.
При отсутствии анализируемого вещества в образце конъюгат Ат-метка связывается с конъюгатом Аг:белок-носитель, иммобилизованным в зоне тестовой линии. Несвязавшийся конъюгат Ат-метка попадает в зону контрольной линии и связывается там с антивидовыми антителами. Таким образом, наличие двух окрашенных линий (тестовой и контрольной) является отрицательным результатом анализа (рис. 15). Формат конкурентного ИХА используется для выявления низкомолекулярных соединений, в том числе метаболитов наркотических соединений в моче, жидкости ротовой полости, экстрактах тканей.
Схема оценки результатов ИХА наркотических веществ представлена на рис. 16. Результат теста является недействительным при отсутствии контрольной линии, т.к. этот факт может свидетельствовать о незавершенной процедуре анализа, либо о том, что иммунохимическая реакция не прошла должным образом по какой-либо причине (из-за испортившихся иммунореагентов или несоблюдения инструкции по применению теста).
Рис. 15. Схема конкурентного ИХА
Рис. 16. Схема оценки результатов ИХА метаболитов наркотических веществ
Часто, особенно в случаях когда недоступны большие количества биообразца для анализа, например, для определения наркотических веществ в слюне, используются тест-полоски в пластиковой кас-
сете (рис. 17).
Рис. 17. Пластиковый корпус иммунохроматографического теста
В качестве меток в ИХА используются различные частицы, обладающие следующими свойствами:
1. Красящие вещества (нано-частицы коллоидного золота или углерода, или частицы окрашенного латекса). В этом случае используется визуальная детекция результата, либо приборное рефлектометрическое определение (например, сканирование). Использование различных красящих меток, присоединенных к частицам латекса, позволяет проводить мильтианализ, в котором линии разного цвета соответствуют различным аналитам. Наиболее часто используемой меткой является нано-частицы коллоидного золота, которые образуют линии темно-бурого (или темно-розового) цвета.
2. Флуоресцентные, фосфоресцентные и биолюминисцентные метки, ковалентно связанные с частицами латекса. Эти метки используются только в приборных вариантах ИХА, когда результат регистрируется специальным ридером. Среди вышеуказанных наиболее распространены флуоресцентные метки.
3. Парамагнитные метки (также закрепленные на частицах латекса). Данный вид меток используется в ИХА с применением приборов, регистрирующих силу магнитного поля.
4. Ферментные метки используются по тому же принципу, что и в ИФА. Ферментативная реакция регистрируется с помощью окрашивания субстратов, и результат анализа является визуальным, или считывается с помощью ридера.
5) Новым направлением в разработке различных разновидностях ИХА является использование липосом в качестве носителей различного рода меток (красящих, флуоресцентных, ферментативных, электроактивных и пр.) [17].
Разработка технологических стадий иммунохроматографического анализа является наукоемким, высокотехнологичным и многостадийным процессом: он включает в себя подбор материалов, реагентов и условий проведения анализа на нескольких этапах разработки ИХА. Перечислим основные этапы разработки:
● выбор материалов для производства тест-полосок;
● подбор оптимальных концентраций иммунореагентов: конъюгатов Ат-метка, конъюгатов антиген-белок-носитель, антивидовых антител;
● подбор дополнительных реагентов для предобработки компонентов тест-полоски (позволяет улучшить свойства потока, и тем самым обеспечить лучшую чувствительность теста);
● подбор реагентов и их концентраций для «забивки» мембраны, если это необходимо (позволяет улучшить характеристики анализа и стабильность теста);
● оптимизация условий проведения анализа реальных образцов;
● изучение стабильности тест-системы, выбор условий хранения и упаковки для увеличения срока хранения тестов.
На рис. 18 представлена схема производства иммунохроматографических тестов. На каждом этапе данной технологической схемы должна быть произведен выбор материалов и реагентов, оптимизация условий проведения технологической стадии.
Все компоненты тест-полоски (фильтр, мембрана с конъюгатом, хроматографическая мембрана, мембрана абсорбции, см. рис. 13) приклеиваются на пластиковую подложку. Подложка – это лист, состоящий из пластика и имеющий клейкое покрытие. При выборе подложки необходимо обращать внимание на качество клея (это может напрямую влиять на характеристики хроматографической мембраны, которая будет приклеена на подложку) и удобство покрывающей пленки (что обеспечивает точность приклеивания компонентов полоски на подложку).
При выборе материала фильтра для образца необходимо руководствоваться теми функциями, которые должен выполнять фильтр:
● впитать достаточное количество образца и доставить его в мембрану для конъюгата;
● довести рН образца до оптимального;
● увеличить или уменьшить вязкость образца для достижения оптимальной скорости прохождения образца по хроматографической мембране;
● увеличить способность образца растворить конъюгат;
● уменьшить забивку мембраны за счет добавления забивки в прокладку для образца.
Рис. 18. Схема стадий производства иммунохроматографических тестов
Фильтры выпускаются из различных пористых материалов: целлюлозы, стекловолокна, тканных сит. Мембраны для конъюгатов производят из стекловолокна, целлюлозы, поверхностно модифицированного полиэфира или искусственных волокон. Подложка для конъюгата должна обладать высокой адсорбционной способностью с одной стороны, и легкостью «смывания» конъюгата из данной зоны, с другой. Т.е. при прохождении жидкости конъюгат должен хорошо десорбироваться из мембраны. При этом при сушке мембраны после нанесения раствора конъюгата не должно происходить изменение конформации антител и разрушения структуры конъюгата.
Хроматографическая мембрана – самый важный элемент иммунохроматографической полоски. Именно на ней проходит иммунохимическая реакция, происходит разделение и связывание иммунореагентов в тестовой и контрольной зонах. Мембрана является самой длинной зоной тест-полоски, именно здесь иммунореагенты проходят максимальный путь в латеральном потоке. При выборе материала для хроматографической мембраны необходимо руководствоваться следующими свойствами, которыми должна обладать мембрана:
1. Гидрофильность – необходима для возможности прохождения потока (а это водная среда) через мембрану. Обеспечивается выбором материала, а также использованием ПАВ.
2. Способность связывать белки: для формирования тестовой и контрольной линии на мембране необходимо закрепить белковые конъюгаты таким образом, чтобы они не смылись латеральным потоком. Белки «прикрепляются» к мембране с помощью электростатического взаимодействия: диполи, содержащиеся в нитроцеллюлозе, связывают диполи белков (рис. 19).
Рис. 19. Диполи нитроцеллюлозы и белков
Для лучшего закрепления белков на мембране после нанесения растворов конъюгатов и антител на мембрану используют «забивку» или блокировку мембраны: ее обрабатывают раствором инертного белка, чтобы занять все вакантные поры, в которые могли бы мигрировать молекулы белковых конъюгатов и антител, находящихся на контрольной и тестовой линиях. Кроме того, в растворах белков необходимо использовать буфер с нужной кислотностью, чтобы обеспечить максимальное электростатическое взаимодействие диполей нитроцеллюлозы и белков.
При производстве мембран для ИХА используются следующие материалы: нитроцеллюлоза (наиболее распространенный материал, используется в 99 % выпускаемых тест-полосок); нейлон; поливинилиденфторид; полиэфирсульфон; стекловолокно.
При выборе материала мембраны необходимо руководствоваться следующими ее физическими параметрами, которые характеризуют свойства латерального потока, проходящего через данную мембрану:
● толщина мембраны, ее объем слоя;
● пористость, размер и распределение пор;
● номинальная скорость потока;
● прочность (предел прочности на разрыв);
● качество поверхности: неровности, порошок и пыль, оставшиеся на поверхности после производства материала.
Все перечисленные характеристики формируют в конечном итоге главный параметр иммунохроматографической мембраны – скорость латерального потока, определяющий все основные параметры ИХА (рис. 20).
Рис. 20. Влияние скорости потока на характеристики анализа
Все вышеописанные подробности приведены для того, чтобы дать представление о сложности процесса разработки и производства на первый взгляд простых тест-полосок. Для того чтобы получить действительно работающий качественный тест, необходимо очень тщательно пройти все стадии разработки и наладки производства. К сожалению, не все нынешние производители это делают на должном уровне, экономя средства для достижения минимальных цен на рынке. В результате мы имеем общепринятое мнение о неточности ИХА тестов. В то же время качественный ИХА тест может иметь характеристики не хуже, чем тест-система для приборного метода ИФА [17].
Современные материалы и возможности тщательного подбора условий при производстве ИХА тестов позволяют разработать даже количественные варианты ИХА. В этом случае детекция результата осуществляется с помощью специальных считывающих устройств – ридеров для ИХА. В зависимости от типа метки, данные устройства осуществляют различные способы детекции: рефрактометрический, флуоресцентный, магнитный (рис. 21).

Рис. 21. Считывающие устройства для детекции результатов ИХА
Рис. 22. Автоматическая платформа для производства ИХА полосок
Количественный формат ИХА характеризуется гораздо большими требованиями к качеству тест-полосок, и, следовательно, к контролю качества каждой стадии производства тестов. Кроме качества материалов и реагентов, на каждой стадии производства необходимо четко, с высокой точностью, контролировать температуру, влажность, концентрацию реагентов, скорость подачи материалов, давления прессов и т.д. Только в этом случае можно получить количественный ИХА тест. Столь высокие требования возможно выполнить только с использованием специальных закрытых, полностью автоматизированных платформ, в которых каждый из параметров контролируется и поддерживается с высокой точностью (рис. 22).